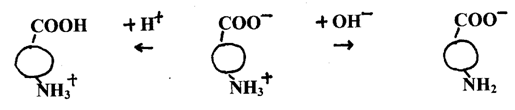Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Высаливание белков сульфатом аммонияВ водном растворе белков их частицы заряжены и гидратированы, что обусловливает устойчивость белковых растворов. Но при высокой концентрации солей, ионы которых тоже гидратируются, происходит разрушение водных оболочек белковых молекул, и снимается заряд с белковой молекулы адсорбирующимися на ней ионами солей. В результате этих двух процессов белковые растворы теряют устойчивость, частицы белка слипаются друг с другом, укрупняются и выпадают в осадок.
Опыт 1.В пробирку наливают 1 мл раствора белка, добавляют равный объем насыщенного раствора сульфата аммония, встряхивают. Выпадает осадок глобулинов. Раствор фильтруют. Одну часть фильтрата нагревают до кипения и наблюдают свертывание альбуминов, находящихся в растворе. К другой части фильтрата добавляют кристаллический сульфат аммония до насыщения. Появляется муть или хлопья выпадающих в осадок белков альбуминов. Если понизить концентрацию солей добавлением дистиллированной воды, то осадок альбуминов вновь растворится. Объясняется это тем, что осаждение белков определенными солями является обратимым процессом. Из приведенного опыта следует, что для высаливания различных белков требуется разная концентрация одной и той же соли.
Свертывание белков при нагревании
Практически все белки при нагревании подвергаются денатурации. Но особенно быстро белки денатурируют вблизи их изоэлектрических точек (ИЭТ), то есть при том значении рН, когда суммарный заряд молекулы белка равен нулю. В этих условиях на молекулах белков имеется равное количество отрицательно и положительно заряженных групп. Благодаря этому белковые молекулы быстрее свертываются. ИЭТ яичных белков находится в слабо-кислой среде, поэтому добавление к раствору яичного белка небольшого  количества слабой уксусной кислоты ускоряет свертывание белка при нагревании. Добавление к раствору белка нейтральных солей в кислой среде облегчает и ускоряет свертывание белков при кипячении благодаря дегидратации белковых молекул. В кислой среде диссоциация белка по карбоксильным группам подавляется, молекулы заряжаются положительно, а в щелочной среде подавляется ионизация по аминогруппам, белки заряжаются отрицательно. И в том и в другом случае молекулы отталкиваются друг от друга, и осадок не образуется даже при кипячении.
Кислая среда Нейтральная среда Щелочная среда Опыт 2.Наливают в 5 пробирок по 2 мл раствора яичного белка. Раствор в первой пробирке нагревают. Осадок образуется до того, как раствор закипит. Произошла денатурация белка.
Опыт 3. Во вторую пробирку добавляют 1 каплю 1% раствора уксусной кислоты и нагревают. Осадок белка образуется быстрее, так как рН раствора близок его ИЭТ. Опыт 4. В третью пробирку добавляют 1-2 капли 1% раствора уксусной кислоты и несколько капель насыщенного раствора хлорида натрия и нагревают. Осадок белка образуется быстро. В изоэлектрической точке и в присутствии соли денатурация происходит быстрее, чем в опыте 3.
Опыт 5. В четвертую пробирку добавляют 0,5 мл 10% раствора уксусной кислоты и нагревают. В кислой среде все белковые молекулы заряжаются положительно, и осадок белка не образуется даже при кипячении.
Опыт 6. В пятую пробирку добавляют 0,5 мл 10% раствора гидроксида натрия и нагревают. В щелочной среде все белковые молекулы заряжаются отрицательно, и осадок белка не образуется даже при кипячении. Осаждение белков концентрированными минеральными кислотами Белки при взаимодействии с концентрированными минеральными кислотами подвергаются необратимой денатурации и выпадают в осадок. В избытке серной и соляной кислот происходит постепенное растворение первоначально выпавших осадков. Избыток азотной кислоты практически не растворяет осадка белка, поэтому для обнаружения белка в исследуемом растворе пользуются азотной кислотой. Опыт 7.В три пробирки наливают по 2 мл концентрированной азотной, серной и соляной кислот. Затем осторожно по стенке добавляют в каждую пробирку по 1-2 мл раствора яичного белка. Наблюдают образование осадков белков на границе двух жидкостей. При перемешивании осадки, образующиеся при действии соляной и серной кислот, растворяются, а в растворе азотной кислоты осадка образуется еще больше. Осаждение белков органическими кислотами Для осаждения белков часто используют органические кислоты, такие как сульфосалициловая и трихлоруксусная. Трихлоруксусная кислота осаждает только белки и не осаждает продукты распада белков и свободные аминокислоты, поэтому ею часто пользуются для полного удаления белков из биологических жидкостей. Опыт 8. В две пробирки наливают по 2 мл раствора белка и добавляют в первую несколько капель 20% раствора сульфосалициловой кислоты, а в другую – несколько капель 5% раствора трихлоруксусной кислоты. В обеих пробирках наблюдается образование осадков белка. Осаждение белков солями тяжелых металлов Соли тяжелых металлов вызывают необратимую денатурацию белков, образуя с ними нерастворимые в воде соединения. Но при избытке некоторых солей происходит растворение осадка за счет адсорбции ионов солей белковыми частицами. В результате белковые частицы приобретают заряд и вновь растворяются. Растворение осадков денатурированных белков в избытке солей тяжелых металлов называется адсорбционной пептизацией. Способность белков образовывать с солями тяжелых металлов нерастворимые соединения используется при отравлениях этими солями, когда в качестве противоядия применяют молоко или яичный белок. Опыт 9.В две пробирки наливают по 2 мл раствора белка. В одну добавляют несколько капель 10% раствора медного купороса, в другую – несколько капель 5% раствора ацетата свинца. В обеих пробирках белки денатурируют. При добавлении в пробирки избытка солей наблюдается растворение образующихся осадков. |
||
|
Последнее изменение этой страницы: 2018-05-29; просмотров: 1636. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |