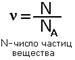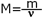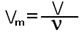Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Понятие о газах. Закон Авогадро. Молярный объем газа. Относительная плотность газов.Моль-это количество вещества, содержащее столько структурных единиц(атомов, молекул, ионов), сколько атомов содержится в 12 г углерода. Обозначается буквой ν(ню) Зная массу атома углерода 1,993·10-26 кг можно вычислить число атомов в 0,012 кг углерода: NA=0,012/1,993·10-26=6,02·1023 Это число называется постоянной Авогодро и обозначается NA Используя эту величину можноопределить количество вещества по формуле:
Молярная масса равна отношению массы вещества к количеству вещества, обозначается буквой М.
Молярная масса рассчитывается так же как и относительная молекулярная масса, но в отличии от неё имеет размерность г/моль. Например М(H2SO4)=1·2+32+16·4=98г/моль.Это означает, что масса 1 моль серной кислоты равна 98 г.
где V-объём газа в л. 3. Допишите уравнения химических реакций, определите тип реакции, расставьте коэффициенты: Са + H2S04= CaSO4 + H2 Р205 + 3Н20= 2H3PO4 Аl203 + 6НСl= 2AlCl3 + 3H2O Билет-9 Водород-простое вещество. Распространение в природе. Положение в ПСХЭ
Самый распространённый элемент во вселенной – 92% от числа всех атомов Водород Н2 – это бесцветный газ, без запаха и вкуса, устойчив к нагреванию до 2000 °С. Практически не растворяется в воде. Получение: Генри Кавендиш впервые получил водород взаимодействием разбавленных серной и соляной кислот с металлами цинком, железом и оловом:  Zn + H2SO4(разб.) = ZnSO4 + H2↑, Zn + 2HCl(разб.) = ZnCl2 + H2↑ В лаборатории для получения водорода используют взаимодействие разбавленных кислот (серной, соляной) с цинком (уравнение реакции см. выше), алюминия с растворами щелочей: 2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2↑ или реакции натрия и гидрида кальция с водой: 2Na + 2H2O = 2NaOH + H2↑ Химические свойства Водород реагирует с неметаллами, металлами, оксидами (обычно при нагревании), например, сгорает в присутствии кислорода и дает воду: 2H2 + O2 = 2H2O реагирует с серой при высоких температурах и образует сероводород: H2 + S = H2S Водород восстанавливает оксид меди до металлической меди: H2 + CuO = Cu + H2O но может быть и окислителем – например, при реакции с металлом кальцием дает гидрид кальция: H2 + Ca = CaH2 В смеси с воздухом водород взрывается, а смесь водорода с кислородом носит название «гремучий газ». Поэтому работа с ним требует большой осторожности. |
||
|
Последнее изменение этой страницы: 2018-06-01; просмотров: 404. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |