
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Молярная масса равна отношению массы вещества к количеству вещества, обозначается буквой М.
Молярная масса рассчитывается так же как и относительная молекулярная масса, но в отличии от неё имеет размерность г/моль. Например М(H2SO4)=1·2+32+16·4=98г/моль.Это означает, что масса 1 моль серной кислоты равна 98 г.
где V-объём газа в л. Отношение масс одинаковых объёмов различных газов при одинаковых условиях равно отношению их молярных масс (поскольку в равных объёмах газов при одинаковых условиях содержится одинаковое число молекул и, следовательно, одинаковое число молей):
Это отношение называется относительной плотностьюD ( или d) одного газа по другому. Относительная плотность газа (D) – показывает во сколько раз один газ тяжелее или легче другого и является безразмерной величиной. Например, DO2 (газа)= Mr(газа)/Mr(O2)=Mr(газа)/32; DH2 (газа)= Mr(газа)/Mr(H2)=Mr(газа)/2; Dвоздуха (газа)= Mr(газа)/Mr(воздуха)=Mr(газа)/29.
3. Осуществите следующие превращения: Ag 1). 4Ag + O2 → 2Ag2O 2). Ag2O + 2HCl → 2AgCI + H2O 3). AgCI + KN03 →AgN03 + KCl
Билет-15 Классификация оснований. Получение. Химические свойства и применение. Основания - это сложные вещества, состоящие из атома металла, связанного с одной или несколькими гидроксогруппами-ОН.По номенклатуре основания называют гидроксидами:
К щелочам относят гидроксиды щелочных и щелочноземельных металлов (LiOH, NaOH, KOH, RbOH, CsOH, Ca(OH)2, Sr(OH)2, Ba(OH)2.Остальные - нерастворимые. К нерастворимым относят так называемые амфотерные гидроксиды, которые при взаимодействии с кислотами выступают как основания, а со щёлочью-как кислоты.  Получение оснований.
Химические свойства оснований.
|
||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-06-01; просмотров: 427. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
|||||||||||||||||||||||||||||||||||||||
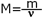
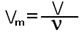
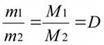
 Ag2O
Ag2O 
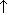 Ba+2H2O=Ba(OH)2+H2
Ba+2H2O=Ba(OH)2+H2