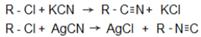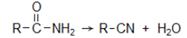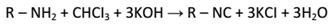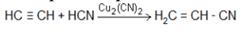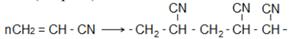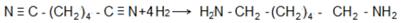Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Отдельные представители (нитробензол, тринитробензол)
Полинитронафталины применяются в качестве взрывчатых веществ.
АМИНЫ Строение. Изомерия. Номенклатура Амины – органические производные аммиака, которые можно рассматривать как продукты замены атомов водорода аммиака на углеводородные радикалы. В зависимости от природы радикала амины могут быть предельными и непредельными, алициклическими, ароматическими и гетероциклическими. В зависимости от числа замещенных на радикалы атомов водорода различают амины первичные –R – NH2, вторичные – R2 – NH, и третичные – R3N. Существование аминов разной степени замещения создает дополнительные возможности для изомерии, увеличивает число возможных соединений. Вспомним, что углеводород бутан имеет два изомера, производящиеся от него спирты – четыре, аминов же с формулой С4H11N имеется восемь. Названия первичных аминов строят из названий углеводородов, добавляя к ним приставку амино-или окончание -амин. Названия вторичных и третичных аминов чаще всего образуют по принципам рациональной номенклатуры, перечисляя имеющиеся в 
Физические свойства Простейшие предельные амины (метиламин (CH3NH2)), диметиламин (CH3)2NH, триметиламин, (CH3)3N, этиламин (C2H5NH2) – газообразные вещества; амины с большим числом атомов углерода – жидкости, а начиная с C12H25NH2 – твердые вещества. Запах
Способы получения 1. Пропусканием паров спиртов и аммиака при 300оС над катализатором (Al2O3, ThO2):
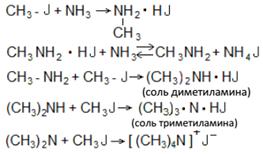
2. Действием аммиака на галогенопроизводные получают смесь различных аминов, т. к. образующиеся в ходе реакции амины (благодаря частичному разложению солей аммиаком) вступают в свою очередь в реакцию с галогеналкилами (Гофман):
Последний продукт рассматривают как сполна замещенное аммониевое соединение и называют иодистым тетраметиламмонием. Эту смесь обрабатывают щелочью и подвергают перегонке с водяным паром. Первичные, вторичные и третичные амины отгоняются с водяным паром, а гидроокись сполна замещенного аммония [(CH3)4N]OH остается в перегонной колбе. Разделение вторичных и третичных аминов производят, пользуясь их различной реакционной способностью по отношению к некоторым сульфохлоридам. 3. Амиды кислот при расщеплении бромной или хлорной щелочью (Гофман) дают амины:
4. Нитросоединения восстанавливаются водородом в присутствии катализаторов с образованием первичных аминов:
5. Нитрилы и изонитрилы при действии восстановителей или водорода в присутствии катализаторов Pt, Ni в зависимости от характера нитрила и условий восстановления дают либо первичные амины, либо вторичные, либо их смесь. Восстановление изонитрилов приводит преимущественно ко вторичным аминам:
Химические свойства Являясь органическими производными аммиака, амины сохраняют главные его химические особенности. Подобно аммиаку, амины проявляют свойства оснований. Это обнаруживается по щелочной реакции водных растворов аминов: 1. 2. С минеральными кислотами амины дают алкилзамещенные аммонийные соли:
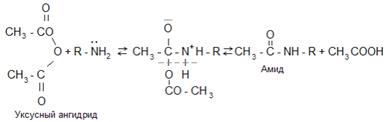
3. Амины способны к алкилированию (см. 2 способ получения). 4. Амины можно ацилировать, в частности ацетилировать. Ацетилирование осуществляют уксусным ангидридом или хлористым ацетилом:
Реакция ацилирования – типичная реакция нуклеофильного присоединения-замещения. Это также, как и электрофильное замещение, осуществляется по гетеролитическому механизму.
В случае нуклеофильного замещения замещаемый атом (или группа атомов) оттягивает пару электронов и уходит с ними; к оставшемуся положительно заряженному карбокатиону присоединяется анион. Нуклеофильным – такой механизм называется потому, что замещение происходит обычно при действии отрицательно заряженной частицы Y, стремящейся к положительно заряженному ядру атома R+, т. е. при действии частицы, «любящей ядро» (дословный перевод слова («нуклеофил» – любящий ядро).
Нуклеофильное замещение обозначается буквами Примером нуклеофильного замещения может служить реакция замещения галогена на гидроксил. В нашем случае:
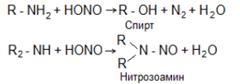
5. Азотистая кислота переводит первичные амины в спирты, вторичные – в нитрозоамины, а с третичными не реагирует:
Ароматические аминыне обладают сильно выраженными основными свойствами. Так, раствор анилина не дает щелочной реакции на лакмус. Наличие основных свойств у ароматических аминов, хотя и выраженных очень слабо, доказывается реакцией образования солей с кислотами, например:
Из двух приведенных солей анилина солянокислый анилин хорошо растворяется в воде, а сернокислый – плохо. Ароматические анилины представляют собой очень слабые основания, что объясняется тем, что в них основные свойства аминогруппы NH2 сильно ослаблены наличием фенильной группы. Они – более слабые основания, чем аммиак. 6. Образование солей. Подобно аммиаку амины, как сухие, и в водных растворах взаимодействуют с кислотами, образуя соли:
7. Представляет интерес, реакция с азотистой кислотой, потому что дает возможность различать первичные, вторичные и третичные алифатические, а также ароматические амины, т. к. они по-разному относятся к действию азотистой кислоты. А.Алифатические амины Первичные амины при действии азотистой кислоты дают спирт
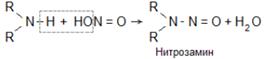
Вторичные амины при действии азотистой кислоты превращаются в нитрозамины:
Нитрозамины представляют собой довольно прочные вещества. Это маслянистые жидкости, имеющие нейтральную реакцию. Б.Ароматические амины При действии азотистой кислоты на соли первичных ароматических аминов образуются диазосоединения, или соли диазония:
Вторичные ароматические амины – как чисто ароматические, так и жирно-ароматические – дают с азотистой кислотой нитрозоамины:
В отличие от третичных аминов жирного ряда третичные амины ароматического ряда взаимодействуют с азотистой кислотой. В этих ароматических аминах атом водорода в бензольном ядре, находящийся в пара-положении к замещенной аминогруппе, отличается большой подвижностью и легко замещается, в частности, нитрозогруппой. Так, при действии азотистой кислоты на диметиланилин получается нитрозодиметиланилин:
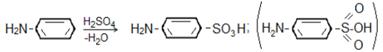
Отдельные представители Метиламин CH3NH2 – газ, tкип = – 6,3оС с запахом похожим на запах аммиака. Содержится в некоторых растениях. Анилин или фениламин – важнейший из ароматических аминов, т. к. служит основным сырьем анилинокрасочной промышленности, а также в производстве ряда важнейших лекарственных и взрывчатых веществ. Анилин – бесцветная жидкость, быстро желтеющая, а затем буреющая на воздухе вследствие окисления. В воде растворяется плохо. Анилин очень ядовит. При нагревании с концентрированной серной кислотой он сульфируется с образованием сульфаниловой кислоты:
Сульфаниловая кислота – HO3S-C6H4-NH2 – твердое вещество, tпл. = 290оС (с разложением) является сырьем для получения сульфамидных препаратов, простейший из которых стрептоцид [амид сульфаниловой кислоты (сульфаниламид)]. Получают:
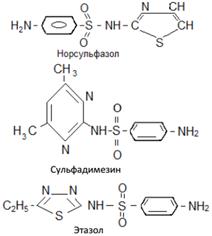
Известны и многочисленные его производные – продукты замещения атома водорода амидной группы на различные органические остатки:
Лекарственное действие сульфамидных препаратов открыто в 30-х гг. прошлого века. С тех пор синтезировано более 6 тысяч соединений этой группы, однако практическое применение получили только около 20 препаратов. Сульфамидные препараты широко применяются для лечения различных инфекционных заболеваний – ангины, менингита, рожистого воспаления, дизентерии. Бесконтрольное применение препаратов может нанести вред здоровью, вызвав тяжелое поражение почек. Дифениламин C6H5-NH-C6H5 – кристаллическое вещество, почти нерастворимое в воде и хорошо растворимое в органических растворителях, получается при нагревании под давлением смеси анилина с гидрохлоридом анилина:
Применяется для получения красителей. Диметиланилин С6H5N(CH3)2 – жидкость, tкип = 194оС – важный промежуточный продукт при синтезе красителей, взрывчатых веществ, проявителей для цветной фотографии. Получается из анилина алкилированием метиловым спиртом:
НИТРИЛЫ И ИЗОНИТРИЛЫ Нитрилы имеют общую формулу
Изомерия. Номенклатура Нитрилы называются по кислотам, в которые они переходят при омылении, или по углеводородам, отвечающим общему числу углеводородных атомов, с добавлением окончания НИТРИЛ. Можно также их рассматривать как цианистые алкилы:
Изонитрилы, или карбиламины, называются по радикалам, а по систематической номенклатуре – как производное углеводорода с прибавлением окончания КАРБИЛАМИН.
Способы получения Способы получения нитрилов и изонитрилов в соответствии с их различным строением сильно отличаются. 1. При взаимодействии с галогеналкилами соли синильной кислоты и щелочных металлов дают преимущественно нитрилы, а соли серебра – изонитрилы:
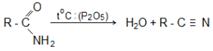
2. Амиды кислот при дегидратации превращаются в нитрилы:
Для первичных аминов характерна так называемая изонитрильная реакция: при нагревании первичных аминов с хлороформом в присутствии едкого калия образуются изонитрилы, которые обнаруживаются по неприятному запаху:
Вторичные и третичные амины не дают этой реакции, следовательно, она может быть использована для открытия первичных аминов. Физические свойства Низшие нитрилы (до С11) – жидкости со слабым эфирным запахом CH3CN и C2H5CN – растворимы в воде. Температура кипения их близка к температуре кипения соответствующих спиртов с тем же числом углеродных атомов, например:
Отдельные представители Ацетонитрил CH3 – CN, tкип = 82ºС, получается дегидратацией ацетамида:
Применяется как растворитель и как исходное вещество в различных синтезах. Акрилонитрил CH2 = CH – CN получают из ацетилена:
Это жидкость, tкип = 78 ºС со слабым приятным запахом. Акрилонитрил применяют для получения синтетического волокна акрилона (нитрона):
и для производства дивинил-нитрильного синтетического каучука, обладающего масло- и бензостойкостью.
ДИАМИНЫ Соединения, содержащие две аминогруппы в молекуле, называются диаминами:
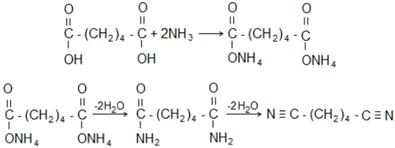
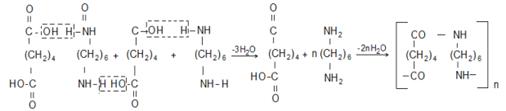
Диамины могут быть получены теми же способами что и моноамины: восстановлением нитросоединений, взаимодействием аммиака с дигалогенидами, восстановлением динитрилов. Низшие диамины растворимы в воде и являются более сильными основаниями, чем моноамины. Гексаметилендиамин в промышленности получают из адипиновой кислоты. Аммонийная соль этой кислоты подвергается дегидратации с образованием диамида адипиновой кислоты и затем ее динитрила:
Каталитическим восстановлением динитрила адипиновой кислоты получают гексаметилендиамин:
Поликонденсацией адипиновой кислоты с гексалметилендиамином получают полиамиды с довольно высокой температурой плавления, способные в размягченном состоянии вытягиваться в чрезвычайно плотные нити – синтетическое волокно по красоте,
В этих продуктах – поликонденсационных смолах – полиметиленовые цепи – (CH2)4 – и – (CH2)6 – связаны амидными группировками – CO – NH –, характерными для белковых веществ, к которым относятся шерсть и натуральный шѐлк. |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 650. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
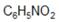 Нитробензол – бесцветная жидкость (примеси окрашивают в желтый цвет), tкип = 211º С; р = 1,203 г/см3. Производится в больших количествах в промышленности и используется главным образом для восстановления в анилин С6Н5NН2.
Нитробензол – бесцветная жидкость (примеси окрашивают в желтый цвет), tкип = 211º С; р = 1,203 г/см3. Производится в больших количествах в промышленности и используется главным образом для восстановления в анилин С6Н5NН2.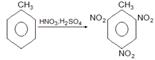 Тринитробензол (тротил) – твердое вещество, tпл = 80 ºС – одно из самых распространенных взрывчатых веществ. Ценным свойством тротила
Тринитробензол (тротил) – твердое вещество, tпл = 80 ºС – одно из самых распространенных взрывчатых веществ. Ценным свойством тротила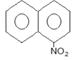 α – нитронафталин, твердое вещество, tпл = 61 ºС.
α – нитронафталин, твердое вещество, tпл = 61 ºС.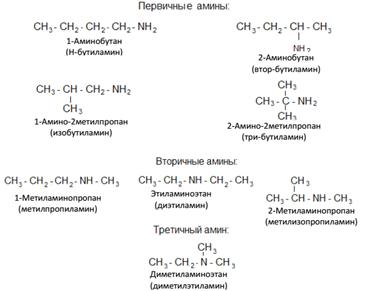
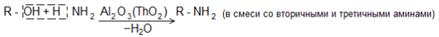
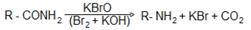
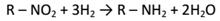
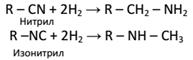
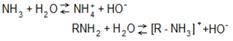
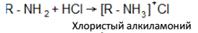
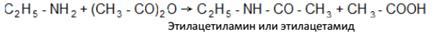
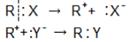
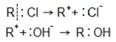
 .
.
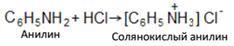
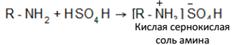
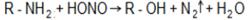
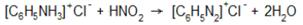
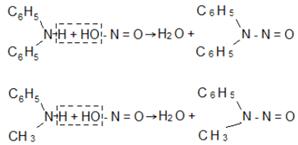
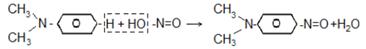
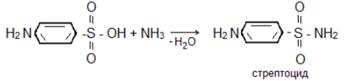
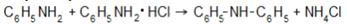
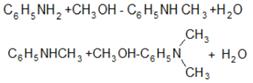
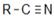 , а изонитрилы:
, а изонитрилы: