Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Отдельные представители (щавелевая кислота, молоновая кислота, янтарная кислота, адипиновая кислота, фталевая кислота, терефталевая кислота)
Щавелевая кислота способна окисляться до СО2 и воды:
На этом основано ее применение в качестве восстановителя и для установления титра марганцовокалиевой соли. При нагревании выше температуры плавления, в присутствии концентрированной H2SO4 происходит разложение щавелевой кислоты:
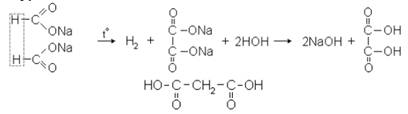
В технике щавелевую кислоту получают: 1) окислением древесных опилок кислородом воздуха при нагревании их с расплавленным едким калием или смесью едких калия и натрия; 2) при быстром нагревании до 400 ºС калиевой или натриевой соли муравьиной кислоты:
Молоновая кислота – кристаллическое вещество с tпл. = 135,6 ºС.
Диэтиловый эфир молоновой кислоты, называемый обычно молоновым эфиром обладает высокой химической активностью и способен к ряду интересных химических превращений. Молоновый эфир представляет собой жидкость с приятным фруктовым запахом. Он применяется при ряде синтезов лекарственных веществ, например при получении барбитала.
Янтарная кислота – твердое кристаллическое вещество с tпл = 182,8 ºС. В технике получается гидрированием малеиновой кислоты и из природной смолы – янтаря путем сухой перегонки. Янтарную кислоту можно применять в реакциях поликонденсации с гликолями; некоторые эфиры янтарной кислоты служат пластификаторами. 
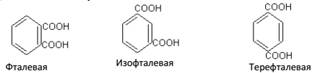
Фталевые кислоты При окислении ароматических углеводородов, содержащих в молекуле две боковые цепи, в зависимости от расположения боковых цепей могут быть получены три изомерные дикарбоновые кислоты, называемые фталевыми:
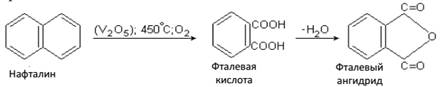
Фталевая кислота – кристаллическое вещество, tпл = 206 –208ºС (с разложением), растворима в горячей воде. Ее получают окислением нафталина. Практически сразу получается фталевый ангидрид.
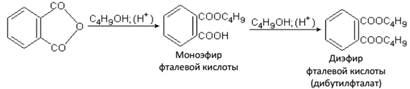
Широкое применение в качестве пластификаторов для пластических масс нашел диэфир фталевой кислоты дибутилфталат, его получают:
При взаимодействии с аммиаком фталевый ангидрид образует имид фталевой кислоты – фталимид:
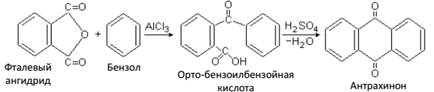
Фталимид – твердое вещество, служит исходным веществом для технического синтеза ценного красителя индиго и ряда других соединений. При конденсации фталевого ангидрида с бензолом в присустствии хлористого алюминия получается антрахинон, широко применяемый в производстве красителей (промышленный способ).
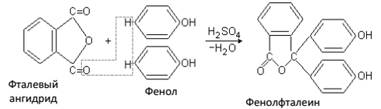
Фталеины – продукты конденсации фталевого ангидрида с фенолами. Важным представителем группы фталеинов является фенолфталеин – индикатор широко применяемый в аналитической химии:
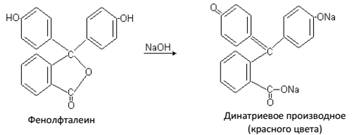
Фенолфталеин – белое кристаллическое вещество, хорошо растворимое в спирте. Под действием щелочей фенолфталеин переходит в соль ярко-малинового цвета:
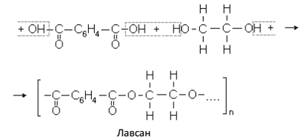
Терефталевая, или n-фенилкарбоновая, кислота (изомер фталевой кислоты) применяется в большом количестве для синтеза ценного волокна – лавсан (терилен). Лавсан – полиэфир, получаемый конденсацией терефталевой кислоты и этиленгликоля:
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 879. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
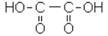 Щавелевая кислота встречается в виде солей во многих растениях, например в щавеле и кислице. Она кристаллизуется из воды в виде дигидрата (СOOH)2 ·2H2O с tплав. = 101,5 ºС. Кристаллизационная вода удаляется медленной сушкой при 110–120 ºС. Безводная кислота плавится при 189 ºС.
Щавелевая кислота встречается в виде солей во многих растениях, например в щавеле и кислице. Она кристаллизуется из воды в виде дигидрата (СOOH)2 ·2H2O с tплав. = 101,5 ºС. Кристаллизационная вода удаляется медленной сушкой при 110–120 ºС. Безводная кислота плавится при 189 ºС.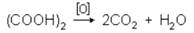
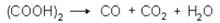
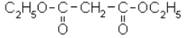
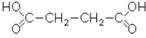 Янтарная кислота, этандикарбоновая кислота или бутандионовая кислота содержится в янтаре, в буром угле, во многих растениях, особенно много ее в недозрелых фруктах.
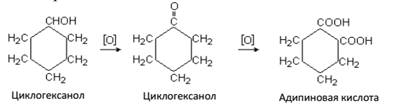
Янтарная кислота, этандикарбоновая кислота или бутандионовая кислота содержится в янтаре, в буром угле, во многих растениях, особенно много ее в недозрелых фруктах.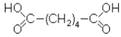 Адипиновую кислоту – белое кристалическое вещество с tпл = 153 ºС в больших количествах приготовляют окислением азотной кислотой циклогексанола. Используют для производства волокон – капрона и найлона.
Адипиновую кислоту – белое кристалическое вещество с tпл = 153 ºС в больших количествах приготовляют окислением азотной кислотой циклогексанола. Используют для производства волокон – капрона и найлона.