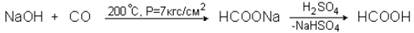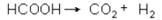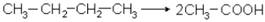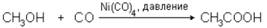Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Отдельные представители (муравьиная кислота, уксусная кислота)
Муравьиная кислота – едкое вещество: капли ее вызывают на коже пузыри. Применяется при крашении тканей в составе закрепителей при омеднении выкрасок, полученных при крашении прямыми азокрасителями (HCOO)2Cu. В промышленности муравьиную кислоту получают нагреванием окиси углерода с порошкообразным едким натром с последующей обработкой образовавшегося формиата натрия разбавленной серной кислотой:
Технический продукт после перегонки представляет собой 85%-ю муравьиную кислоту. Муравьиная кислота отличается рядом особенностей. Под влиянием водоотнимающих веществ муравьиная кислота разлагается. Эта реакция используется для получения чистой окиси углерода:
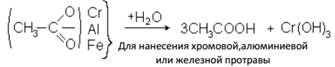
Уксусная кислота CH3COOH широко распространена в природе: содержится в выделениях животных (моче, желчи), в растениях (в зеленых листьях), образуется при брожении, скисании вина, пива, содержится в кислом молоке и сыре. Безводная уксусная  В красильной промышленности используют способность уксусной кислоты гидролизоваться:
Уксусная кислота в промышленности производится окислением ацетальдегида кислородом воздуха в присутствии марганцевых катализаторов, уксуснокислым брожением жидкостей, содержащих этиловый спирт. Последний способ относится к биохимическим (микробиологическим) процессам. Под влиянием «уксусного грибка», зародыши которого всегда присутствуют в воздухе, содержащие спирт жидкости «скисают», образуя натуральный уксус. 1. Процесс сложен, но суммарно уравнение реакции можно записать так:
Натуральный уксус содержит около 5 % уксусной кислоты. Из него путем фракционной перегонки приготавливают уксусную эссенцию, используемую в пищевой промышленности для консервирования овощей, грибов, рыбы. 2. Сухая перегонка древесины. Способ сейчас имеет значение лишь для утилизации отходов лесотехнической промышленности. 3. Из углеводородов нефти – прямым окислением бутана (200 ºС; 50 кгс/см2):
4. Из метилового спирта оксосинтезом в присутствии тетракарбонилникеля Ni(CO)4:
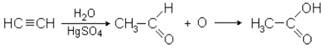
5. Из ацетилена по реакции Кучерова получают уксусный альдегид (ацетальдегид), который окисляют далее в уксусную кислоту.
Особое место среди жирных кислот занимают высокомолекулярные кислоты:
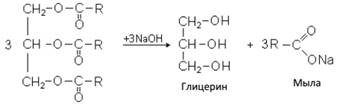
Глицериды этих кислот являются главной составной частью природных жиров и масел. В настоящее время большие количества высших жирных кислот получают окислением парафина. Окисление проводят, продувая воздух через расплавленный парафин в присутствии окислов марганца при 100 ºС. После промывки низкие кислоты С1 – С4 переходят в раствор, откуда их выделяют отгонкой. Высшие жирные кислоты C5 – C22 нейтрализуют, после чего выделяют действием серной кислоты и затем разгоняют. Из 1000 кг парафина получается 50–60 кг низших и 600–700 кг высших кислот. Получаемые из нефти жирные кислоты используют в технике. Из них изготовляют мыла, смазочные материалы для защиты металлов, применяют в горно-рудной и металлообрабатывающей промышленности, при изготовлении резины, линолеума, лакокрасочных изделий.
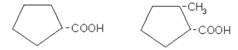
Нафтеновые кислоты, кислоты нефти, открыты М. В. Марковниковым в 1892 г. Природная нефть содержит небольшое количество (до 1 %) этих кислот. Главным образом это алициклические кислоты с пятичленным циклом – циклопентанкарбоновая
При очистке нафтеновых продуктов щелочью образуются натриевые соли этих кислот, обладающие моющей способностью, так называемый мылонафт.
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 372. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
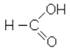 Муравьиная кислота, или метановая кислота, – простейший представитель класса кислот. В свободном состоянии встречается в организме и едких выделениях муравьев, жгучей крапиве и в небольших количествах в моче и поте животных.
Муравьиная кислота, или метановая кислота, – простейший представитель класса кислот. В свободном состоянии встречается в организме и едких выделениях муравьев, жгучей крапиве и в небольших количествах в моче и поте животных.