Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Двухатомные и трёхатомные спирты.Спирты - это производные углеводородов, в которых один или несколько атомов водорода замещены на гидроксильные группы В зависимости от количества гидроксильных групп различают одноатомные и многоатомные спирты (двухатомные, трехатомные.). Двухатонмные спирты: Наиболее известны СН2ОН-СН2ОН - этандиол СН2ОН-СНОН-СН3 - пропандиол-1,2 СН2ОН-СН2-СН2ОН - пропандиол-1,3, Трехатомные спирты: глицерин СН2-СН -СН2пропантриол1,2,3 ОН ОН ОН Получение:. Гидролиз ди- и тригалогеналканов. ,. СH2Cl-CH2Cl + 2NaOH →CH2OH-CH2OH + 2NaCl этиленгликоль СH2Cl-СHCl-CH2Cl + 3NaOH →CH2OH-CHOH-CH2OH + 3NaClглицерин 2. Гидратация оксида этилена. Основной промышленный способ получения этиленгликоля. (CH2-CH2)O + H2O →CH2OH-CH2OH 4. Глицерин в основном получают гидролизом (омылением) жиров.
Глицерин. ХИМ св-ва. 1)Взаимодействие с галогеноводородами, пентахлоридом фосфора, тионилхлоридом. приводит к замещению гидроксигрупп спиртов на галоген. СH2OH-CHOH-CH2OH + 3SOCl2 →СH2Cl-CHCl-CH2Cl + 3SO2 + 3HCl 1,2,3-трихлорпропан 2). При нагревании глицерина в присутствии водоотнимающих средств образуется акролеин - непредельный альдегид, имеющий запах кухонного газа. Это одна из качественных реакций на глицерин. СH2OH-CHOH-CH2OH →CH2=CH-COH + 2H2O 3).
4)
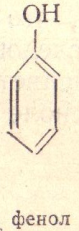
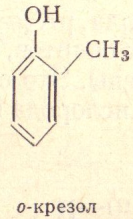
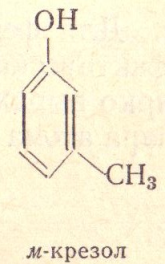
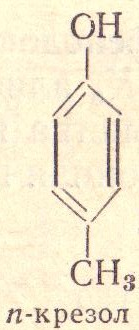
Это производные аромати ческих уг леводородов, у которых гидрок сильная группа связана непоср едственно бензольным ядром.
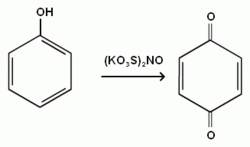
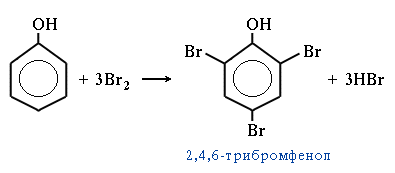
Хим. Св-ва 1.Кислотные свойства фенолов. 1)диссоциа ция с образованием ионов Н+, C6H5OH →С6Н5O- + H+ 2) щелочными металлами и щело чами стойкие феноляты 2C6H5OH + 2Na →2С6Н5ONa + H2; С6H5OH + NaOH →С6Н5ONa + H2O 3)с кисло тами, Феноляты C6H5ONa + HCl →С6Н5OH + NaCl 4) с ан- гидридами карбоновых кислот, Фенолы образуют сложные эфирыС6H5OH + CH3СOCl →С6H5-O-CO-CH3 + HCl  Фенилацетат 5) Фенолы обра зуют простые эфиры при взаи модействии с галогеналканами испиртами. С6H5ONa + C2H5I →С6H5-O-C2H5(фенетол) + NaI; С6H5OH + CH3OH →С6H5-O-CH3 (анизол)+ H2O Окисление фенолов идет да же на воздухе, Реакции замещения в бензольном ядре. 1)Взаимодействие фенолов с бром ной водой.Гидроксильная группа фенола ориентирует бром в орто- и параположения
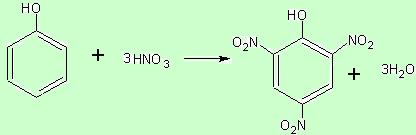
2)Нитрование фенола идет в орто- и пара-положения
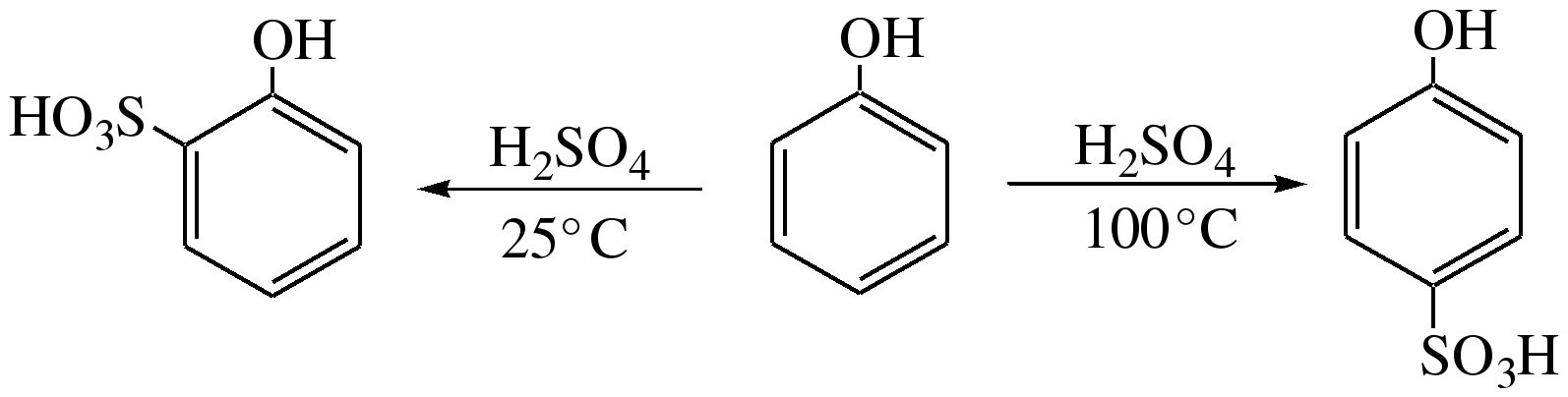
(2,4,6 тринитрофенол(пикриновая кислота)) 3) Сульфирование
Получение фенолов. Кислотные свойства фенолов Это производные аромати ческих углеводородов, у которых гидроксильная группа связана непосредственно бензольным ядром. Кислотные свойства фенолов.1)диссоциация с образованием ионов Н+, C6H5OH С6Н5O- + H+ 2) щелочными металлами и щело чами стойкие феноляты 2C6H5OH + 2Na →2С6Н5ONa + H2; С6H5OH + NaOH →С6Н5ONa + H2O 3) с ангидридами карбоновых кислот, Фенолы образуют сложные эфирыС6H5OH + CH3СOCl →С6H5-O-CO-CH3 + HCl Фенилацетат 5) Фенолы обра зуют простые эфиры при взаи модействии с галогеналканами испиртами. С6H5ONa + C2H5I →С6H5-O-C2H5(фенетол) + NaI; С6H5OH + CH3OH →С6H5-O-CH3 (анизол)+ H2O Получение: 1. Перегонкой каменноугольной смолы. 2. Синтез из бензола, через промежуточный продукт хлорбензол. C6H5Cl + 2NaOH →C6H5OH + NaCl 3. Кумольный метод одновременно получаются 2 ценных продукта - фенол и ацетонC6H6 + CH2=CH-CH3 →C6H5-CH(CH3)2 (кумол) 4. Сплавление солей сульфо кислот со щелочами. Образую щийся фенолят натрия разрушают кислотами.C6H5-SO3K+KOH→C6H5OH + K2SO3 5. Гомологи фенола получают алкилированием фенола.C6H5+CH3Cl→C6H5OCH3+HCl |
||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 732. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
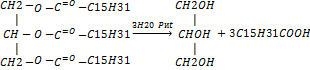
 17)Фенолы и их свойства.
17)Фенолы и их свойства.