
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Алкены и их химические свойства.ненасыщенные углеводороды с открытой цепью. Они имеют общую формулу СnН2n,где n -число атомов углерода, что совпадает с общей формулой циклоалканов.Поэтому алкены и циклоалканы являются меж классовыми изомерами. В алкенах имеется одна двойная связь. Окончание -ен является характерным для названийалкенов. С2Н4 или СН2=СН2 - этен (этилен) ;С3Н6 – пропен (пропилен) С4Н8 - бутен (бутилен) Химические св-ва:А)Реакции присоединения,которые идут за счет разрыва пи-связей 1. Реакция гидрирования CH2=CH2 + H2 →СH3-CH3 2. обесцвечивание бромной водыCH2=CH2 + Вr2 →СH2Br-CH2Br (1,2-дибромэтан) 3 (гидрогалогенирование)., CH2=CH2 + НВr →СH3-CH2Br (бромэтан) 4) СH2=CH2 + H2O →CH3-CH2-OH; Б)Окисление1)горение C2H4 + O2→CO2+H2+Q 2)окисление
(Этандиол,этиленгликоль) В)полимеризация(соединение одинаковых молекул nCH2=CH2→(-CH2-CH2-)n (полиэтилен) Диеновые углеводороды. Особенности реакции присоединения в зависимости от положения двойных связей. Это непредельные углеводороды, в молекулах которых присутствуют две двойные связи. Общая формула алкадиенов СnH2n-2 a) кумулированными – обе двойные связи принадлежат одному атому углерода СH2=C=CH2 - пропадиен CH2=C=CH-CH3 - бутадиен-1,2 б) сопряженными (конъюгиро ванными) - разделены одной простой связью СH2=CH-CH=CH2 - бутадиен-1,3; CH3-CH=CH-CH=CH2 - пентадиен-1,3 в) изолированными - разделены двумя и более простыми связями CH2=CH-CH2-CH=CH2 - пентадиен-1,4 Реакцииприсоединения.1) CH2=CH-CH=CH2(бутандиен 1.3) + Br2 →СH2Br-CH=CH-CH2Br (1,4-дибромбутен-2) CH2=CH-CH=CH2 + Br2 →СH2Br-CHBr-CH=CH2 1,2-дибромбутен-1 СH2=CH-CH=CH2+Br2 (избыток) →СH2Br-CHBr-CHBr-CH2Br (тетрабромбутан) По правилу Морковникова: атом водорода присоединяется к более гидрированному атому углерода.  Алкины. Ацетилен и его химические свойства. CnH2n-2 . Простейший алкин ацетилен, СН≡СН - ацетилен (этин ); CH3-С≡СН - метилацетилен (пропин) CH3-CH2-С≡СН - бутин-1 (этилацетилен) CH3-С≡С-CH3 -диметилацетилен(бутин-2) CH3-CH2-СН2-С≡СН,пентин-1 1) Реакции присоединения ,идут за счет разрыва пи-связей, 1,Постепенное присоединение СН≡СН + H2 →СH2=CH2 + H2 →СH3-CH3 2. Галогенирование (например реакция обесцвечивание бромной воды). СН≡СН + Br2 →СHBr=CHBr (1,2-дибромэтен) + Br2 →СHBr2-CHBr2 1,1,2,2-тетрабромэтан 3.присоединение воды(реакция Кучерова) СН≡СН + H2O →СH2=CH-OH( виниловый спирт) →СH3-COH уксусный альдегид(ацетальдегид) 2)Окисление. а)горение СН≡СН + О2 →C+CO+H2 Б)каталитическое СН≡СН 3)Полимеризация -n СНСН →(СH=CH-)n полиацетелен-чередование двойной и одинарных связей 4)2CH≡CH→CH≡C-CH=CH2 5) CH≡CH→(400t,Cакт)→С6Н6 Получение непредельных углеводородов. Алкинов1) из алканов при высокой температуре (1200 -1500о)метан,этан 2CH4 →CH≡СН + 3H2 ; 2C2H6 →CH≡СН + 2H2 2) из дигалагенопроизводных CH2Cl-CH2Cl →(NaOH/t*)→CH≡CH + 2НCl 3) из карбида кальция СаС2(карбит кальция) + Н2О C2H2 + Ca(OH)2гашенная известь4)Разложением ацетиленидов кислотами СаС2 + 2HCl C2H2 + CaCl2 Алкенов.1) из алкановCH3-CH2-CH3=(t*,кат)CH3-CH=CH2 + H2(I) 2)из галаге нопрозводных алканов При этом соблюдается правило Зайце ва(.отщепление атома водорода в реакциях происходит преимущест венно от наименее гидрогенизиро ванного атома углерода) CH3-CH2Br + KOH→(t) →CH2=CH2 + KBr + H2O3) издигалагенопрозводныхалкановCH2Br-CH2Br + Zn →CH2=CH2 + ZnBr2 4)изспиртовCH3-CH2-OH→ (t*,Н2SО4) →CH2=CH2 + H2OАлкодиенов 1) изалкановCH3-CH2-CH2-CH3 →(t*,кат)→СH2=CH-CH=CH2 + 2H2 (бутандиен) 2)изэтиловогоспирта2C2H5OH =(t*)_ СH2=CH-CH=CH2 + H2 + 2H2O3)СН2=СН-СН2-ОН→(-Н2О)→СН2=С=СН2 4)СН2=СН-С≡СН→(+Н2)→СН2=СН-СН=СН2 Качественные реакции на двойную, тройную связь. На двойную связь а)обесцвечивание бромной водыCH2=CH2 + Вr2 →СH2Br-CH2Br (1,2-дибромэтан) б) Обесцвечивание перманганата калия в водной и кислой среде при пропускании через неё алкена.(окисление алкенов) CH2=CH2(этилен) =( KMnO4,НОНводный раствор,{O})=CH2OH-CH2OH этандиол(этиленгликоль), На тройную связь а)р-ии с хлоридом меди CuCl+HC≡CH+СuСl+NH3→ Сu-C≡C-Cu+2NH4Cl (ацетилинит меди) коричневое окрашивание. Б)галагинирование (реакция обесцвечивание бромной воды).СН≡СН + Br2 →СHBr=CHBr+ Br2 →СHBr2-CHBr21,1,2,2-тетрабромэтан |
||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 453. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
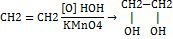
 НOOC-COOН щавелевая кислота
НOOC-COOН щавелевая кислота