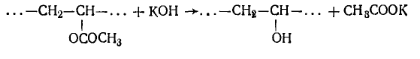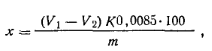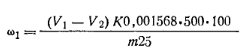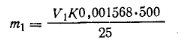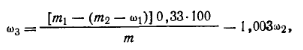Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
ПОЛИВИНИЛОВЫЙ СПИРТ, ЕГО СЛОЖНЫЕ ЭФИРЫ И ПОЛИВИНИЛАЦЕТАЛИ
Поливиниловый спирт (ГОСТ 10779—78) представляет собой белый порошок, растворимый в воде и нерастворимый в органических растворителях. Это единственный полимер, который нельзя получить полимеризацией мономера, так как виниловый спирт в свободном состоянии не существует, а изомеризуется в ацетальдегид. В технике поливиниловый спирт получают омылением спиртового раствора поливинилацетата в кислой или щелочной среде. Поливинилацетат — прозрачное беcцветное вещество плотностью 1,19 г/см3, растворим во многих органических растворителях: спиртах, ацетоне, ароматических углеводородах, четырех-хлористом углероде. Получают поливинилацетат полимеризацией винилацетата. Поливинилацетали (производные поливинилового спирта)— важные технические продукты, получаемые в результате конденсации поливинилового спирта с альдегидами. Технические поливинилацетали всегда содержат кроме ацетальных групп незамещенные гидроксильные группы и некоторое количество ацетатных групп. Наличие небольшого количества ацетатных групп обусловлено присутствием этих групп в техническом поливиниловом спирте. Максимальная степень замещения гидро-ксильных групп составляет 86,47 мол.долей, %, поэтому поливинилацетали всегда содержат не менее 13,53 мол. долей, %, свободных гидроксильных групп. Промышленное применение получили ацетали формальдегида (ГОСТ 10758—75), ацетальдегида, масляного альдегида (ГОСТ 9439—85) и смешанные поливинилацетали. Работа 1. Определение молярной доли ацетатных групп в поливинилацетате.Ацетатные группы в поливинилацетате определяют, омыляя его спиртовым раствором гидроксида калия: 
Избыток гидроксида калия оттитровывают соляной кислотой.
Реактивы н оборудование
Гидроксид калия, 0,5 н. спиртовой Бикс дли взятия навески раствор (приготовление см. разд. 8.3, Колба коническая на 250 мл с при работа 6) шлифованным шариковым холодиль- Соляная кислота, 0,5 н. раствор никои Фенолфталеин, 1%-ный спиртовой раствор
Ход определения. В коническую колбу емкостью 250 мл помещают ~0,2 г полимера, взвешенного с точностью до 0,0002 г, вливают 25 мл 0,5 н. спиртового раствора гидроксида калия, присоединяют к колбе обратный холодильник и нагревают смесь на кипящей водяной бане в течение 3 ч при периодическом взбалтывании. После охлаждения раствор титруют 0,5 н. раствором соляной кислоты в присутствии фенолфталеина до розовой окраски. Параллельно в тех же условиях проводят контрольный опыт. Молярную долю ацетатных групп х(%) в поливинилацетате вычисляют по формуле
где v1— объем 0,5 н. раствора соляной кислоты, пошедший на титрование в контрольном опыте; v2— объем 0,5 н. раствора соляной кислоты, пошедший на титрование пробы; К— коэффициент поправки для 0,5 н. раствора соляной кислоты; 0,0295 — массовое количество ацетатных групп, соответствующее 1 мл 0,5 н. раствора соляной кислоты; m — масса навески поливинилацетата.
Работа 2. Определение молярной доли гидроксильных групп в поливиниловом спирте.Гидроксильная группа является основной функциональной группой поливинилового спирта.-Наиболее распространенный метод ее определения — этерификация гидроксильных групп поливинилового спирта фталевым ангидридом в присутствии пиридина. Реакция идет по схеме
Реактивы и оборудование
Фталевый ангидрид, раствор в пи- Бюкс для взятия навески ридине
Гидроксид натрия, 0,5 н. раствор Колба круглодонная на 250 мл с пришлифованным шариковым холодильником Фенолфталеин, 1%-ный спиртовой раствор Цилиндр мерный на 50 мл
Ход определения.Навеску 0,1 — 0,2 г поливинилового спирта, взятую с точностью до 0,0002 г, помещают в круглодонную колбу емкостью 250 мл, приливают из бюретки с краном 25 мл свежеприготовленного раствора фталевого ангидрида в пиридине (20 г фталевого ангидрида растворяют в 200 мл пиридина), соединяют колбу с пришлифованным обратным холодильником и нагревают горелкой на асбестовой сетке в течение 3 ч. По окончании реакции, не охлаждая колбы, через верх холодильника вливают 50 мл дистиллированной воды, нагревают 5 мин, затем раствор охлаждают и титруют 0,5 н. раствором гидроксида натрия в присутствии фенолфталеина до появления розовой окраски. Одновременно в тех же условиях проводят контрольный опыт. Молярную долю гидроксил.ьных групп х (%) вычисляют по формуле
где v1— объем 0,5 н. раствора гидроксида натрия, пошедший на титрование в контрольном опыте; v2— объем 0,5 н. раствора гидроксида натрия, пошедший на титрование пробы; К — коэффициент поправки для 0,5 н. раствора гидроксида натрия; 0,0085 — массовое количество гидроксильных групп, соответствующее 1 мл точно 0,5 н. раствора гидроксида натрия; m — масса навески поливинилового спирта. Ацетатные группы в поливиниловом спирте определяют, омы-ляя их спиртовым раствором гидроксида калия (см. 10.4, работу 1), при этом поливинилового спирта следует взять ~2 г.
Работа 3. Определение молярной доли ацетальных групп в поливинилацеталях.Метод основан на гидролизе поливинилацеталя с одновременным оксидированием карбонильной группы солянокислым гидроксиламином. Реакция поливинилацеталя (поливинилформаля, поливинилэтаналя или поливинилбутираля) с солянокислым гидроксиламином в спиртовой среде протекает по схеме
В результате реакции образуются соответствующий оксим, поливиниловый спирт и соляная кислота, которую оттитровывают щелочью. Реактивы и оборудование
Этиловый спирт Бюкс для взятия навески Гидроксиламин солянокислый, 7%- Колба криглодонная на 250 мл иый водный раствор пришлифованным шариковым Гидроксид натрия, 0,5 и. раствор холодильником Метиловый оранжевый, 0,1%-ный Пипетка иа 25 мл раствор Цилиндры мерные на 50 и 100 мл
Ход определения. Навеску ~2 г поливинилацеталя, высушенного до постоянной массы, помещают в круглодонную колбу емкостью 250 мл, приливают 50 мл этилового спирта, присоединяют к колбе обратный холодильник и нагревают на водяной бане до полного растворения ацеталя. Затем добавляют пипеткой 25 мл 7%-ного раствора солянокислого гидроксил-амина и нагревают при сильном кипении 1,5—2 ч. По окончании нагревания через верх холодильника вливают 100 мл дистиллированной воды для растворения осадка поливинилового спирта, перемешивают и нагревают 10—15 мин. Полученный прозрачный раствор после охлаждения титруют 0,5 н. раствором гидроксида натрия в присутствии индикатора метилового оранжевого до желтовато-оранжевой окраски. Одновременно в тех же условиях ставят контрольный опыт. Молярную долю ацетатных групп х, (%) в поливинилацетате формуле
где v1— объем 0,5 н. раствора гидроксида натрия, израсходованный на титрование поливинилацеталя; V2— объем 0,5 н. раствора гидроксида натрия, израсходованный на титрование в контрольном опыте; К—коэффициент поправки для 0,5 н. раствора гидроксида натрия; F—массовое количество ацетальных групп, соответствующее 1 мл точно 0,5 н. раствора гидроксида натрия (в случае определения ацетальных групп Fравно: в поливинилбутирале — 0,044, в поливинилэтилале — 0,030, в поливинилформале — 0,023); m — масса навески поливинилацеталя. В поливинилацеталях молярную долю ацетатных групп определяют но методике, описанной в разд. 10.4, работа 1, гидроксильных групп — фталированием (см. разд. 10.4, работа 2).
ФЕНОЛОАЛЬДЕГИДНЫЕ СМОЛЫ
Фенолоальдегидные смолы представляют собой твердые (ГОСТ 18694—80) или жидкие продукты от светло-желтого до темного цвета. Плотность 1,1—1,27 г/см3. Растворимы во многих органических растворителях: этиловом спирте, ацетоне, пиридине и др. Получают смолы конденсацией различных фенолов с альдегидами в кислой или щелочной среде. В зависимости от соотношения фенола и альдегида и от рН среды образуются смолы двух типов: 1) новолачные, термопластичные и 2) резольные, термореактивные. Новолачные смолы получают конденсацией альдегидов с избытком фенола в присутствии кислых катализаторов. Эти смолы сохраняют плавкость и растворимость при длительном хранении, а также при нагревании до 200—250°С. Они могут превращаться в неплавкие продукты после дополнительной обработки формальдегидом или гексаметилентетрамином. Резольные смолы получают конденсацией фенола с избытком альдегида в присутствии главным образом щелочных катализаторов. Эти смолы при длительном хранении, нагревании или на холоду переходят в неплавкое и нерастворимое состояние. При нагревании фенолоальдегидных смол до температуры 300°С происходит их разложение. Анализ фенолоформальдегидных смол состоит в определении массовой доли свободного фенола, альдегида и определении бромного числа, массовой доли метилольных групп (для резольных смол), вязкости, температуры каплепадения, времени желатинизации. Работа 1. Определение массовых долей свободного фенола и формальдегида.В фенолоформальдегидиых смолах могут содержаться различные количества свободного фенола и формальдегида. Свойства изделий из фенолоформальдегидных смол зависят от содержания свободных компонентов, и поэтому определение их весьма важно. Метод определения основан на отгонке из смолы свободного фенола и формальдегида водяным паром. Фенол определяют в отгоне бромированием по методу Коппершаара. Обработкой бромид-броматным раствором в кислой среде получают трибромфенол. При избытке брома бромирова-ние идет дальше с образованием трибромфенолброма. По окончании бромирования к реакционной смеси приливают раствор иодида калия и избыток брома, и бром, замещающий водород гидроксильной группы, вытесняет эквивалентное количество иода; выделившийся иод титруют 0,1 н. раствором тиосульфата натрия. Реакции протекают по уравнениям, приведенным в разд. 8.4, работа 5. Свободный формальдегид определяют в том же дистилляте, полученном перегонкой смолы с водяным паром. Формальдегид окисляется в щелочной среде реактивом Несслера:
Выделившуюся ртуть после подкисления растворяют в растворе иода и избыток иода оттитровывают тиосульфатом натрия:
Массовая доля эквивалента формальдегида равна 1/2 массы моля, т. е. 15,01 г. Реактивы и оборудование
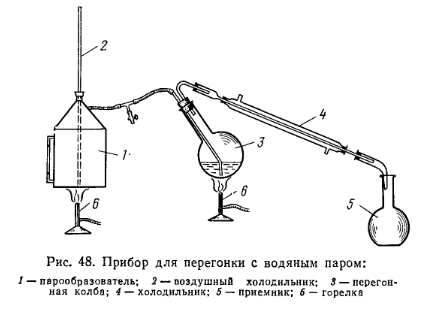
Приготовление реактива Несслера. Растворяют 25 г ртути, 28 г иода и 55 г иодида калия в 100 мл дистиллированной воды. Смесь энергично взбалтывают до обесцвечивания (допускается слабо-желтая окраска), фильтруют в мерную колбу емкостью 500 мл и объем в колбе доводят до метки дистиллированной водой. Раствор должен храниться в склянке оранжевого стекла в темном месте. Приготовление раствора иода. Последовательно растворяют 25 г иодида калия и 12,7 г кристаллического иода в 100 мл дистиллированной воды, после чего объем раствора доводят до 1000 мл. Ход определения. Навеску ~2 г тонко измельченной смолы отвешивают по разности в бюксе или на часовом стекле с точностью до 0,0002 г и помещают в длинногорлую кругло-донную колбу емкостью 1000 мл. Навеску смолы растворяют в 20 мл этилового спирта и прибавляют 200 мл воды. Полученную эмульсию перегоняют с водяным паром (рис. 48) в мерную колбу емкостью 500 мл до прекращения образования мути с бромной водой. Для проведения пробы отставляют мерную колбу и 2 — 3 мл дистиллята собирают в пробирку. Затем в пробирку по стенке прибавляют несколько капель бромной воды. По окончании отгонки раствор в мерной колбе разбавляют дистиллированной водой до метки и тщательно перемешивают. Для определения содержания свободного фенола отбирают пипеткой 25 мл дистиллята и вносят в коническую колбу с притертой пробкой емкостью 250 мл. Прибавляют пипеткой 50 мл 0,1 н. бромид-броматного раствора, 5 мл соляной кислоты (р=1,19), быстро закрывают пробкой, хорошо перемешивают и выдерживают при комнатной температуре 15 — 20 мин. Затем Добавляют 15 мл 10%-ного раствора иодида калия, перемешивают и через 15 — 20 мин титруют выделившийся иод 0,1 н. раствором тиосульфата натрия, прибавляя в конце титрования (к раствору светло-желтого цвета) несколько капель раствора крахмала в качестве индикатора и титруя до обесцвечивания. Параллельно проводят контрольный опыт, в котором вместо 25 мл испытуемого раствора берут 25 мл дистиллированной воды. Массовую долю фенола в смоле ω1 (%) вычисляют по формуле где v1—объем 0,1 н. раствора тиосульфата натрия, израсходованный на титрование в контрольном опыте; V2 — объем 0,1 н. раствора тиосульфата натрия, израсходованный на титрование испытуемого раствора; К—коэффициент поправки для 0,1 н. раствора тиосульфата натрия; т — навеска смолы; 0,001567 — масса фенола, соответствующая 1 см3 точно 0,1 н. раствора тиосульфата натрия.
Для определения содержания свободного формальдегида можно использовать дистиллят, полученный при определении содержания свободного фенола. Отбирают пипеткой 25 мл отгона и вносят в коническую колбу с притертой пробкой емкостью 250 мл. Прибавляют 10 мл реактива Несслера, 25мл 50%-ного раствора гидроксида натрия, закрывают пробкой и взбалтывают в течение 5 мин. После выделения ртути (жидкость принимает темно-серую окраску) содержимое колбы нейтрализуют 30—35 мл соляной кислоты (р=1,19) до слабокислой реакции по лакмусовой бумаге, затем, не давая смеси охладиться, прибавляют пипеткой 20 мл 0,1 н. раствора иода, взбалтывают до полного растворения ртути и избыток иода оттитровывают 0,1 н. раствором тиосульфата натрия, прибавляя в конце титрования раствор крахмала в качестве индикатора и титруя до обесцвечивания. Одновременно проводят контрольный опыт, где вместо испытуемого раствора берут 25 мл дистиллированной воды. Массовую долю свободного формальдегида в смоле ω2 (%) вычисляют по формуле
где v1— объем 0,1 н. раствора тиосульфата натрия, израсходованный на титрование в контрольном опыте; v2— объем 0,1 н. раствора тиосульфата натрия, израсходованный на титрование испытуемого раствора; К—коэффициент поправки для 0,1 н. раствора тиосульфата натрия; т — навеска смолы; 0,0015 — масса формальдегида, соответствующая 1 см3 точно 0,1 н. раствора тиосульфата натрия. Работа 2. Определение бромного числа по методу Петрова. Бромное число — это масса брома, присоединяющаяся к низкомолекулярным водорастворимым продуктам, содержащимся в 100 г смолы. Метод состоит в растворении исследуемой смолы в водном растворе щелочи, осаждении ее раствором кислоты и определении массы брома, присоединяющегося к низкомолекулярным продуктам, находящимся в фильтрате.
Реактивы и оборудование
Гидроксид натрия, 10%-ный раствор Крахмал растворимый, 1%-ный водный раствор Соляная кислота, 7%-ный раствор Соляная кислота, р=1,19 Бюкс для взятия навески Бромид-броматный, 0,1 н. раствор Цилиндры мерные на 10 и 25 мл Иодид калия, 10%-ный раствор Колба коническая на 250 мл с пришлифованной пробкой Тиосульфат натрия, 0,1 и. раствор Пипетка на 25 мл
Ход определения. Навеску смолы 0,2—0,3 г, взятую с точностью до 0,0002 г, обрабатывают 20 мл 10%-ного раствора гидроксида натрия и оставляют стоять при комнатной температуре в течение 24 ч. После этого раствор нейтрализуют 7%-ным раствором соляной кислоты до слабокислой реакции (проба на синюю лакмусовую бумагу). Образующийся осадок отфильтровывают и промывают несколько раз дистиллированной водой. Фильтрат и промывные воды собирают в коническую колбу емкостью 250 мл с притертой пробкой. К полученному раствору прибавляют пипеткой 25 мл 0,1 н. бромид-броматного раствора и 5 мл соляной кислоты. Колбу закрывают пробкой, взбалтывают и оставляют стоять в течение 15 мин, после чего прибавляют 10 мл 10%-ного раствора иодида калия и 50 мл дистиллированной воды. Через 5 мин титруют выделившийся иод 0,1 н. раствором тиосульфата натрия, прибавляя в конце титрования несколько капель раствора крахмала в качестве индикатора и продолжая титровать до обесцвечивания раствора. Одновременно проводят контрольный опыт. Значение бромного числа (б.ч.) в г/100 г вычисляют по формуле
где v1— объем 0,1 н. раствора тиосульфата натрия, пошедший на титрование в контрольном опыте; V2— объем 0,1 н. раствора тиосульфата натрия, пошедший на титрование испытуемого раствора; К — коэффициент поправки для 0,1 н. раствора тиосульфата натрия; 0,00799 — масса брома, соответствующая 1 см3 точно 0,1 н. раствора тиосульфата натрия; m — масса навески смолы. Работа 3. Определение массовой доли метилольных групп в резольной смоле.Метод основан на конденсации фенолоспиртов с большим избытком фенола в присутствии соляной кислоты с образованием производных дифенилметана. Реакция проходит по схеме
Избыток непрореагировавшего фенола отгоняют с водяным паром. При определении метилольных групп с фенолом реагируют не только метилольные группы, но и свободный формальдегид, содержащийся в исходной смоле. Кроме того, с метилольными группами реагирует и свободный фенол, содержащийся в смоле. Поэтому при расчете содержания метилольных групп необходимо учитывать содержание свободного фенола и свободного формальдегида в смоле. Реактивы и оборудование Фенол, 80%-ный раствор Соляная кислота, р=1,19 Соляная кислота, 0,1 н. раствор Этиловый спирт Бромид-броматный 0,1 н. раствор (приготовление см. разд. 8.3, работа 7) Иодид калия, 10%-иый раствор Тиосульфат натрия, 0,1 н. раствор Крахмал растворимый, 1%-ный раствор Бромная вода Бюкс для взятия навески Колба круглодонная на 250 мл с пришлифованным шариковым холодильником Колба круглодонная, длинногорлая на 1000 мл Колба коническая на 250 мл с пришлифованной пробкой Колба мерная на 500 мл Прибор для перегонки с водяным паром Цилиндр мерный на 25 мл Пипетки на 1, 25 и 50 мл
Ход определения. Навеску тонко измельченной смолы - 0,2 г, взвешенную в бюксе с точностью до 0,0002 г, помещают в круглодонную колбу емкостью 250 мл и вносят пипеткой 1 мл 80%-ного раствора фенола. Колбу соединяют с пришлифованным обратным холодильником, ставят ее на кипящую водяную баню и через холодильник вносят 10 мл 0,1 н. раствора соляной кислоты. Нагревают в течение 2 ч, охлаждают, не снимая холодильника. Затем содержимое колбы переносят в колбу для перегонки с водяным паром, обмывают колбу 20 мл этилового спирта и сливают спирт в колбу для перегонки. Избыток фенола отгоняют с водяным паром, собирая дистиллят в мерную колбу емкостью 500 мл. Перегонку с водяным паром ведут до тех пор, пока дистиллят не перестанет образовывать муть с бромной водой. Затем раствор доводят дистиллированной водой до метки, хорошо перемешивают, отбирают 25 мл раствора и определяют содержание фенола способом Коппершаара (см. разд. 10.5, работа 1). Одновременно проводят контрольный опыт, предварительно перегнав смесь из 1 мл 80%-ного фенола, 10 мл 0,1 н. раствора соляной кислоты и 20 мл этилового спирта с водяным паром. Массу фенола т1(г) в контрольном опыте рассчитывают по формуле
и в рабочем опытеm2по формуле
где v1— объем 0,1 н. раствора тиосульфата натрия, израсходованный на титрование в контрольном опыте; V2— объем 0,1 н. раствора тиосульфата натрия, израсходованный на титрование в рабочем опыте; К— коэффициент нормальности для 0,1 н. раствора тиосульфата натрия; 0,001567 — количество фенола, соответствующее 1 мл точно 0,1 н. раствора тиосульфата натрия. Массовую долю метилольных групп ω3 (%) рассчитывают по формуле
где т1— масса фенола в контрольном опыте; т2— масса избыточного фенола, найденного при титровании в рабочем опыте;ω1— массовая доля свободного фенола в исследуемой навеске Смолы; т — навеска смолы; ω2 — массовая доля свободного формальдегида в исследуемой смоле; 0,33 — масса метилольных групп, соответствующая 1 г фенола; 1,003 — соотношение молярных масс метилольной группы и формальдегида. Работа 4. Определение вязкости.В фенолоальдегидных смолах определяют относительную вязкость 50%-ного раствора смолы в ацетоне или этиловом спирте при 20°С. Определение ведут при помощи вискозиметра ВПЖ (см. рис. 14). |
||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 708. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |