Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Окисление окисью серебра (реакция “серебряного зеркала”).Если к прозрачному бесцветному аммиачному раствору окиси серебра* прибавить раствор альдегида и нагреть жидкость, то на стенках пробирки при достаточной чистоте их образуется налѐт металлического серебра в виде зеркала; если же стенки пробирки
Окисление гидроокисью меди Если к жидкости со светло-голубым осадком гидроокиси меди (II) прибавить раствор, содержащий альдегид, и нагреть смесь, то вместо голубого осадка появляется желтый осадок гидроокиси меди (I) CuOH. Альдегид при этом превращается в кислоту:
3. Кислородом воздуха окисляются некоторые наиболее легко окисляющиеся альдегиды, к которым относятся ароматические альдегиды, как, например, бензальдегид:
*Аммиак образует с ионом серебра комплексное соединение, что приводит к
4. Реакция Канниццаро или реакция дисмутации является реакцией окисления – восстановления, при которой из двух молекул альдегида одна окисляется в кислоту, а другая при этом восстанавливается в спирт. Эта реакция, свойственная преимущественно ароматическим альдегидам, была открыта в 1853 г. итальянским ученым Канниццаро, который установил, что в присутствии Бензойная кислота концентрированного раствора щелочи (например, 60%-го раствора КОН) бензальдегид превращается в соль бензойной кислоты и бензиловый спирт:
Из алифатических альдегидов в реакцию Канниццаро вступают формальдегид и альдегиды, содержащие альдегидную группу у четвертичного атома углерода: 
II. РЕАКЦИИ ПРИСОЕДИНЕНИЯ Реакции присоединения к карбонилу альдегидов При протекании этих реакций в большинстве случаев первой стадией является присоединение к положительно заряженному атому углерода карбонила
1. Гидрирование (восстановление) с образованием первичных спиртов RCH2OH:
2. Присоединение спиртов с образованием полуацеталей:
При взаимодействии альдегидов со спиртами образуются полуацетали:
Гидроксильная группа полуацеталей (полуацетальный гидроксил) очень реакционно-способна. В присутствии катализатора – хлороводорода HCl при избытке спирта образуются ацетали RCH(OR´)2:
3. Присоединение синильной кислоты к альдегидам дает оксинитрилы или циангидрины, происходит нуклеофильное присоединение:
4. Присоединение гидросульфита натрия NaHSO3 с образованием гидросульфитных производных альдегидов:
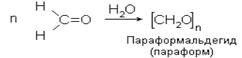
Этой реакцией часто пользуются для выделения альдегидов из смесей или с целью их очистки. III. Реакции полимеризации(характерны для низших альдегидов) Полимеризацией называется процесс соединения одинаковых молекул (мономеров), протекающий за счѐт разрыва кратных связей, с образованием высокомолекулярного соединения (полимера). Линейная полимеризация При испарении или длительном стоянии раствора формальдегида
Полимеризация безводного формальдегида в присутствии катализатора – пентакарбоната железа Fe(CO)5 – приводит к образованию высокомолекулярного соединения с n = 8÷100 – полиформальдегида (полиоксиметилен, полиметиленоксид):
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 380. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |






 отрицательно заряженной частицы (например, аниона ОН¯). Поэтому многие реакции этой группы относятся к реакциям нуклеофильного присоединения.
отрицательно заряженной частицы (например, аниона ОН¯). Поэтому многие реакции этой группы относятся к реакциям нуклеофильного присоединения.