
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
II. Реакции с участием бензольного кольцаРеакции замещения в бензольном кольце протекают легче, чем у бензола, и в более мягких условиях. 1. Галогенирование:
Особенно легко происходит бромирование в водных растворах, при этом сразу образуется 2,4,6-трибромфенол:
2. Нитрование:
3. Сульфирование: Соотношение орто- и пара-изомеров определяется температурой реакции: при комнатной температуре в основном образуется орто-фенолсульфокислота, при t = 100 ºC – пара-изомер.
III. Реакции присоединения Гидрирование:
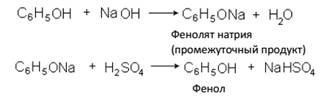
Способы получения 1. Из каменноугольной смолы. Каменноугольную смолу, содержащую в качестве одного из компонентов фенол, обрабатывают вначале раствором щелочи (образуются феноляты), а затем – кислотой:
2. Сплавление солей аренсульфокислот со щелочью:
3. Взаимодействием галогенопроизводных ароматических углеводородов со щелочами:
или с водяным паром:
4. Кумольный способ: В качестве исходного сырья используют бензол и пропилен, из которых получают изопропилбензол (кумол), подвергающийся дальнейшим превращениям:
В результате этих процессов получают два ценных продукта – фенол и ацетон. Применение фенола Схема применения фенола представлена на рис. 2.
ГЛАВА 13. КАРБОНИЛЬНЫЕ СОЕДИНЕНИЯ Органические соединения, в молекуле которых имеется карбонильная группа
а в молекулах кетонов – с двумя углеводородными радикалами:  Углеводородные радикалы могут быть алифатическими (насыщенными или ненасыщенными), алициклическими и ароматическими. Мы рассмотрим только алифатические карбонильные соединения. АЛЬДЕГИДЫ Изомерия. Номенклатура Общая формула предельных альдегидов CnH2nO или CnH2n+1–CHO. Изомерия альдегидов связана только со строением углеродного скелета и с положением карбонильной группы, например:
Альдегиды называют или по кислотам, в которые они переходят при окислении (с тем же числом углеродных атомов) или по предельным углеводородам с добавлением окончания –аль (систематическая номенклатура). Примеры:
Способы получения 1. Окисление первичных спиртов – важнейший способ получения альдегидов:
б) окисление спирта кислородом воздуха в присутствии металлических катализаторов. В качестве катализатора в промышленности используется мелко раздробленная медь. При нагревании медь окисляется кислородом воздуха в окись меди:
Через систему пропускают пары метилового спирта, смешанные с воздухом. Метиловый спирт окисляется окисью меди, а образующаяся металлическая медь вновь окисляется кислородом воздуха. Таким образом, эти реакции повторяются неограниченное число раз.
Реакция окисления метилового спирта окисью меди является экзотермической, поэтому нагревание нужно только в начале реакции. Этот способ лежит в основе технического получения некоторых альдегидов. 2. Из дигалогенопроизводных, имеющих оба галогена у одного и того же первичного атома углерода, альдегиды получаются в результате реакции нуклеофильного замещения галогенов на гидроксилы:
Этот способ используется для получения бензойного альдегида:
Физические свойства Карбонильные соединения не образуют водородных связей, поскольку в их молекулах нет атомов водорода с положительным зарядом. По этой причине температура кипения альдегидов значительно ниже, чем соответствующих спиртов. Низшие альдегиды – легкокипящие жидкости (формальдегид – газ) с резким запахом, хорошо растворимы в воде.
Химические свойства Альдегиды вступают в очень большое число реакций, представляя собой одну из наиболее реакционноспособных групп соединений. Для удобства рассмотрения реакций альдегидов их можно разделить на группы в соответствии с теми атомами и группами атомов, которые присутствуют в молекуле альдегида:
I – атом водорода альдегидной группы, находящийся в непосредственном соседстве с карбонилом и потому обусловливающий легкую способность окисляться; II – карбонильная группа, которая обусловливает большой ряд реакций присоединения к карбонилу и замещения атома кислорода карбонила; III – радикал, который может участвовать в ряде реакций, свойственных остаткам углеводородов. Таким образом, для альдегидов характерны реакции окисления, присоединения, полимеризации и поликонденсации. I. Реакции окисления Альдегиды очень легко окисляются. Особенно характерно для альдегидов то, что такие слабые окислители, как некоторые окиси и гидроокиси тяжелых металлов, которые не действуют на ряд других органических соединений, легко окисляют альдегиды с выделением свободных металлов или их закисей (“альдегидные реакции”). |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 517. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |










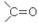 , называют карбонильными соединениями или оксосоединениями. Они делятся на две родственные группы – альдегиды и кетоны. В молекулах альдегидов карбонильная
, называют карбонильными соединениями или оксосоединениями. Они делятся на две родственные группы – альдегиды и кетоны. В молекулах альдегидов карбонильная








