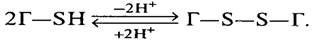Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
ПРЕВРАЩЕНИЯ ВЕЩЕСТВ ПРИ АЭРОБНОМ И АНАЭРОБНОМ МЕТАБОЛИЗМЕ ДРОЖЖЕЙЭнергетический эффект анаэробного использования углеводов дрожжевой клеткой невелик, так как большое количество потенциальной энергии остается в спирте, не подвергающемся ферментативному распаду, поэтому процессы синтеза в дрожжевой клетке при брожении протекают значительно медленнее, чем при дыхании. Для получения необходимой энергии она должна потреблять значительное количество гексозы, что снижает экономичность процесса спиртового брожения. Для своего развития, роста и размножения дрожжевая клетка нуждается в веществах, растворимых в воде, из которых она строит свою живую ткань. Эти вещества клетка разлагает, и из продуктов распада образуются белки протоплазмы, углеводы, жиры, фосфаты и ряд других веществ. Для жизнедеятельности клетке нужна химическая энергия. Все остальные виды энергии (механическая, тепловая, электрическая, световая) для этих целей не могут быть использованы. Химическая энергия может быть востребована только в том случае, если она получена в самой клетке. Следовательно, энергия индуцируется из растворенных в среде веществ, которые могут через оболочку проникать в клетку. Нерастворимые вещества должны быть сначала переведены в растворимое состояние; вещества, неспособные к диффузии, должны быть сначала разложены. Для этого клетки выделяют в среду ферменты, экзоферменты, например гидролазы, внутри клеток остаются эндоферменты, которые из усвоенных веществ выделяют энергию. Первый процесс называется ассимиляцией, второй процесс (синтез) — диссимиляцией. При ассимиляции энергия потребляется, при диссимиляции — выделяется. Ассимиляция и диссимиляция — это два основных процесса обмена веществ или метаболизма. Если при диссимиляции участвует кислород, то этот процесс носит окислительный характер (дыхание), если кислород не участвует — восстановительный (брожение). Окислительно-восстановительные процессы возникают как при дыхании, так и при брожении и состоят в основном в переносе водорода от одного вещества к другому.  Вещества, участвующие при дыхании в окислительно-восстановительных превращениях, называют дыхательными ферментами. Они являются катализаторами окислительно-восстановительных процессов. К ним относится система цитохромов а, b и с. Цитохромы окисляются только из восстановленной формы в присутствии фермента цитохромоксидазы. Все три цитохрома окисляются последовательно: сначала окисляется цитохром с, потом а при одновременном восстановлении цитохрома с и, наконец, цитохром b при одновременном восстановлении цитохрома а. Эти окислительно-восстановительные процессы происходят благодаря наличию атома железа, являющегося частью порфиринного ядра цитохромов. В анаэробных условиях окисление цитохромов тормозится. Дрожжевые клетки обладают полной системой цитохромов. Кроме цитохромов в клетках присутствует желтый фермент, состоящий из бесцветного белка (апофермента) и желтого кофермента, называемого флавоном. Основу флавона составляет рибофлавин (витамин В2) в сочетании с фосфорной кислотой и аденозиннуклеотидом. В соединении с белковым веществом флавон образует целую ферментную систему — флавопротеин. При брожении флавопротеин отнимает водород у восстановленной формы козимазы (кодегидраза I). Козимаза, основу которой составляет амид никотиновой кислоты (ниацин), является катализатором в процессе спиртового брожения при окислении дифосфоглице-ринового альдегида в дифосфоглицериновую кислоту; при этом она восстанавливается в дегидрокодегидразу I. В начале процесса брожения исходную козимазу обновляет флавопротеин, и только позже эту функцию акцептора водорода выполняет ацетальдегид. В дрожжевых клетках также содержится глутатион — трипептид глутаминил-цистеинил-глицин. В биохимическом отношении имеет значение его сульфоводородная группа — SH. В нейтральном или щелочном растворе он легко окисляется:
Следовательно, глутатион выполняет функцию внутриклеточного восстановительного фактора. При окислительно-восстановительных превращениях аскорбиновой кислоты участие глутатиона сводится к следующему:
Такая восстановительная система путем торможения окислительных реакций способствует процессу брожения в клетке. Следовательно, восстановители в клетке подавляют эффект Пастера — в присутствии кислорода брожение ухудшается. Глутатион наряду с липоевой кислотой, коэнзимом А, тиоредоксином относится к числу тиоловых кофакторов. Тиоловые кофакторы являются переносчиками ацильных групп, простетичес-кой группой у которых выступает 4-фосфопантотеин. Роль SH-группы в глутатионе и других тиоловых кофакторах во многих отношениях аналогична роли SH-групп цистеиновых остатков, выполняющих каталитические функции в активных центрах некоторых ферментов. Содержание глутатиона в дрожжах может достигать 1 % на сухую массу дрожжей. В процессе брожения дрожжи Saccharomyces cerevisiae выделяют часть глутатиона в окружающую среду, причем этот процесс зависит как от интенсивности брожения, так и от особенностей расы дрожжей. Выделение дрожжами глутатиона в процессе брожения — это физиологический процесс, связанный с обменом бродящей дрожжевой клетки. Внесение в состав питательной среды сульфата аммония в качестве источника азота усиливает выделение глутатиона в сбраживаемую среду в 1,5 раза и составляет, например, 27,0—33,5 мкг/см3 вместо 15,0—21,7мкг/см3. Следовательно, источник азота, в состав которого входит сера, усиливает синтез глутатиона и выделение его в окружающую среду. Выделяясь в окружающую среду, глутатион, обладая восстановительными свойствами, может отрицательно повлиять на белковый комплекс и реологические свойства теста. Физиологическая роль глутатиона еще не вполне выявлена. Считают, что он защищает SH-группы внутриклеточных ферментов от окисления и блокирования ионами тяжелых металлов. Возможна и такая реакция, в результате которой глутатион в дисульфидной форме реагирует с SH-группами белков и тем самым влияет на регуляцию активности ферментов. Кроме того, полагают, что дисульфид глутатиона участвует в окислительном фосфо-рилировании. Для получения высокой стабильности сушеных дрожжей к прессованным дрожжам перед их высушиванием добавляют антиоксиданты, поверхностно-активные вещества или эмульгаторы — сорбаты, моно- и диэфиры лимонной кислоты, эфиры полиглицерола для защиты клеточных стенок и мембран дрожжевых клеток от повреждений, возникающих при испарении свободной внутриклеточной влаги. При введении таких добавок получают активные сушеные дрожжи влажностью 6—8 %, активность которых остается стабильной в течение года. Глутатион накапливается при сушке в дрожжевых клетках. Перед использованием сушеные дрожжи размачивают. При ре-гидратации сушеных дрожжей в воде температурой 38—40 °С глутатион переходит из дрожжевой клетки в водную фазу, и этот переход продолжается и в процессе спиртового брожения. Выделение глутатиона связано, вероятно, с его участием в переходе аминокислот через наружную мембрану, т. е. с функционированием g-глутаминового цикла. Превращение глутатиона связано с метаболизмом коэнзима А (КоА). По-видимому, образуется смешанный дисульфид глутатиона и КоА, а также фермент, катализирующий реакцию между этим дисульфидом и свободным глутатионом: Г–SH + KoA–S–SГ ↔ ГS–SГ + KoA–SH. Глутатион проявляет специфические коферментные функции. Он является коферментом глиоксилазы, катализирующей превращение метилглиоксаля [СН3—С(ОН)=СО] в молочную кислоту. Сходную функцию глутатион выполняет в качестве кофермента формальдегиддегидрогеназы. Сократить содержание глутатиона в инкубационной среде при применении сушеных дрожжей возможно за счет использования быстродействующих сушеных инстантных дрожжей, не требующих предварительного размачивания (гидратации) и действующих так же эффективно, как прессованные. Сушеные инстантные дрожжи заменяют 3—6 кг прессованных дрожжей. В России инстантные дрожжи выпускают на Сарапульском и Волгоградском дрожжевых заводах под названием «Экспресс». Высокая ферментативная активность этих дрожжей обеспечивается специально подобранными штаммами дрожжей, устойчивых к сушке, с пониженным синтезом глутатиона, с повышенным содержанием сухих веществ (30—33 %) в прессованных дрожжах, направляемых на сушку, и белка (45—55 %). Перед прессованием биомассу дрожжей обрабатывают эмульгаторами, добавляя 1 % к сухим веществам дрожжей. Сушка дрожжей при 38 °С без перегрева в массе дрожжей в течение 30—60 мин обеспечивает сохранность клеточных стенок и мембран дрожжевых клеток. При отделении клеток от питательной среды обмен веществ продолжается до тех пор, пока в межклеточном пространстве находятся растворенные питательные вещества. После использования последних обмен веществ в клетках продолжается за счет клеточных резервов (углеводов, липидов). После того как использованы резервные вещества, начинается автолиз клеток — саморазрушение, в результате которого белки распадаются на аминокислоты и углерод аминокислот расходуется на энергетические нужды. При влажности биомассы свыше 20 % вода полностью заполняет объем клетки и функционирует как непрерывная среда, поэтому в клетке свободно протекают все ферментативные процессы. При высушивании биомассы до влажности 10—12% вода прочно связана с поверхностью макромолекул биополимеров, т. е. это в основном связанная вода. Коллоиды клеток переходят в гели, и протекание ферментативных процессов затрудняется. При уменьшении содержания свободной воды в биомассе снижается интенсивность биохимических и жизненных процессов. В настоящее время неизвестно, можно ли полностью остановить обмен веществ в клетке. При хранении сушеных дрожжей выделяется СО2 и уменьшается количество сухой массы. Так, при хранении сушеных дрожжей влажностью от 10 до 12% в герметических сосудах при 30 °С уже через 2 нед объем СО2 увеличивается почти в 10 раз, т. е. от 2,5 до 30 %, а объем О2 уменьшается от 18 до 19 %. Кроме того, при хранении сушеных дрожжей происходит инактивация клеток. При хранении дрожжевого молока также наблюдаются потери продукта. Находясь в активном состоянии, соответствующем дыхательному типу жизнедеятельности, дрожжевые клетки продолжают «дышать», используя запасные углеводы. В результате уменьшается масса клеток и биомассы. Этот процесс зависит от длительности и температуры хранения и протекает более активно, чем в прессованных или сушеных дрожжах. При хранении дрожжевого молока более 1 сут потери биомассы наблюдаются и при оптимальной температуре. Все вышесказанное свидетельствует о том, что при хранении дрожжей происходят изменение их химического состава, расход клеточных резервов, в связи с чем снижаются показатели качества дрожжей, их бродильная и ферментативная активность в хлебопекарных полуфабрикатах. Поэтому использование в хлебопекарной промышленности дрожжей требует предварительной их обработки с целью восстановления или улучшения исходной активности и активного перехода с дыхательного на бродильный тип метаболизма. Эффект этой операции зависит от состава питательной смеси и скорости адаптации дрожжевых клеток к специально созданным условиям (температуре, рН). Для быстрой адаптации дрожжевых клеток к мучным полуфабрикатам, повышения их физиологической активности и экономичности спиртового брожения целесообразно использование жидких питательных смесей, содержащих углерод, воду, азот, биогенные и олигобиогенные элементы, витаминные и ростовые вещества. Вода составляет наибольшую часть содержимого клетки. Она необходима для обмена веществ, поддержания плазмы в сильно разбавленном состоянии, для ферментативных реакций. К биогенным элементам, необходимым для жизни дрожжевых клеток, относятся калий, натрий, магний, кальций, сера, фосфор и железо. Калий участвует в образовании спор, магний — в построении белков, так же как сера и фосфор.
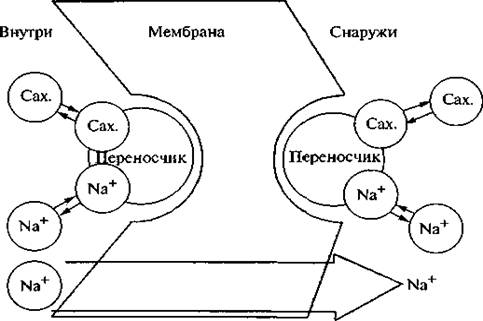
Рис. 2.15. Механизм переноса сахаров через клеточную мембрану в присутствии ионов натрия Магний необходим, кроме того, для активизации фосфатаз, ферментов, участвующих в спиртовом брожении. В питании живой клетки особое значение придается иону натрия. Это единственный компонент, передвижение которого связано с двумя механизмами: из среды в клетку ион натрия поступает пассивно, из клетки в среду — активно, при помощи «натриевого насоса», который «выкачивает» воду из клетки и обеспечивает постоянное осмотическое давление в ней. Одновременно этот насос регулирует концентрацию натрия внутри клетки и поддерживает необходимую разность потенциалов. При пассивном переносе натрия вслед за ним внутрь клетки поступают сахара и аминокислоты даже против градиентов концентраций и потенциала для этих веществ. При активном переносе иона натрия из клетки вслед за ним происходят пассивное перемещение иона хлора по электрохимическому градиенту из клетки в среду и одновременно поступление иона калия в клетку (рис. 2.15). Необходимо отметить, что повышенное осмотическое давление среды является фактором, обусловливающим ее защитные свойства. Росту дрожжевых клеток содействуют олигобиогенные элементы — цинк, медь, молибден, бор, марганец, никель, кремний, алюминий. Минеральные вещества в питательной среде оказывают разное влияние на течение процессов: 1) регулируют осмотическое давление и влияют на проницаемость оболочки; 2) ассимилируются в виде составных частей протоплазматических соединений (питательные соли); 3) оказывают каталитическое действие, так как входят в ферментные соединения или являются переносчиками водорода; 4) их катионы и анионы влияют на плотность электрического заряда на поверхности клеток и этим повышают или понижают агглютинацию клеток (соединение клеток в агрегаты) и изменяют величину поверхности полупроницаемой оболочки. Исключительное место в ряду необходимых элементов занимают углерод и азот. Эти два элемента должны присутствовать в каждой питательной смеси в легкоусвояемой форме. Легче всего углерод усваивается из глюкозы. Некоторые сахара, например лактоза, способствуют росту дрожжевых клеток. Хорошими углеродсодержащими источниками питания являются органические кислоты: уксусная, лимонная, винная; спирты: этанол, глицерин, маннит; жиры, белки и продукты их распада: пептоны и аминокислоты. Неорганические соединения могут быть также ассимилированы в форме карбонатов. При высоких концентрациях источника углерода основной ферментативный процесс может перейти в побочный. Например, при спиртовом брожении в этом случае процесс может не заканчиваться образованием этанола и углерода, а только образованием некоторых промежуточных продуктов. В производстве такое резкое изменение направления процесса очень опасно, так как новая среда может в данных условиях создать предпосылки для развития посторонней микрофлоры. Азот является необходимой составной частью питания и может быть представлен в самых разнообразных формах органических и неорганических соединений. По ассимиляции азотистых соединений различают четыре группы микроорганизмов (табл. 2.2).
Таблица 2.2 |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 652. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |