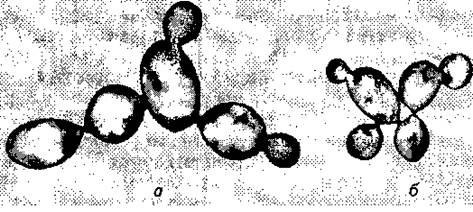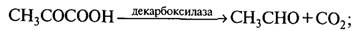Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Дрожжи, обитающие на винограде, в виноградном сусле и вине(по данным И. Хиггинса и др., 1988)
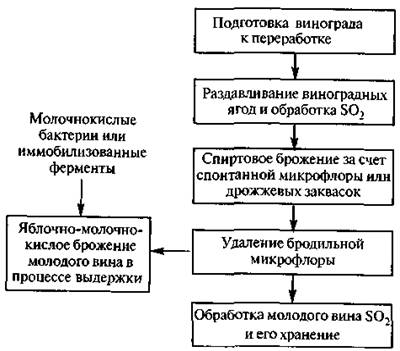
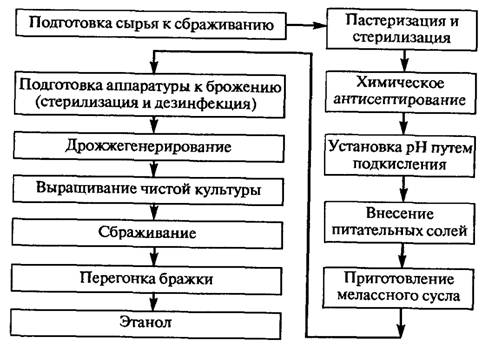
В настоящее время широко применяются дрожжевые закваски. Связано это с тем, что желаемая микрофлора может отсутствовать, а инокуляция стандартной культурой дрожжей позволяет получать вина с заданными свойствами. Использование заквасок дает ряд преимуществ: сокращается лаг-период размножения дрожжей, образуется продукт с желаемыми свойствами, уменьшается вероятность появления нежелательного вкуса. Смешанные закваски позволяют получать продукцию с полным букетом, что невозможно при работе с индивидуальными штаммами. После завершения спиртового брожения вино могут подвергать яблочно-молочнокислому дображиванию, предварительно удалив дрожжи. Этот этап брожения осуществляется молочнокислыми бактериями, в частности Leuconostoc, Lactobacillus и Pedicoccus. Брожение не идет при низких значениях рН, так как при таких условиях его можно подавить. Для инициации брожения вместо бактерий применяют иммобилизованные ферменты.  Некоторые сорта вин получают при использовании микроскопического гриба Botrytis cinerea. Развитие гриба на ягодах приводит к их обезвоживанию и повышению содержания сахара, что определяет сладкий вкус вина. В крепленых винах (портвейн, херес, мадера) часть этанола образуется при сбраживании винограда дрожжами, а часть добавляется. На рис. 1.16 приведена функциональная схема производства красного виноградного вина. Пути модификации существующих технологий для совершенствования вкусовых и ароматических качеств вин, придания им заданных свойств будут определяться выбором более эффективных штаммов винных дрожжей и комплексных дрожжевых заквасок.
Рис. 1.16. Функциональная схема производства красного виноградного вина Спиртовое брожение — один из самых изученных биохимических процессов. Чаще всего его вызывают дрожжи, реже — некоторые бактерии (Sarcina) и микромицеты (Мисог). В промышленности дрожжи обычно разделяют на верховые и низовые. Верховые дрожжи интенсивно ведут брожение и труднее осаждаются. К ним принадлежат спиртовые и хлебопекарные дрожжи Saccharomyces cerevisiae, а также винные дрожжи Saccharomyces elipsoideus (рис. 1.17).
Рис. 1.17. Клетки дрожжей: а — Saccharomyces cerevisiae; б — Saccharomyces elipsoideus
К низовым дрожжам относятся виды, используемые в технологии пива. В основе спиртового брожения лежит разрушение углеводов до этанола и диоксида углерода по следующему суммарному уравнению: С6Н12О6→2СН3СН2ОН + 2СО2 +117 кДж. Начало метаболизма глюкозы идет по схеме гликолиза, в результате образуется пировиноградная кислота. При декарбоксилировании пировиноградной кислоты образуется ацетальдегид в результате гидрогенизации которого образуется этанол по уравнению
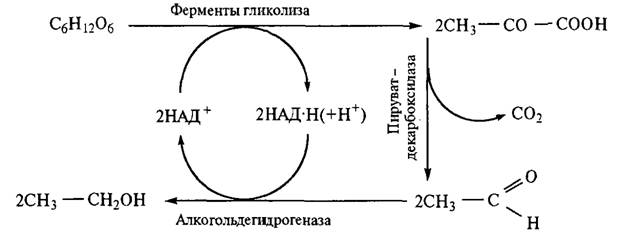
На начальном этапе брожения (период индукции) водород соединяется с глицеральдегидом, восстанавливая его до глицерина. В среде накапливаются глицерин, ацетальдегид и СО2. При образовании в гидролизуемой смеси определенного количества глицеральдегида ход реакции меняется и процесс переходит в стадию стационарного брожения, где акцептором водорода становится ацетальдегид, и образуется этанол (рис. 1.18). Если в питательную смесь добавить сульфиты, связывающие ацетальдегид, то в процессе брожения можно получить значительное количество глицерина, что успешно применяется в промышленности. В этом случае суммарное уравнение брожения примет следующий вид: С6Н12О6 → СН2ОНСНОНСН2ОН + СН3СНО + СО2. В процессе спиртового брожения в смеси могут накапливаться различные высшие спирты — изоамиловый, амиловый и изобутиловый по уравнению R–CH–NH2–COOH + Н2О → R–CH2OH + NH3+CО2. Однако это мнение спорно. Предполагают, что высшие спирты образуются из продукта гликолиза — пировиноградной кислоты путем аминирования ее до аланина, который, в свою очередь, переаминируется в соответствующую кетокислоту. В условиях спиртового брожения кетокислоты, восстанавливаясь, образуют высшие спирты.
Рис. 1.18. Схема образования этанола
В производстве этанола используются штаммы дрожжей Saccharomyces. При выработке рома с сильным запахом применяют штаммы дрожжей Schizosaccharomyces. Процесс образования этанола ускоряется бактериями Clostridium saccharobutyricum. Самый лучший ром получают при соотношении бактерий и дрожжей 1:5. Штаммы дрожжей, используемые в спиртовой промышленности, должны сохранять жизнеспособность до концентрации этанола 12—15 об.%. Они должны обладать способностью гидролизовать низкомолекулярные олигосахариды до глюкозы, что необходимо для полного превращения крахмала в этанол и диоксид углерода. Этанол пищевого назначения получают из крахмалсодержащих пищевых продуктов и сахарсодержащего сырья. При получении этанола из крахмалсодержащего сырья клей-стеризованный крахмал осахаривают при помощи неферментированного солода и ферментных препаратов, содержащих a-амилазу, β-амилазу, глюкоамилазу. Для культивирования микроорганизмов при получении ферментных препаратов, используемых для интенсификации биотехнологических процессов при производстве этанола, используют микроскопические грибы: при поверхностном культивировании — Aspergillus oryzae и Aspergillus awamori, при глубинном — Aspergillus awamori 446 и иногда ВУД-Т2. На спиртовых заводах США применяют высокоактивный штамм Aspergillus awamori NRRL-3112, в России — высокоактивный по глюкоамилазе штамм Aspergillus awamori 466 и ВУД-Т2, выращиваемые на концентрированном кукурузном сусле с содержанием 18 % СВ. Амилолитические ферменты синтезируют также некоторые дрожжи и дрожжеподобные грибы следующих родов: Saccharomyces, Candida, Endomycopsis и Endomyces. В спиртовом производстве нашли применение Endomycopsis bispora и Endomycopsis species 20-9, выращиваемые глубинным способом. Из-за отсутствия других ферментов их используют в комплексе с ферментными препаратами из микроскопических грибов или бактерий. Активные амилазы способны синтезировать следующие бактерии: Bacillus subtilis, Bacillus diastaticus, Bacillus mesentericus, Bacillus macerans и Bacillus polymycus. Бактерии — продуценты амилолитических ферментов — это палочки длиной 1,2—1,3 мкм и диаметром 0,6—0,8 мкм. Они соединяются по две, три, иногда образуют цепочки. Особенностью бактерий является их способность образовывать высокоактивную термостойкую a-амилазу, необходимую для разжижения и декстринизации клейстеризованного крахмала на стадии подваривания замесов и осахаривания сусла. Пока углеводы не переведены в форму, усваиваемую дрожжами, брожения не происходит. Добавление ферментов (амилазы из культуральной жидкости штаммов Bacillus subtilis и амилоглюкозидазы из культур грибов Aspergillus niger), гидролизующих крахмал, ускоряет этот процесс. Ферменты, используемые для осахаривания и при спиртовом брожении, приведены ранее (см. табл. 1.9).a-Амилаза расщепляет амилозу и амилопектин до декстринов, которые, в свою очередь, гидролизуются β-амилазой до мальтозы, а глюкоамилазой до глюкозы. При ферментативном гидролизе в клейстеризованном крахмале остается 20—30 % промежуточных продуктов, которые гидролизуются в ходе брожения, поэтому ферменты сохраняются до конца процесса брожения. Этанол получают также из мелассы, которая является одним из побочных продуктов производства сахара из свеклы. В ней содержится 75—83 % СВ. В том числе (%): сахаров 44—53 (сахарозы до 51%); инвертного сахара 0,1—1,2; раффинозы 0,1—1; кетозы 0,1—0,4; азотистых веществ 14,5—15,0; безазотистых веществ и золы 8,5—12. В свеклосахарной мелассе содержатся витамины: рибофлавин, тиамин, никотиновая и пантотеновая кислоты, пиридоксин, биотин и др. Минеральная часть несахаров мелассы состоит из сульфатов, хлоридов, карбонатов и фосфатов калия, натрия, кальция и железа. При комплексной переработке мелассы в спиртовом производстве кроме этанола получают углекислоту и хлебопекарные дрожжи, а при переработке послеспиртовой мелассной барды (отход спиртового брожения) — кормовые дрожжи, глутаминовую кислоту, бетаин и его производные, витамин В12 и удобрения. В состав раффинозы входит по одной молекуле фруктозы, глюкозы и галактозы. При действии β-фруктофуранозидазы дрожжей раффиноза частично расщепляется с образованием дисахарида мелибиозы и фруктозы. Последняя сбраживается дрожжами, а мелибиоза остается несброженной, поэтому коэффициент сбраживания раффинозы равен 0,34. Кестоза состоит из двух молекул фруктозы и одной молекулы глюкозы, которые сбраживаются полностью. Минеральные соли, определяющие буферность мелассы, в небольших дозах используются дрожжами, но некоторые из них задерживают брожение. Повышенное содержание SО2 в мелассе (0,03 % и больше) тормозит размножение дрожжей и замедляет процесс сбраживания. Такие мелассы обрабатывают хлорной известью в течение 5—6 ч при периодическом перемешивании: SО2 + СаОС12 + Н2О → H2SО4 + СаС12. Эта реакция проходит более интенсивно в кислой среде. Для получения этанола пригодны тростниково-сахарная меласса — продукт, получаемый при переработке тростникового сахара-сырца на белый сахар, рафинадная меласса — при получении сахара-рафинада и тростниковая меласса — при производстве сахара из сахарного тростника. Технология получения этанола из мелассы основана на ферментативном сбраживании сахаров дрожжевыми микроорганизмами и состоит из следующих основных процессов (рис. 1.19).
Рис. 1.19. Технологическая схема производства этанола из мелассы
Для сбраживания мелассного и смешанного мелассно-сахарного сусла в спирт необходимы культуры дрожжей, наиболее приспособленные к сбраживанию сахаров в условиях больших концентраций солей в несахарной группе мелассы и к высокому осмотическому давлению в среде культивирования (табл. 1.11). В технологии спирта применяются следующие культуры дрожжей: дрожжи расы В и ее модификации Вл и В30, раса V-30 гибридные дрожжи Г-67, Г-73, Г-75, Г-105, Г-112 и осмофильныё дрожжи М-5. Для получения наряду со спиртом большого количества дрожжей, используемых в качестве хлебопекарных, с повышенной a-глюкозидазной активностью сусло сбраживают на первой стадии гибридными дрожжами Г-112, а на второй – дрожжами расы В. Таблица 1.11 |
||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 430. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |