Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Прискорений дихроматний методМетодика визначення № 1 з використанням сульфату ртуті для зв'язування хлорид іонів та запобігання окисненню їх дихроматом. У колбу (рис.6.1) кладуть кілька кип'ятильних камінців, вносять 10 см3 проби (або менший об'єм, доведений до 10 см3 бідистильованою водою) і добавляють 5 см3 0,25 моль-екв/дм3 розчину дихромату калію, в якому міститься сульфат ртуті. Потім обережнодобавляють 20 см3 розчину сульфату срібла, у колбу вставляють лійку з термометром, розчин перемішують і ставлять колбу на електроплитку. Коли температура підвищиться до 155 − 160 °С (при цьому суміш закипає), вмикають секундомір. Кипіння має бути слабким і рівномірним. Після 5-хвилинного кипіння температура суміші має становити 165 − 175 °С. Колбу швидко охолоджують до 50 − 60 °С. Якщо розчин набув зеленого забарвлення (недостатня кількість дихромату), то для аналізу беруть менший об'єм проби. Суміш кількісно переносять у колбу для титрування, розбавляють бідистильованою водою приблизно до 100 см3, добавляють 3 − 4 краплі розчину індикатору і з бюретки 10 см3 розчину солі Мора для повного відновлення дихромату, який залишився. При цьому розчин має стати зеленим. Якщо розчин залишився червоним (добавлено недостатню кількість солі Мора), знову доливають з бюретки розчин солі Мора до зміни забарвлення індикатору на зелене і ще 1,0 см3 надлишку. Під час проведення «холостого» досліду з бідистильованою водою добавляють точно таку саму кількість розчину солі Мора. Надлишок солі Мора відтитровують робочим 0,02 моль-екв/дм3 розчином дихромату калію. У точці еквівалентності зелений колір розчину переходить у фіолетовий.  Хімічне споживання кисню (мг О/дм3) обчислюють за рівнянням
де 8 − молярна маса еквівалента кисню; 0,02 − концентрація робочого розчину дихромату калію, моль-екв/дм3; V1 − об'єм робочого розчину дихромату калію, витрачений на титрування проби води, см3; V2 − об'єм робочого розчину дихромату калію, витрачений на титрування «холостої» проби, см3, V − об'єм проби води, см3. Відбирати для аналізу більше ніж 10 см3 проби неприпустимо, оскільки це порушує концентраційний та температурний режими аналізу. Нижня межа визначення становить 10 ± 3 мг О/дм3 за об'єму проби 10 см3.
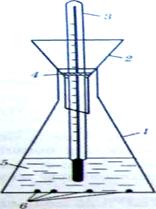
Рис. 6.1. Установка для прискореного визначення ХСК: 1 — термостійка конічна колба місткістю 100 см3 з вузьким горлом (d = 10 мм); 2 — скляна лійка; 3 — термометр скляний лабораторний на інтервал температур 0-200 °С з ціною поділки 1 °С; 4 — обмежувальне кільце з пластику або гуми; 5 —досліджувана проба води; 6 — кип'ятильні камінці
Методика визначення № 2 без використання сульфату ртуті. Аналіз виконують аналогічно методиці визначення № 1, використовуючи 0,25 моль-екв/дм3 розчину дихромату калію, в якому немає сульфату ртуті. Від результату аналізу віднімають по 0,23 мг О/дм3 на 1 мг/л хлорид-іонів, що містяться у пробі. Цю методику можна використовувати для аналізу проб, в яких концентрація хлорид-іонів не перевшцуе 250 мг/дм3. Апаратура Установка для аналізу (див. рис. 6.1). Секундомір. Реактиви Сірчана кислота Н2SO4, х.ч., концентрована. Розчин дихромату калію, 0,25 моль-екв/дм3, який містить сульфат ртуті: 12,258 ± 0,001 г К2Сr2O7, х.ч., і 80 г НgSО4, ч.д.а., розчиняють у 400 − 500 дм3 бідистильованої води, повільно за перемішування добавляють 100 см3 концентрованої сірчаної кислоти, охолоджують і доводять об'єм розчину бідистильованою водою до 1 дм3 у мірній колбі. Розчин дихромату калію, 0,25 моль-екв/дм3, який не містить сульфату ртуті: готують аналогічно попередньому, але без добавляння НgSО4. Робочий розчин дихромату калію, 0,020 моль-екв/дм3: 0,981 ± 0,001 г К2Сr2О7, х.ч., розчиняють у бідистильованій воді й доводять об'єм розчину до 1 дм3 у мірній колбі. Робочий розчин можна також приготувати, розбавивши 80,0 см3 0,25 моль-екв/дм3 розчину К2Сr2О7, який не містить сульфату ртуті, бідистильованою водою до 1 дм3 у мірній колбі. Розчин сульфату срібла: 10 г Аg2SO4, ч.д.а., розчиняють в 1 дм3 концентрованої сірчаної кислоти. Розчин солі Мора, приблизно 0,13 моль-екв/дм3: 51 г Fe(NH4)2(SO4)2∙6H2O, ч.д.а., розчиняють у бідистильованій воді й доводять об'єм розчину до 1 дм3. Розчин індикатору N-фенілантранілової кислоти: 0,1 г сухої N-фенілантранілової кислоти С13Н11O2N розчиняють за нагрівання у 40-50 см3 бідистильованої води, до якої добавлено 0,6 г Nа2СО3∙10Н2O або 0,2 г Nа2СО3, і розбавляють бідистильованою водою до об'єму 100 см3.
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 387. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |