Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
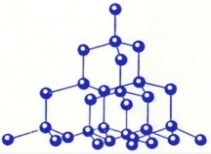
Атомные кристаллические решеткиВ узлах – атомы,связанные прочными ковалентными связями.
Физические свойства веществ с атомной кристаллической решеткой: 1. Твердые. 2. Прочные. 3. Нелетучие. 4. Высокая tпл. 5. Нерастворимы в воде.

Молекулярные кристаллические решетки В узлах молекулярных кристаллических решеток –молекулы.
Физические свойства веществ с молекулярной кристаллической решеткой: 1. Имеют малую твёрдость. 2. Низкие t пл. 3. Летучие. 4. При обычных условиях находятся в газообразном или жидком состоянии.
Металлические кристаллические решетки
В узлах металлических кристаллических решёток находятсяатом-ионыметалла. Физические свойства веществ с металлической кристаллической решеткой: 1. Пластичность. 2. Ковкость. 3. Металлический блеск. 4. Электропроводность. 5. Теплопроводность. Состав атомных ядер. Изотопы. Понятие химического элемента. Атомы, представляют собой сложные образования, построенные из более мелких структурных единиц.
ē - электрон - вне ядра Каждый хим. элемент в периодической системе был пронумерован. Номер, который получает каждый элемент, называется порядковым номером. Физический смысл порядкового номера: 1. Каков порядковый номер элемента, таков и заряд ядра атома. 2. Столько же электронов вращается вокруг ядра . Z = р+ Z - порядковый номер элемента Z = ē n0 = А - Z n0 = А - р+ А - атомная масса элемента n0 = А - ē  Например, Li. Z = 3 р+ = 3 ē = 3 n0= 7- 4 = 3 В результате экспериментальных исследований было установлено, что, например, в природном кислороде кроме атомов кислорода с массой 16 имеются также атомы с массой 17 и 18.
изотопы кислорода Оказалось, что и другие элементы состоят из атомов с различной массой. Так, например, в природной воде кроме атомов водорода с массой 1, имеются также атомы с массой 2, в ядерных реакциях получен также Н с массой 3.
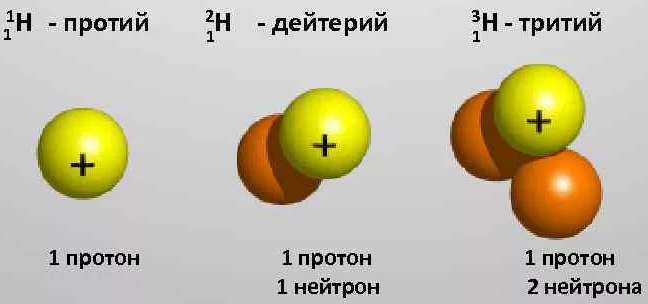
Разновидности атомов одного и того же элемента, имеющие одинаковый заряд ядра (одинаковое число протонов в ядре), но разную массу (разное число нейтронов), называются изотопами. "Изотоп"означает "занимающий одно и то же место". 1Н: р+ = 1 2Н: р+ = 1 3Н: р+ = 1 n0= 0 n0= 1 n0= 2
Среди хим. элементов есть и такие, которые в природе встречаются только в виде одного изотопа (Ве, F, Na, Р и др.) Но их меньшинство.
изобары ("равновесящие") Изобарами называются атомы, имеющие одинаковые массовые числа, но различные порядковые номера, а значит и различные заряды ядер. Химический элемент — это совокупность атомов с одинаковым зарядом атомных ядер.
|
|||||||||||||||
|
Последнее изменение этой страницы: 2018-05-29; просмотров: 480. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |