
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Критерии стабильности стекол
Для оценки стабильности стекла используется ряд критериев, основанных на характеристических температурах Tg (соответствует переходу стекла в состояние переохлажденного расплава), Тх (соответствует началу кристаллизации), Тс (соответствует концу кристаллизации), Тl (температура ликвидуса). В первом приближении мерой термической стабильности стекол является величина Tg/Тх. Чем она выше, тем больше стеклообразующая способность системы и тем медленнее идет процесс расстекловывания при нагреве стекла вблизи Tg. Это так называемое «правило двух третей», согласно которому для большинства стеклообразующих систем в широком интервале температур (100-2000 К) и при скорости охлаждения расплава 10-2<Vохл<10 К/с, выполняется условие Tg/Тх ≈ 2/3. при этом уменьшение приведенной температуры стеклования трактуется как снижение тенденции системы к стеклообразованию. Кроме Tg/Тх для количественной оценки термической стабильности стекол используют величины разница между температурой начала кристаллизации и температурой стеклования: ∆Т = Тх – Tg, приведенная температура: Н´ = ∆Т/Tg, критерий Груби, определяет способность к стеклованию образцов: Нr = ∆Т/(Тl – Тх). Чем выше значение Нr, тем легче получить стекло и тем выше его устойчивость. При Нr ~ 0,1 получение стекла затруднительно и требует специального подбора условий эксперимента, при Нr = 0,5 стекло можно получить, охлаждая расплав на воздухе, при Нr > 1,0 устойчивость стекла высока. Критерий стабильности стекла, вычисляемый по уравнению Саде-Пуле [18], учитывающий как Tg, так и разности между температурами начала кристаллизации и максимума экзотермики:   (1) (1) Величина n является средним значением главного квантового числа валентных электронов, осуществляющих химическую связь, и рассчитывается по формуле:
Величина Z – средний заряд ядра элементов, входящих в состав данного вещества:  , (3)где Zi – значение заряда ядра в формульной единице i -го элемента.Величина К – жесткость электронного каркаса химических связей (ЭКХИС) является функцией электронной структуры свободного атома, определяемой квантовыми числами, и для ковалентных веществ может быть рассчитана, исходя из представлений Р.Л. Мюллера о дискретно-локализованных связях в структурных единицах (СЕ), составляющих данное ковалентное вещество, как отношение числа связей λ в СЕ к числу атомов в ней ν, т.е. , (3)где Zi – значение заряда ядра в формульной единице i -го элемента.Величина К – жесткость электронного каркаса химических связей (ЭКХИС) является функцией электронной структуры свободного атома, определяемой квантовыми числами, и для ковалентных веществ может быть рассчитана, исходя из представлений Р.Л. Мюллера о дискретно-локализованных связях в структурных единицах (СЕ), составляющих данное ковалентное вещество, как отношение числа связей λ в СЕ к числу атомов в ней ν, т.е.  . Однако такой подход справедлив для преимущественно ковалентных веществ, у которых число связей атома равно его координационному числу. При значительной поляризации химических связей, как, например, в оксидах или галогенидах s – элементов, представление о дискретно-локализованных связях и расчет жесткости (ЭКХИС) по соотношению становится некорректным. Различие рассчитанных и реальных величин жесткости каркаса связей в таких веществах обусловлено вкладом ионной составляющей в химическое взаимодействие компонентов. Для учета этого вклада, увеличивающего число эффективных связей центрального атома с окружением, была введена поправка для соединений модификаторов. К ним отнесены вещества, катионообразователи которых имеют электроотрицательность ЭО <1,6. Это позволило использовать представление о валентных возможностях химических элементов, определяемых их электронной структурой, для расчета жесткости ЭКХИС в соответствующих сложных веществах. Так, число неспареных валентных электронов u химического элемента с ЭО <1,6 может быть взято за основу расчета К: . Однако такой подход справедлив для преимущественно ковалентных веществ, у которых число связей атома равно его координационному числу. При значительной поляризации химических связей, как, например, в оксидах или галогенидах s – элементов, представление о дискретно-локализованных связях и расчет жесткости (ЭКХИС) по соотношению становится некорректным. Различие рассчитанных и реальных величин жесткости каркаса связей в таких веществах обусловлено вкладом ионной составляющей в химическое взаимодействие компонентов. Для учета этого вклада, увеличивающего число эффективных связей центрального атома с окружением, была введена поправка для соединений модификаторов. К ним отнесены вещества, катионообразователи которых имеют электроотрицательность ЭО <1,6. Это позволило использовать представление о валентных возможностях химических элементов, определяемых их электронной структурой, для расчета жесткости ЭКХИС в соответствующих сложных веществах. Так, число неспареных валентных электронов u химического элемента с ЭО <1,6 может быть взято за основу расчета К:  Первое слагаемое является суммой произведений числа неспареных электронов i–х свободных атомов или степеней окисления i–х катионообразователей в сложном веществе, удовлетворяющих критерию ЭО< 1,6, на их мольную долю Nik . Этот член учитывает ионный вклад катионообразователей. Второе – сумма (x/y)i – отношение индексов i–х катионообразователей и анионообразователей на мольную долю i–х анионообразователей. Учитывает вклад ковалентной составляющей связи металл – неметалл (Me - F). Третье – сумма (x/y)i мольных долей i–х доноров Nid, т.е. учитывает вклады донорно-акцепторного взаимодействия металл – неметалл (Ме←F). Четвертое – эффективное число химических связей в веществе, влияющее на жесткость структуры, может быть рассчитана только с учетом всех факторов, влияющих на природу химического взаимодействия атомов, в том числе металлизация связи, которая учтена добавочным членом:
где Nik, Nia –мольные доли i–х катионо- и анионообразователей элементов, входящих в вещество; Мi –средняя мольная масса. Множитель Mi/2Zi–1 монотонно возрастает по мере увеличения порядкового номера элементов Zi, отражая тем самым усиление металлизации химических связей. Условием стеклообразования ковалентного расплава является следующее соотношение: 1) 0,09 £ GТ £ 0,36. Кроме этого, для классических стеклообразователей по Захариасену, расплавы, которые стеклуются при их самопроизвольном охлаждении (скорость охлаждения < 100 град/с). Кроме величины GТ необходимо учитывать величину стеклообразующей способности, рассчитанную из полуэмпирического уравнения, которое справедливо для классических стеклообразователей:
где А, В –эмпирические константы: А = 30,84; В = 9,04 Вторым условием образования стекла условными стеклообразователями в сочетании с модификаторами сетки является соотношение:
Если же величина относительного отклонения Диаграммы плавкости систем NaF – MeF2, NaF – CdSO4, MeF2 – CdSO4 (Me – Ca, Ba) В литературе представлена диаграмма плавкости системы NaF –CaF2 (рис. 1.1) [24]. Система эвтектического типа с ограниченными областями твердых растворов на основе исходных компонентов. Образование твердых растворов установлено при помощи термодинамических расчетов. Получено достаточное соответствие между теоретическими и экспериментальными данными. Состав эвтектики определен методом визуально-политермического анализа и приходится на 68 мол. % CaF2. Температура плавления эвтектики составляет 8180С. Рис.1.1. Диаграмма плавкости системы NaF – CaF2 [24]. Данных по другим системам в литературе не обнаружено. |
||
|
Последнее изменение этой страницы: 2018-05-29; просмотров: 381. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 , (2)
, (2)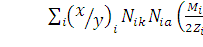
 (5)
(5) (6)
(6) лежит в пределах от 10 до 12 %, то расплав способен стекловаться, но только при быстрых скоростях охлаждения (q > 100 град/с) [2, 22, 23].
лежит в пределах от 10 до 12 %, то расплав способен стекловаться, но только при быстрых скоростях охлаждения (q > 100 град/с) [2, 22, 23].