Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Химические свойства ароматических соединенийБензольное ядро обладает высокой прочностью, чем и объясняется склонность ароматических углеводородов к реакциям замещения. В отличие от алканов, которые также склонны к реакциям замещения, ароматические углеводороды характеризуются большой подвижностью атомов водорода в ядре, поэтому реакции галогенирования, нитрования, сульфирования и др. протекают в значительно более мягких условиях, чем у алканов. 5.1. Электрофильное замещение в бензоле Несмотря на то, что бензол по составу является ненасыщенным соединением, для него нехарактерны реакции присоединения. Типичными реакциями ароматических соединений являются реакции замещения атомов водорода – реакции электрофильного замещения. Рассмотрим примеры наиболее характерных реакций этого типа. 5.1.1. Галогенирование. При взаимодействии бензола с галогеном (в данном случае с хлором) атом водорода ядра замещается галогеном.
(хлорбензол) Реакции галогенирования осуществляются в присутствии катализатора, в качестве которого чаще всего используют хлориды алюминия или железа. Рассмотрим механизм реакции электрофильного замещения в ряду бензола на примере реакции хлорирования. Первичной стадией является генерирование электрофильной частицы. Она образуется в результате гетеролитического расщепления ковалентной связи в молекуле галогена под действием катализатора и представляет собой хлорид-катион. Cl:Cl + AlCl3 à Cl+ + AlCl4- Образующаяся электрофильная частица атакует бензольное ядро, приводя к быстрому образованию нестойкого π- комплекса, в котором электрофильная частица притягивается к электронному облаку бензольного кольца.  π-комплекс Иными словами, π-комплекс – это простое электростатическое взаимодействие электрофила и π-электронного облака ароматического ядра. Далее происходит переход π-комплекса в σ-комплекс, образование которого является наиболее важной стадией реакции. Электрофильная частица "захватывает" два электрона p-электронного секстета и образует σ-связь с одним из атомов углерода бензольного кольца. σ-комплекс σ- Комплекс – это катион, лишенный ароматической структуры, с четырьмя p-электронами, делокализованными (иначе говоря, распределенными) в сфере воздействия ядер пяти углеродных атомов. Шестой атом углерода меняет гибридное состояние своей электронной оболочки от sp2 до sp3, выходит из плоскости кольца и приобретает тетраэдрическую симметрию. Оба заместителя – атомы водорода и хлора располагаются в плоскости, перпендикулярной к плоскости кольца. На заключительной стадии реакции происходит отщепление протона от σ- комплекса и ароматическая система восстанавливается, поскольку недостающая до ароматического секстета пара электронов возвращается в бензольное ядро. Отщепляющийся протон связывается с анионом четыреххлористого алюминия с образованием хлористого водорода и регенерацией хлорида алюминия. H+ + AlCl4- à HCl + AlCl3 Именно благодаря такой регенерации хлорида алюминия для начала реакции необходимо очень небольшое (каталитическое) его количество. 5.1.2. Нитрование. При действии на бензол нитрующей смеси атом водорода замещается нитрогруппой (нитрующая смесь – это смесь концентрированных азотной и серной кислот в соотношении 1:2 соответственно).
(нитробензол) Серная кислота в данной реакции играет роль катализатора и водоотнимающего средства. 5.1.3. Сульфирование. Реакция сульфирования осуществляется концентрированной серной кислотой или олеумом (олеум – это раствор серного ангидрида в безводной серной кислоте). В процессе реакции водородный атом замещается сульфогруппой, приводя к моносульфокислоте.
(бензолсульфокислота) 5.1.4. Алкилирование (реакция Фриделя-Крафтса). При действии на бензол алкилгалогенидов в присутствии катализатора (хлористого алюминия) осуществляется замещение R-углеводородным радикалом атома водорода бензольного ядра.
(R-углеводородный радикал) Следует отметить, что реакция алкилирования представляет собой общий способ получения гомологов бензола - алкилбензолов. Реакции присоединения. Несмотря на склонность бензола к реакциям замещения, он в жестких условиях вступает и в реакции присоединения. 5.2.1. Гидрирование. Присоединение водорода осуществляется только в присутствии катализаторов и при повышенной температуре. Бензол гидрируется с образованием циклогексана, а производные бензола дают производные циклогексана. Катализаторы никель, платина или палладий.
(циклогексан) Присоединение галогенов. На солнечном свету под воздействием ультрафиолетового излучения бензол присоединяет хлор и бром с образованием гексагалогенидов, которые при нагревании теряют три молекулы галогеноводорода и приводят к тригалогенбензолам.
гексахлорциклогексан сим-трихлорбензол 5.3. Окисление. Бензольное ядро более устойчиво к окислению, чем алканы. Даже перманганат калия, азотная кислота, пероксид водорода в обычных условиях на бензол не действуют. При действии же окислителей на гомологи бензола ближайший к ядру атом углерода боковой цепи окисляется до карбоксильной группы и дает ароматическую кислоту.
(калиевая соль бензойной кислоты)
Во всех случаях, независимо от длины боковой цепи образуется бензойная кислота. При наличии в бензольном кольце нескольких заместителей можно окислить последовательно все имеющиеся цепи.
(терефталевая кислота) |
||
|
Последнее изменение этой страницы: 2018-05-27; просмотров: 337. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 + Cl2 à
+ Cl2 à 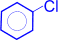 + H2O
+ H2O + Cl+ à
+ Cl+ à  Cl+
Cl+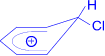
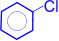 + H+
+ H+ + H2O
+ H2O + H2O
+ H2O + HCl
+ HCl
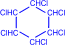 à
à 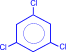 + 3HCl
+ 3HCl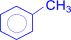 + 2KMnO4 à
+ 2KMnO4 à 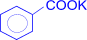 + 2MnO2 + KOH + H2O
+ 2MnO2 + KOH + H2O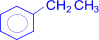 + 4KMnO4 à
+ 4KMnO4 à 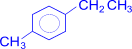 + [ O ] à
+ [ O ] à