Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Общий анализ термодинамических процессов в идеальном газеЦелью расчета и исследования любого термодинамического процесса является определение термических параметров рабочего тела в начале и конце процесса, а также полученной (затраченной) работы и теплоты, подведенной (отведенной) в исследуемом процессе. Для этого необходимо знать: — уравнение состояние рабочего тела (молекулярную массу идеального газа); — уравнение внутренней энергии (количество атомов в молекуле газа); — уравнение процесса в одной из систем координат (p,v; p,T или T,v); — состояние рабочего тела в начале процесса (два независимых параметра, либо величины, из которых их можно определить); — значение одного из изменяющихся параметров в конце процесса (либо величину, из которой его можно рассчитать). Выбор тех или иных исходных данных обусловлен характером процесса либо решаемой задачи. Например, могут быть заданы параметры рабочего тела в одном из его состояний и значения теплоты либо работы процесса, а требуется определить параметры в другом состоянии. Ниже приводятся примеры расчета и анализа термодинамических процессов, используемых в технике. Поскольку чаще всего используется совокупность термодинамических процессов, задачи составлены так, чтобы учащийся с самого начала осваивал методику построения и расчета такой совокупности. Для облегчения восприятия приводимых ниже расчетов и анализа термодинамических процессов в идеальном газе в табл.1 приведены соотношения Таблица 1. Аналитические соотношения между термическими параметрами состояния идеального газа в термодинамических процессах
Таблица 2. Соотношения для расчета теплоты и работы процессов 
между изменяющимися в них термическими параметрами состояния, а в табл. 2 — формулы для расчета теплоты и работы процессов. На рис. 1.1. изображена совокупность политропных процессов расширения, исходящих из одной точки. Соотношения между внутренней энергией, теплотой и работой политропных процессов расширения, протекающих в трёх зонах, отмеченных на рисунке, представлены в табл. 3. Рис. 1.1. Совокупность политропных процессов расширения в координатах p,v и T,s. Таблица 3. Соотношения между внутренней энергией, теплотой и работой в политропных процессах расширения |
||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 377. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |

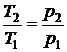 прямо пропорционально
прямо пропорционально

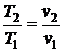 прямо пропорционально
прямо пропорционально

 обратно пропорционально
обратно пропорционально
 , где k – показатель адиабаты, зависящий от количества атомов в молекуле газа
, где k – показатель адиабаты, зависящий от количества атомов в молекуле газа
 с ростом Т растет р, и уменьшается v.
с ростом Т растет р, и уменьшается v.
 , где n – показатель политропы
(может принимать значение от -∞ до +∞)
, где n – показатель политропы
(может принимать значение от -∞ до +∞)
 с ростом Т растет р, и уменьшается v.
с ростом Т растет р, и уменьшается v.