Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Общий анализ термодинамических процессов в реальном газеЦель исследования термодинамических процессов в реальном газе и необходимые исходные данные такие же, как и для идеального газа (см. § 1.1.). При этом следует иметь в виду, что для воды и водяного пара и для многих хладагентов имеющиеся таблицы свойств и диаграммы состояния заменяют уравнения состояния и уравнения для внутренней энергии, то есть позволяют получать данные, необходимые для расчета термодинамических процессов. При расчете и исследовании процессов в реальном газе применяют табличный, графический (с помощью диаграмм) либо аналитический (с помощью уравнений состояния) методы определения свойств в зависимости от процесса и требуемой точности расчета. Все термодинамические процессы можно рассчитать с помощью таблиц, но при этом приходится много интерполировать. Поэтому иногда сочетают два метода: часть свойств определяют по таблицам, а часть — по диаграммам. В последнее время применяют аналитический метод расчёта термодинамических свойств рабочих тел непосредственно по их уравнениям состояния на ЭВМ с использованием термодинамических соотношений. Такой метод особенно эффективен при оптимизационных расчетах циклов паротурбинных и холодильных установок, когда приходится многократно определять свойства рабочих тел. Важной особенностью процессов в реальном газе является возможность их протекания, как в однофазной так и в двухфазной области (влажный пар) либо последовательно в двух областях. В связи с этим необходимо определять с помощью таблиц либо диаграмм, к какой области относятся начальное и конечное состояния рабочего тела, совершающего термодинамический процесс. Это обстоятельство определяет использование таблиц для однофазной области либо для состояния насыщения и, при необходимости, известных аддитивных формул для расчета свойств влажного пара.  При расчетах термодинамических процессов в реальном газе встречаются следующие случаи: — начальное и конечное состояния находятся в однофазной области (пар либо жидкость), причем процесс может проходить через двухфазную область — начинается в жидкости и оканчивается в паре (либо наоборот). В этом случае задача решается с помощью таблиц термодинамических свойств жидкости и перегретого пара; — начальное и конечное состояния находятся в двухфазной области. Тогда используют таблицы свойств насыщенных жидкости и пара и аддитивные формулы для расчета свойств влажного пара; — процесс начинается в однофазной области (жидкости либо паре), а заканчивается в двухфазной области (либо наоборот). В таком случае термодинамические свойства в однофазной области определяют по таблицам для жидкости и перегретого пара, а в двухфазной области рассчитывают по аддитивным формулам, используя таблицы для состояния насыщения. В большинстве перечисленных случаев можно определять свойства и рассчитывать процессы с помощью диаграмм состояния, но на диаграмме h,s для водяного пара отсутствуют пограничная кривая жидкости и область жидкости. Ниже приводятся примеры расчета и анализа процессов, протекающих в воде и водяном паре при постоянных значениях термических параметров (изохорного, изобарного и изотермического), а затем более сложных процессов, совершающиеся при постоянных значениях калорических свойств (изоэнтропного и процесса дросселирования). В конце раздела подробно рассмотрен процесс течения пара — основной рабочий процесс паротурбинных установок.
Изохорный процесс
Рис. 3.1. Изображение изохорных процессов на энтропийных диаграммах На рис. 3.1 изображены в координатах T,s и h,s две изохоры: v1 = idem и v2 = idem (v2>v1). На изохорах указаны восемь точек. Точки 1, 2, 5 и 6 соответствуют состоянию перегретого пара, точки 3, 4 – состоянию обычной жидкости, наконец, точки 7, 8 – влажному пару. В соответствии с указанным расположением точек могут быть идентифицированы следующие варианты изохорного процесса: - 1-2 и 5-6 – процессы, протекающие в области перегретого пара; - 3-4 – процесс, протекающий в области жидкости; - 4-7 – процесс с фазовым переходом жидкость – влажный пар; - 7-8 – процесс в области влажного пара; - 8-5 – процесс с фазовым переходом влажный пар – перегретый пар. Рассмотрим примеры решения задач, в которых рабочее тело совершает изохорный процесс. Задача 1.Определить фазовое состояние и термодинамические свойства воды либо водяного пара, если температура вещества 200°С, а удельный объём 0,12 м3/кг. Задачу решить с помощью диаграммы h,s, а затем уточнить по таблицам свойств воды и водяного пара (табл. 1 приложения). Решение задачи с помощью диаграммы h,s.
Рис. 3.2. Определение состояния пара по заданным значениям температуры и удельного объема с помощью диаграммы h,s. Находим точку пересечения изотермы 200°С (на цветной диаграмме h,s обычно красная линия) с пограничной кривой х = 1 (рис. 3.2) и определяем давление насыщения ps= р8= 1,55 МПа. Далее в пересечении изобары р8 (чёрная линия) с изохорой v = 0,12 м3/кг (зелёная линия) находим искомую точку 8. Она находится слева от пограничной кривой х = 1 и соответствует состоянию влажного пара, которое характеризируется в данном случае: степенью сухости х8 = 0,94, энтальпией h8 = 2680 кДж/кг, энтропией s8 = 6,2 кДж/(кг·К) (определение значений h8 и s8 показано стрелками, исходящими из точки 8). Решение задачи с помощью таблицы свойств воды и водяного пара в состоянии насыщения (табл. 1 приложения) Из табл.1 видно, что при t1 = 200°С удельный объём насыщенной жидкости v' = 0,00116 м3/кг, а удельный объём насыщенного пара v''= 0,12714 м3/кг, то есть v’< v8< v’’, что соответствует состоянию влажного пара. Тогда степень сухости влажного пара х8 рассчитывается из тождества:
Из первого равенства этого тождества рассчитываем степень сухости
Зная величину х8, вычисляем из указанного тождества значения энтальпии h8 и энтропии s8:
Сопоставляя значения параметров х, h и s, определённые по диаграмме и по таблицам, можно сделать вывод, что они хорошо согласуются между собой. Задача 2. Определить количество теплоты, которое необходимо подвести к 1 кгвлажного пара, находящегося в состоянии 8 (см. предыдущую задачу), чтобы его изохорно перевести в состояние перегретого пара, с температурой t5 = 300°С (точка 5). Задачу решить с помощью диаграммы h,s, а затем уточнить по таблицам свойств воды и водяного пара (табл. 1). Решение задачи с помощью диаграммы h,s
Рис. 3.3. Определение состояния перегретого пара с помощью диаграммы h,s при заданных значениях t и v На пересечении изохоры v8 = 0,12 м3/кг (зелёная линия) с изотермой t5 = 300°С (красная линия) находим точку 5, в которой давление равно 2,1 МПа. Определяем калорические свойства перегретого пара в этой точке(показано стрелками): энтальпия h5 = 3020 кДж/кг; энтропия s5 = 6, 75 кДж/(кг·К). Теплота в изохорном процессе расходуется только на изменение внутренней энергии и рассчитывается из соотношения:
Тогда
Решение задачи с помощью таблиц термодинамических свойств воды и водяного пара. Поскольку на диаграмме h,s изохора круче изобары, искомая точка 5 на изотерме 300°Св области перегретого пара находится при более высоком давлении, чем давление в точке 8 р8 = 15,5 бар. Поэтому в таблицах свойств воды и водяного пара при р > р8 ищем две смежные изобары, на которых удельные объёмы при t = 300°С образуют интервал для заданного удельного объёма v5 = =v8 = 0,12 м3/кг. Такими являются изобары 20 бар и 21 бар, термодинамические свойства на которых при t=300°C равны: pб = 20 бар pм = 21 бар vб= 0,1255 м3/кг vм= 0,1192 м3/кг hб= 3024 кДж/кг hм= 3021,1 кДж/кг sб = 6,7679 кДж/(кг·К) sм= 6,7416 кДж/(кг·К) Интерполируем по v (определяем коэффициент интерполяции kv)
Используя найденное значение kv, рассчитываем свойства в точке 5: - давление
- энтальпию - энтропию Тогда – внутренняя энергия перегретого пара в точке 5
– внутренняя энергия влажного пара в точке 8
Теплота, подводимая в изохорном процессе 8-5
Таким образом, результаты определения параметров в точке 5 и расчета теплоты, подводимой в процессе 8-5,по диаграмме и таблицам согласуются вполне удовлетворительно, учитывая точность определения h по диаграмме (1мм = 4 кДж/кг). Изобарный процесс На рис. 3.4. изображены в координатах T,s и h,s две изобары: одна (р1 = =idem) – докритическая, а вторая (р2 = idem) – сверхкритическая, то есть р2>р1. На изобарах отмечены восемь точек, из них точки 1, 2, 5 и 6 находятся в состоянии перегретого пара, 3 и 4 — в состоянии жидкости), 7 и 8 — в двухфазной области (влажный пар).
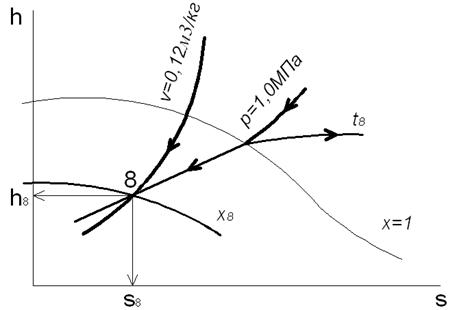
Рис. 3.4. Изображение изобарных процессов на энтропийных диаграммах Используя принятые обозначения точек, выделим возможные варианты изобарного процесса: - 1-2 и 5-6 – процессы, протекающие в области перегретого пара; - 3-4 – процесс в области жидкости; - 4-7 – процесс с фазовым переходом жидкость – влажный пар; - 7-8 – процесс в области влажного пара; - 8-5 – процесс с фазовым переходом влажный пар – перегретый пар. Рассмотрим примеры решения задач. Задача 1.Определить фазовое состояние и термодинамические свойства водяного пара, если его давление 10 бар, а удельный объём 0,12 м3/кг. Задачу решить с помощью диаграммы h,s, а затем уточнить по таблицам свойств воды и водяного пара (табл. 2 приложения). Решение задачи с помощью диаграммы h,s. Находим точку пересечения изобары р = 1,0 МПа на диаграмме h,s (черная линия) с изохорой v = 0,12 м3/кг (зелёная линия). Это и есть искомая точка, которую обозначим цифрой 8 (рис. 3.5). Поскольку данная точка находится левее и ниже пограничной кривой пара (х = 1), она соответствует состоянию
Рис. 3.5. Определение состояния пара с помощью диаграммы h,s по заданным значениям давления и удельного объема. влажного пара со степенью сухости х8 = 0,6, которое характеризируется следующими калорическими свойствами: энтальпия h8 = 2000 кДж/кг; энтропия s8 = 4,87 кДж/(кг·К). Определение значений h8 и s8 показано стрелками, исходящими из точки 8. Температура в точке 8 определяется по точке пересечения изобары р = 1,0 МПа с пограничной кривой х = 1; в рассматриваемом случае t8 = 180 °C Решение задачи с помощью таблицы свойств воды и водяного пара в состоянии насыщения (табл. 2) Из табл.2 видно, что при р = 10 бар удельный объём насыщенной жидкости v'= 0,0011274 м3/кг, а удельный объём насыщенного пара v''= 0,19430 м3/кг, то есть v'< v8< v'', что соответствует влажному пару. Тогда
Из первого равенства этого тождества рассчитываем степень сухости
Затем, используя соответствующие равенство этого тождества, рассчитываем калорические свойства:
Значение температуры в точке 8 определяется по табл. 2 – t8 = ts = 179,88°С. Результаты обоих вариантов расчета согласуются в пределах точности определения свойств по диаграмме h, s. Задача 2. Определить количество теплоты, которое необходимо подвести к 1 кгпара, находящегося в состоянии 8 (см. предыдущую задачу), чтобы его изобарно перевести в состояние перегретого пара, имеющего температуру 300°С (точка 5). Задачу решить с помощью диаграммы h,s, а затем уточнить по таблицам свойств воды и водяного пара (табл. 1 приложения). Решение задачи с помощью диаграммы h,s
Рис. 3.6. Определение состояния пара по заданным значениям давления и температуры с помощью диаграммы h,s Находим точку 5 на пересечения изобары р = 1,0 МПа (черная линия) и изотермы t = 300°С (красная линия). Точка 5 находится в состоянии перегретого пара (выше и правее пограничной кривой х = 1). Определяем калорические свойства пара в точке 5:энтальпию h5= 3050 кДж/кг;энтропию s5= =7,1 кДж/(кг·К) — показано стрелками. Значение удельного объёма v5 = =0,26 м3/кг определяем, интерполируя визуально между изохорами, охватывающими точку 5 Теплота в изобарном процессе 8-5 рассчитывается из соотношения
Решение задачи с помощью таблиц термодинамических свойств воды и водяного пара. Поскольку параметры точки 5 (р5=10 бар и t5=300°С) совпадают с табличными (см. табл. III, [3], стр.98), выписываем термодинамические свойства перегретого пара в соответствующей точке: удельный объём v5= 0,2580 м3/кг;энтальпия h5=3051,3 кДж/кг;энтропия s5=7,2391 кДж/(кг·К). Тогда теплота, подводимая в изобарном процессе 8-5, равна:
Как и в предыдущих случаях, результаты двух вариантов расчета хорошо согласуются между собой. Изотермический процесс На рис. 3.7 изображены в координатах T,s и h,s две изотермы: одна (Т1=idem) – сверхкритическая, а вторая (Т2=idem) – докритическая, то есть Т1>Т2. На этих изотермах отмечены восемь точек, из которых точки 1, 2, 5, 6, 3 и 4 находятся в однофазной области: первые четыре точки соответствуют состоянию перегретого пара, точка 3 —состоянию обычной жидкости, а точка 4 — насыщенной (кипящей) жидкости. Точки 7, 8 находятся в двухфазной области (в области влажного пара).
Рис. 3.7. Изображение изотермических процессов на энтропийных диаграммах На рис.3.7 выделим возможные варианты изотермического процесса: 1-2 и 5-6 – процессы, протекающие в области перегретого пара; 3-4 – процесс, совершающийся в области жидкости; 4-7 – процесс с фазовым переходом жидкость – влажный пар; 7-8 – изобарно-изотермический процесс в области влажного пара (остаются постоянными давление и температура); 8-5 – процесс с фазовым переходом влажный пар – перегретый пар. Рассмотрим решение задачи, в которой рабочее тело (водяной пар) совершает изотермический процесс. Задача. Определить конечное состояние и параметры пара, имеющего температуру 200°С и удельный объем 0,12 м3/кг (точка 8 на рис. 3.2 и 3.7), если к нему изотермически подводится 320 кДж/кг теплоты. Определить также удельную деформационную и техническую работы. Задачу решить с помощью диаграммы h,s , а затем уточнить по таблицам свойств воды и водяного пара (табл. 1 приложения). Решение задачи с помощью диаграммы h,s Количество теплоты, подводимой к 1 кг рабочего тела в изотермическом процессе, рассчитывается из соотношения
где значение s8 =6,2 кДж/(кг·К) принято по данным задачи 1 для изохорного процесса (стр.34). На пересечении изотермы 200°Сс изоэнтропой s5=6,876 кДж/(кг·К) находится искомая точка 5 – конечная точка заданного изотермического процесса подвода теплоты (рис. 3.7). Поскольку точка 5 находится выше и правее пограничной кривой пара х = =1 она соответствует перегретому пару. Искомые термодинамические свойства перегретого пара в этой точке: давление р5 = 0,7 МПа; удельный объём v5 = =0,29 м3/кг; энтальпия h5 = 2844 кДж/кг Деформационная работа изотермического процесса рассчитывается на основании первого закона термодинамики по формуле: где
Здесь значение h8 =2680 кДж/кг принято по данным задачи (стр.34). Техническая работа изотермического процесса рассчитывается также из 1-го закона термодинамики по формуле: Решение задачи с помощью таблиц термодинамических свойств воды и водяного пара. Рассчитываем значение энтропии в точке 5, как и ранее, из выражения для расчета теплоты в изотермическом процессе
Изотермический подвод теплоты сопровождается ростом энтропии, увеличением удельного объёма и уменьшением давления. Поэтому, выбрав изотерму 200°С в области перегретого пара, ищем две смежные изобары, на которых значения энтропии больше и меньше рассчитанного значения s5= =6,8728 кДж/кг. Такими изобарами являются: pб=7,0 бар; sб=6,8873 кДж/(кг·К); hб=2844,8 кДж/кг; vб=0,2999 м3/кг, pм=7,5 бар; sм=6,8508 кДж/(кг·К); hм=2842,0 кДж/кг; vм=0,2791 м3/кг. Заметим, что индексы «б» и «м» относят величины к большему и меньшему значению заданного параметра (в данном случае энтропии) независимо от соотношения определяемых величин в этом интервале. Тогда интерполируем по энтропии между выбранными изобарами
Отсюда
После определения значений h5,v5 и p5 рассчитываем энергетические эффекты, приняв свойства пара в точке 8 по данным задачи 1 изохорного процесса, приведенным на стр.34-35. Деформационная работа, совершаемая в изотермическом процессе 8-5 где
Техническая работа, совершаемая в рассматриваемом процессе:
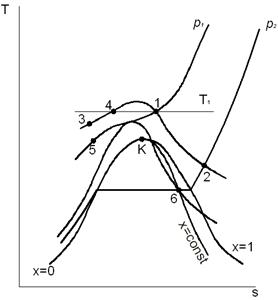
Результаты определения термодинамических свойств и расчета значений работы по диаграмме и таблицам удовлетворительно согласуются между собой (с учетом меньшей точности определения свойств по диаграмме, особенно значения v). Изоэнтропный процесс На рис. 3.9 изображены в координатах T, s и h, s три изоэнтропных процесса расширения: 1-2 – процесс в перегретом паре; 3-4 – во влажном паре; 5-6 – процесс, начинающийся в области перегретого пара (точка 5) и оканчивающийся во влажном паре (точка 6); Рассмотрим особенности расчета и исследования этих процессов с помощью диаграммы h, s и таблиц термодинамических свойств воды и водяного пара.
Рис. 3.9. Изображение адиабатных процессов на энтропийных диаграммах T,s и h,s Задача 1. Определить деформационную и техническую работы обратимого адиабатного расширения 1 кг пара (процесс 1-2на рис. 3.9). Начальные параметры пара р1 = 4,0 МПа, t1 = 400°С, конечное давление р2 = 1,0 МПа. Задачу решить с помощью диаграммы h, s, а затем уточнить по таблицам термодинамических свойств воды и водяного пара. Решение задачи с помощью диаграммы h,s . На пересечении изобары р1 = 4,0 МПа(черная линия) с изотермой t1= 400°С(красная линия) определяем положение точки 1 и термодинамические свойства в этом состоянии: удельный объём v1= 0,073 м3/кг; энтальпия h1= 3214 кДж/кг; энтропия s1 = 6,77 кДж/(кг·К). Как известно обратимый адиабатный процесс является изоэнтропным. Поэтому на пересечении изоэнтропы s2 = s1 = 6,77 кДж/(кг·К) с изобарой р2 = =1,0 МПа определяем положение точки 2 и термодинамические свойства пара в конце расширения: удельный объём v2 = 0,21 м3/кг; энтальпия h2 = =2864,0 кДж/кг. Деформационная работа изоэнтропного процесса:
где
Техническая работа этого процесса
Решение задачи с помощью таблиц термодинамических свойств воды и водяного пара. По табл. ІІІ ([3], стр.118) при р1 = 40 бари t1 = 400°С определяем термодинамические свойства пара в точке 1: удельный объём v1 = 0,07339 м3/кг; энтальпия h1 = 3214,5 кДж/кг; энтропия s1 = 6,7713 кДж/(кг·К). По этой же таблице (стр.98) рассчитываем термодинамические свойства в точке 2 из условия: s2 = s1 = 6,7713 кДж/(кг·К) и р2 = 10бар. Для этого, взяв в “оперативную память” значение s2=6,7713, на изобаре 10 бар в колонке s ищем, между какими значениями sі и si+1 находится значение 6,7713. В рассматриваемом случае s2 = 6,7713 находится между sб = 6,7921 и sм=6,7442. Тогда коэффициент интерполяции, определяемый по s:
Используя значение ks, рассчитываем искомые термодинамические свойства пара в точке 2:
При расчете t2, v2и h2 в качестве их “больших” и “меньших” значений принимаются величины, соответствующие sб и sм, даже если их истинные значения не соответствуют понятию “большая” и “меньшая”. Деформационная работа рассматриваемого процесса:
где
Техническая работа:
Результаты расчетов, выполненных двумя способами, согласуются вполне удовлетворительно. Более существенные расхождения значений деформационной работы объясняются меньшей точностью определения по диаграмме h,s значений удельного объема, используемых при расчете внутренней энергии. Задача 2. До какой температуры, необходимо изобарно нагреть пар, находящийся в состоянии 2 (см. предыдущую задачу, рис.3.9), чтобы при последующем обратимом адиабатном расширении до давления р6=0,01 МПа (процесс 5-6 рис. 3.9) влажность пара не превышала бы 10%. Сколько технической работы при этом будет получено в совокупности процессов (1-2-5-6, рис. 3.9). Задачу решить с помощью диаграммы h,s, а затем уточнить по таблицам термодинамических свойств воды и водяного пара. Решение задачи с помощью диаграммы h,s . В условии задачи сказано, «чтобы влажность пара в конце адиабатного расширения 5-6 не превышала 10%.» Это значит, что степень сухости пара в точке 6 должна быть не ниже 90%, то есть х6 = 0,9. Тогда на пересечении изолинии х = 0,9 с изобарой р6 = 0,01 МПаполучаем точку 6 (рис. 3.10), и определяем термодинамические свойства в этой точке: удельный объём v6 = 13 м3/кг, энтальпию h6 = 2344 кДж/кг и энтропию s6 = =7,4 кДж/(кг·К).
Рис. 3.10. Определение состояния и свойств пара по заданным значениям степени сухости и давления с помощью диаграммы h,s Из точки 6 проводим вверх изоэнтропу до пересечения с изобарой р2 = =1,0 МПа. Получаем точку 5 и определяем термодинамические свойства пара в этой точке: температуру t5 = 380°С; удельный объём v5= 0,3 м3/кг; энтальпию h5 = 3220 кДж/кг; энтропию s5 = s6= 7,4 кДж/(кг·К). Значение t5=380°Сявляется ответом на первый вопрос задачи. Суммарная техническая работа в рассматриваемой совокупности процессов 1-2-5-6 равна:
где
Решение задачи с помощью таблиц свойств воды и водяного пара. Из условия задачи следует, что х6 = 0,9. Тогда из тождества:
определяем значения свойств в состоянии 6:
При этих расчетах значения v’’, v’, h’’, h’ и s’’, s’ взяты из табл. 1 приложения при давлении 0,01 МПа. Термодинамические свойства пара в точке 5 определяем из условия s5 = =s6 = 7,4004 кДж/(кг·К) и р5 = р2 = 1,0 бар. Взяв в «оперативную память» значение 7,4004, в колонке s изобары 1,0 бар, ищем, между какими значениями siи si+1 находится это значение. В данном случае значение s5=7,4004 находится между sб=7,4019 и sм=7,3855. Тогда коэффициент интерполяции, определяемый по s:
С помощью значения ks, рассчитываем параметры пара в точке 5:
Итак, пар должен быть изобарно перегрет до температуры t5=379,54°С, чтобы при последующем обратимом адиабатном расширении до давления 0,01 МПа его влажность не превышала бы 10%. Суммарная техническая работа в рассматриваемой совокупности процессов 1-2-5-6 равна:
где
lтех,2-5=0,
Итак, результаты расчета технической работы отдельных процессов и суммарной по диаграмме h,s и по таблицам термодинамических свойств воды и водяного пара практически совпали. Процесс дросселирования Дросселированием называется термодинамический процесс необратимого перетекания газа (жидкости) от большего давления к меньшему без совершения работы. Дросселирование, протекающее без теплообмена с окружающей средой, называется адиабатным. Этот процесс происходит при большом местном сопротивлении, когда можно пренебречь изменением кинетической энергии рабочего тела. Из основного уравнения термодинамики для потока:
следует, что при адиабатном дросселировании h1=h2, то есть начало и конец процесса находятся на линии h=const (на изоэнтальпе).
Рис. 3.11. Изображение процесса дросселирования на энтропийных диаграммах Поскольку признаком необратимости процесса является рост энтропии рабочего тела на энтропийных диаграммах конечная точка процесса дросселирования всегда лежит правее начальной (рис. 3.11). Необратимый процесс на диаграммах состояния рабочего тела изображается штриховой линией. При дросселировании температура рабочего тела может понижаться, повышаться, либо не изменяться. Если процесс дросселирования протекает правее максимума изоэнтальпы на диаграмме T,s либо правее минимума изотермы на диаграмме h,s (процесс 1-2), то температура рабочего тела понижается (дроссель-эффект αh=(∂T/∂p)h > 0). Если же процесс начинается и оканчивается левее соответствующих экстремумов этих линий (процесс 3-4), то температура рабочего тела повышается (αh < 0). Кривая, соединяющая соответствующие экстремумы и разделяющая области параметров, в которых дроссельный эффект имеет разные знаки, называется кривой инверсии. На кривой инверсии αh = 0. Если процесс начинается в области αh < 0, а оканчивается в области αh > 0 (процесс 5-6), то в итоге может произойти как понижение, так и повышение температуры рабочего тела по сравнению с первоначальной, в зависимости от протяженности участков процесса в указанных областях. Процесс дросселирования является одним из четырёх основных процессов холодильных циклов большинства парокомпрессорных холодильных машин. Он используется для понижения температуры рабочего тела (хладагента) от температуры конденсации до температуры кипения. Заменяя расширительный механизм (детандер) дроссельным клапаном, мы существенно упрощаем (удешевляем) холодильную установку. Рассмотрим примеры решения задач, в которых рабочее тело (вода и водяной пар) совершают процесс дросселирования. Задача 1. Определить термодинамические свойства пара, получаемого при дросселировании насыщенной жидкости (воды), находящейся при температуре 300°С, до нормального атмосферного давления. Решение. Поскольку область жидкости на диаграмме h,s не приведена, эту задачу можно решить только с помощью таблиц свойств воды и водяного пара, в частности с помощью табл. 1 приложения. Энтальпия насыщенной жидкости при температуре 300°С равна h1 = =1345,4 кДж/кг, а давление p1 = 8,5917 МПа (точка 5 на рис. 3.11). При дросселировании этой жидкости до атмосферного давления получается влажный пар (точка 6), степень сухости которого рассчитывается из соотношения:
где h2 = h1= 1345,4 кДж/кг; h’=419,06 Тогда остальные свойства влажного пара в конце дросселирования:
Задача 2. Вода при температуре 40°С и давлении 50 бар дросселируется до давления 0,005 МПа. Определить состояние рабочего тела в конце дросселирования и его термодинамические свойства. Решение По таблице свойств воды и водяного пара ([3] стр. 124) определяем энтальпию и энтропию воды в начальной точке процесса дросселирования (точка 7 на рис. 3.11). Из таблицы для состояния насыщения видно, что h’<h< h’’, то есть конечная точка процесса (точка 8) соответствует состоянию влажного пара. При дросселировании h8 = h7 = 171,9 кДж/кг, тогда
Остальные термодинамические свойства влажного пара в конце процесса t8= ts= 32,9°C — это температура насыщения при давлении 0,05 бар,
Следовательно, температура образовавшегося влажного пара ниже температуры воды на 7,1°C, а его энтропия вследствие необратимости процесса дросселирования больше на 0,0175 кДж/(кг·К). Задача 3. До какого давления необходимо дросселировать перегретый пар, находящийся при температуре 310°С и давлении 9 МПа, чтобы он стал насыщенным. Задачу решить с помощью диаграммы h,s, а затем уточнить по таблицам свойств воды и водяного пара. Решение задачи с помощью диаграммы h,s. На пересечении изотермы t1 = 310°С и изобары р1 =9 МПа, находим начальную точку 1. Из полученной точки проводим линию h1= const (горизонтальная линия) до пересечения с пограничной кривой. Поскольку пограничная кривая пара на диаграмме h,s имеет максимум, а начальная точка заданного процесса находится в однофазной области левее этого максимума, то линия h1=const пересекает эту кривую в двух точках (2 и 3) при давлениях 6,2 МПа и 1,15 МПа. Поэтому при дросселировании пара от состояния 1 до указанных давлений он станет насыщенным (но его термодинамические свойства в этих состояниях, естественно, будут различными). При дросселировании до любого промежуточного давления пар на выходе будет влажным. Решение задачи с помощью таблиц термодинамических свойств воды и водяного пара. В таблице свойств воды и водяного пара ІІІ [3] находим изобару 90 бар (стр.137) и при температуре 310°Сопределяем свойства пара: удельный объём v1 = 0,02142 м3/кг; энтальпию h1 = 2781,8 кДж/кг; энтропию s1 = =5,7163 кДж/(кг·К). Затем, используя табл. ІІ, интерполяцией по значению энтальпии h1 = =2781,8 кДж/кг определяем свойства в точках 2 и 3: Точка 2:
Следовательно, при дросселировании пара от давления 90 бар до 61,36 его температура уменьшилась на 32,97°С; энтропия увеличилась на 0,1609 кДж/(кг·К); а удельный объём увеличился в 1,48 раза. Точка 3:
В данном случае температура пара уменьшилась на 124,21°С; энтропия увеличилась на 0,2773 кДж/(кг·К); а удельный объём увеличился в 7,98 раза.
Процесс течения Основное уравнение термодинамики для стационарного (установившегося) потока, когда отсутствует техническая работа имеет вид:
откуда
Следовательно, в общем случае приращение кинетической энергии рабочего тела происходит за счёт уменьшения его энтальпии и подводимой извне теплоты. С другой стороны, в [2] показано, что изменение кинетической энергии потока равно технической работе статического процесса расширения, уравнение которого совпадает с уравнением процесса, совершаемого движущимся элементом
Приведенные уравнения справедливы как при наличии, так и при отсутствии в потоке трения, обусловленного силами вязкости, поскольку закон сохранения энергии, на основании которого получены эти уравнения, справедлив для любых процессов. Течение без трения и теплообмена (обратимое или идеальное адиабатное течение) является изоэнтропным, и для него справедливо равенство
Тогда скорость потока (м/с) на выходе из канала равна:
если значения энтальпии подставлять в Дж/кг. При истечении из сосуда большого объема (w1=0) и при подстановке значений h в кДж/кг формула (3.5) преобразуется к виду
На практике имеет место реальное (необратимое) адиабатное течение при наличии трения. Действительная скорость с учетом трения рассчитывается через скорость идеального течения:
где φ – скоростной коэффициент, определяемый по опытным данным. Он всегда меньше 1, зависит от рода движущегося вещества, степени шероховатости поверхности канала и других факторов. Для сопел паровых турбин значения φ находятся в пределах 0,95…0,98. Поскольку необратимый процесс (изображаемый штриховой линией) сопровождается ростом энтропии, на энтропийных диаграммах он располагается правее вертикальной линии обратимого изоэнтропного процесса расширения s=idem, проведенной из общей начальной точки. Из уравнений (3.5) и (3.7) при w1 = 0 следует
где Из формулы (3.8) следует
где Итак, если на диаграмме h, s от начальной точки изоэнтропы расширения (1-2) отложить вниз отрезок φ2(h1-h2) либо от конечной точки 2 отложить вверх отрезок ζ·(h1-h2) и из полученной точки провести горизонтальную линию до пересечения с изобарой р2, то точка их пересечения 2' будет соответствовать реальному конечному состоянию потока рабочего тела. Таким же образом можем определить положение промежуточных точек действительного процесса истечения рабочего тела (1-2') (рис.3.13)
Рис. 3.13. Обратимый (1-2) и действительный (1-2’) процессы течения рабочего тела на диаграмме h,s, где 1-а=φ2(h1- h2),2-a=ζ(h1 – h2) . Для определения профиля канала, по которому движется поток, и для обеспечения заданного режима его движения необходимо рассмотреть вопрос о форме струи потока. В [2] на основании уравнения (3.3) получено соотношение между скоростью течения и поперечным сечением струи пара (газа) в дифференциальной форме:
где w/a=M – отношение скорости потока к местной скорости распространения звука в движущемся потоке (так называемое число Маха). Из этого уравнения следует ряд важных выводов. Так, для увеличения скорости потока (dw>0): - при дозвуковых скоростях потока (w< a или M<1) его струя должна сужаться (df < 0); - при сверхзвуковых скоростях потока (w>a или M >1) сечение струи должно увеличиваться (df >0); - для последовательного увеличения скорости потока от дозвуковых до сверхзвуковых значений, поперечное сечение струи сначала должно уменьшаться (df <0), а затем увеличиваться (df >0). При этом в минимальном сечении df=0и М=1, то есть скорость потока равна местной скорости звука. Естественно, профиль канала, по которому движется газообразное рабочее тело, должен соответствовать указанным формам струи во избежание потерь кинетической энергии потока. Скорость звука в жидкостях существенно больше, чем в газах, поэтому течение жидкости всегда происходит при дозвуковых скоростях, и для увеличения скорости потока жидкости сечение канала должно уменьшаться (df < 0). Для замедления потока газа, движущегося со сверхзвуковой скоростью (М >1), до дозвуковой скорости (М<1) канал также должен иметь сначала сужающуюся, а затем расширяющуюся части. При адиабатном течении с трением описанная выше форма струи сохраняется, но в расчетном минимальном сечении скорость потока отличается от местной скорости звука. Так, при ускоренном движении потока сечение, в котором М=1, смещается в расширяющуюся часть струи (канала). Скорость потока, совпадающая с местной скоростью звука, называется критической, а давление газа (пара) в соответствующем сечении — критическим давлением истечения рк (не путать с критическим давлением в критической точке состояния реального газа). Отношение критического давления истечения рк к давлению заторможенного потока в начальном сечении р1 (где можно пренебречь начальной скоростью потока w1), называется критическим отношением давлений βк=pк/p1. Если отношение конечного давления истечения (давления среды, в которую проходит истечение) ра, к начальному давлению р1, больше значения βk (ра/р1>βк), то канал должен иметь только сужающуюся часть, в противном случае (ра/р1<βк) он должен иметь также расширяющуюся часть. Сопло, состоящее из сужающейся и расширяющейся частей, называется соплом Лаваля. Для изоэнтропного течения идеального газа значение βк определяется аналитически и зависит от числа атомов в молекуле: - для двухатомных газов βк = 0,528; - для трехатомных газов βк = 0,546. Для водяного пара, как реального газа, βк является переменной величиной, зависящей от начального термодинамического состояния потока: - в области перегретого пара при умеренных давлениях βк = 0,546; - для насыщенного пара βк = 0,577; - для оценочных расчетовβк можно принимать равным 0,5. Профилирование сопла заключается в определении зависимости площади его поперечного сечения от длины сопла. Чаще всего расширяющаяся часть сопла имеет коническую форму. Угол раствора этой части γ не должен превышать 11…12° во избежание отрыва потока от стенок канала. Тогда, для определения длины расширяющейся части сопла, достаточно рассчитать значения диаметра минимального и максимального (выходного) сечений (dmin и d2). Тогда длина расширяющейся части сопла определяется из соотношения:
Сужающаяся часть сопла чаще всего не рассчитывается, а профилируется так, чтобы входной участок плавно сопрягался с минимальным сечением. Площадь поперечного сечения рассчитывается из уравнения сплошности:
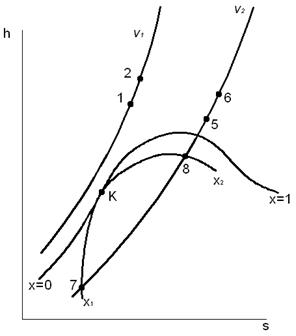
Скорость w определяется из уравнения (3.6) для идеального адиабатного течения потока либо по формуле (3.7) для течения с трением. Значения удельного объема пара (v) определяются по диаграммам либо по таблицам термодинамических свойств рабочего тела. Рассмотрим примеры решения задач, в которых рабочее тело (вода и водяной пар) совершают процесс истечения. Задача 1. Определить форму канала и выходную скорость идеального адиабатного истечения водяного пара из сопла, если давление заторможенного потока р1 = 2,0 МПа, температура – 400°С. Давление среды, в которую происходит истечение пара, равно ра = 0,01 МПа. Решение. Определяем форму канала, которая обеспечит идеальное ускорение (без энергетических потерь) потока, движущегося под действием указанной разности давлений. Для этого определяем отношение:
Поскольку β < βк (для перегретого пара βк = 0,546), сопло должно иметь сужающуюся и расширяющуюся части. Как указано выше, такой канал называется соплом Лаваля. Скорость идеального истечения газа (пара) рассчитывается из соотношения:
где h1= 3246 кДж/кг – энтальпия пара в начале истечения (при р1 = 2,0 МПа и 400°С); точка 1 определяется на пересечении указанных изобары и изотермы. h2 = 2256 кДж/кг – энтальпия пара в конце истечения (при р2= 0,01 МПа); точка 2 определяется на пересечении изоэнтропы s1=s2 и изобары р2. Задачу можно (и нужно!) решить с помощью таблиц термодинамических свойств воды и водяного пара. По [3] (табл. ІІІ стр. 108) находим значения калорических свойств пара в начальной точке процесса: h1 = 3248,1 кДж/кг, s1 = 7,1285 кДж/(кг·К). Значение энтропии в конце изоэнтропного процесса истечения s2 = s1 = =7,1285 кДж/(кг·К). Так как s2< s'' = 8,1505 кДж/(кг·К) при давлении р2 = =0,1 бар, то пар в конце истечения влажный. Тогда по [3] (табл. ІІ стр.62) при р=0,1 бар рассчитываем степень сухости и энтальпию пара в конце процесса
Тогда скорость идеального истечения пара
Сопоставляя значения w2, рассчитанные с помощью таблиц [3] и диаграммы h,s, можно сделать вывод, что они практически совпали. Задача 2. Определить теоретическую скорость адиабатного истечения пара из отверстия трубопровода в атмосферу, если давление пара 1,0 МПа, а температура 500°С. Как изменится скорость истечения, если при той же температуре давление пара в трубопроводе уменьшится до 0,16 МПа. Решение. Давление среды, в которую происходит истечение – атмосферное, то есть ра = 1 бар = 0,1 МПа. Тогда отношение ра/р1=0,1, то есть значительно меньше критического βк. Следовательно, для максимального ускорения потока пара при заданном соотношении давлений надо применить сопло Лаваля. Однако истечение происходит не из сопла Лаваля, поскольку в условии задачи сказано “адиабатное истечение из отверстия трубопровода”. Из диаграммы h,s следует, что процесс совершается в области перегретого пара, для которого можно принять значение βк=0,546 как для трехатомного газа. Тогда критическое давление истечения равно:
Из теории известно, что если значение конечного давления истечения ра становится меньше рк, то не происходит дальнейшего ускорения потока, а возникает его завихрение при выходе из отверстия, то есть потеря энергии. Тогда на пересечении изобары р1 = 1,0 МПа и изотермы t1 = 500°Сопределяем положение точки 1 (начало процесса) и значение h1 = 3476кДж/кг. Проведя из точки 1 изоэнтропу до пересечения с изобарой р2 = рк = 0,546 МПа, определяем значение энтальпии в точке 2 – h2 = 3278 кДж/кг. Скорость идеального истечения пара из отверстия трубопровода равна:
Во втором случае (при р1 = 0,16 МПа и t1=500°С) процесс истечения также проходит в области перегретого пара, однако отношение ра/р1 = 0,1/0,16 = =0,625 > βк = 0,546. Следовательно, скорость истечения пара из отверстия меньше критической. Определив по диаграмме h,s значения h1 =3488 кДж/кг и h2 = 3328 кДж/кг, рассчитываем теоретическую скорость идеального истечения пара из отверстия:
Уточним решение этой задачи с помощью таблиц термодинамических свойств воды и водяного пара. В первом случае значения энтальпии и энтропии пара в начальном состоянии (при р1 = 10 бар и t1 = 500°С) равны: h1 = 3478,3кДж/кг, s1= =7,7627 кДж/(кг·К)(табл. ІІІ стр.99 [3]). Значение энтальпии пара при рк = =5,46 бар определим из условия s2 = s1 = 7,7627 кДж/(кг·К) методом двойной интерполяции. Сначала интерполируем на изобарах рм = 5,0 бар и рб = 5,5 бар по энтропии s2=7,7627 кДж/(кг·К), затем по давлению kp= (5,46-5,0)/(5,5-5,0) = = 0,92; в итоге получим h2 = 3277,6 кДж/кг. Тогда скорость истечения
Во втором случае, когда давление пара в трубопроводе понизилось до 1,6 бар, значения энтальпии и энтропии пара в начальном состоянии (при р1 = =1,6 бар и t1 = 500°С) равны h1 = 3487,3 кДж/кг, s1 = 8,6171 кДж/(кг·К). Значение энтальпии в конце процесса истечения в этом случае определяем из условия р2 = 1 бар и s2 = s1 = 8,6171 кДж/(кг·К). Интерполяцией по энтропии на изобаре 1 бар определяем h2 = 3328,2 кДж/кг. Тогда скорость истечения
Расхождение при определении скорости истечения с помощью диаграммы h,s и таблиц термодинамических свойств воды и водяного пара составляет 0,71% в первом и 0,34% во втором случае (точность расчетов по таблицам выше, чем по диаграмме). Задача 3. Перегретый пар с начальными параметрами р1 = 14,0 МПа и t1= 450°Свытекает в среду с давлением ра = 2,2 МПа. Определить форму и размеры канала, обеспечивающего максимальное ускорение потока пара, действительную скорость истечения и размеры сопла, если скоростной коэффициент φ=0,96, а расход пара т=6,4 кг/с. Решение. Рассчитываем отношение давлений β = ра/р1 = 2,2/14,0 = 0,1571. Поскольку β<βк (0,1571<0,546), канал должен иметь как сужающуюся, так и расширяющуюся части, то есть для максимального ускорения потока надо использовать сопло Лаваля. В соответствии с рассмотренным выше алгоритмом расчета адиабатного процесса истечения, определяем значения энтальпии пара в начальном и конечном состояниях процесса (на входе и выходе из сопла): h1 = 3176 кДж/кг, h2 = 2744 кДж/кг. Действительная скорость истечения рассчитывается по формуле:
Для расчета площади выходного сечения сопла f2 определяем действительное значение энтальпии
|
||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 376. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |



 .
. ,
, .
.
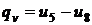 ,
, ,
, .
. .
.



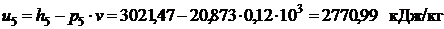




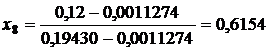 .
.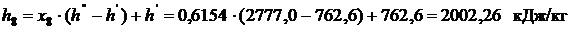






 . Применительно к рассматриваемому случаю
. Применительно к рассматриваемому случаю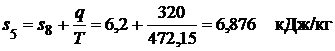 ,
, ,
,
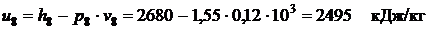
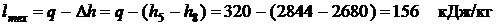

 .
.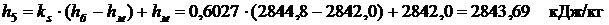



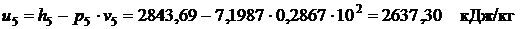

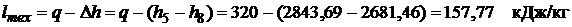
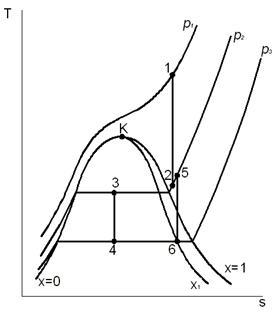

 ,
,
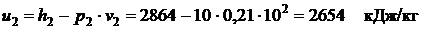


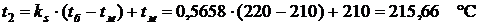
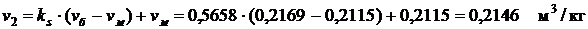

 ,
,



 ,
,
 (техническая работа изобарного процесса равна нулю)
(техническая работа изобарного процесса равна нулю)


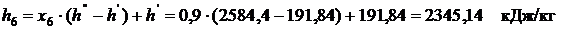
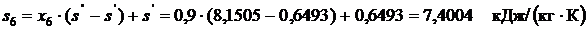




 ,
, ,
, .
.

 ,
, и h’’ =2676,3 кДж/кг – энтальпия насыщенных жидкости и пара при атмосферном давлении р2= 0,101325 МПа.
и h’’ =2676,3 кДж/кг – энтальпия насыщенных жидкости и пара при атмосферном давлении р2= 0,101325 МПа.




 Рис. 3.12. Дросселирование перегретого пара до состояния насыщения
Рис. 3.12. Дросселирование перегретого пара до состояния насыщения , тогда
, тогда
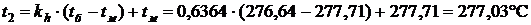


 , тогда
, тогда


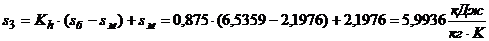
 (3.1)
(3.1) (3.2)
(3.2) . (3.3)
. (3.3) . (3.4)
. (3.4) , (3.5)
, (3.5) . (3.6)
. (3.6) , (3.7)
, (3.7) , (3.8)
, (3.8) >
>  – действительное значение энтальпии в конце истечения при фиксированном значении р2.
– действительное значение энтальпии в конце истечения при фиксированном значении р2. , (3.9)
, (3.9)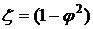 – коэффициент потери энергии.
– коэффициент потери энергии.
 (3.10)
(3.10) (3.11)
(3.11) (3.12)
(3.12)