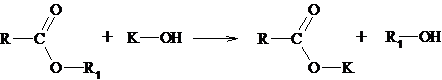Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Реакция с реактивом ФелингаАльдегиды жирного ряда восстанавливают двухвалентную медь в одновалентную. В качестве реактива, содержащего ионы двухвалентной меди, применяется реактив Фелинга. Его готовят перед употреблением, смешивая
Ароматические альдегиды эту реакцию не дают. Методика проведения: приготавливают в пробирке реактив Фелинга, сливая по 1 см3 исходных растворов, и прибавляют 2 см3 1%-ного раствора глюкозы. Верхнюю часть содержимого пробирки нагревают в пламени горелки до начала кипения и наблюдают появление желтого или красного осадка оксида меди (I). Параллельно проводят реакцию с формалином и бензальдегидом, прибавляя к 2 см3 реактива Фелинга (по отдельности) по 2-3 капли формалина и 1-2 капли бензальдегида. Наблюдают происходящие изменения. Карбоксильная группа Реакция на кислотность среды Карбоновые кислоты, будучи кислотами средней силы (Ка =10-3-10-5), приближаются по силе к фосфорной кислоте (Ка = 8×10-3). Они диссоциируют в водном растворе и изменяют окраску индикатора (лакмус или метиловый оранжевый). Методика проведения:к 10%-ному раствору исследуемого вещества в воде добавляют 2-3 капли раствора индикатора или помещают на полоску универсальной индикаторной бумаги; наблюдают изменение окраски. Аналогичную реакцию дают также сульфокислоты , нитрофенолы и некоторые другие соединения с «кислым» атомом водорода. Реакция с гидрокарбонатом натрия  Карбоновые кислоты вытесняют из гидрокарбоната натрия диоксид углерода: NaHCO3 + RCOOH ¾® RCOONa + H2O + CO2 Методика проведения:в пробирку наливают 2 см3 насыщенного раствора гидрокарбоната натрия и 0,2 см3 50%-ного исследуемого раствора в спирте или в воде. При наличии кислоты выделяются пузырьки СО2. Качественная реакция a-оксикислот с хлоридом железа (III) a-Оксикислоты вытесняют фенол из комплексного фенолята и фиолетовая окраска раствора переходит в желтую. В присутствии молочной кислоты фиолетовый цвет железного комплекса изменяется на зеленовато-желтый вследствие образования лактата железа – молочнокислого железа: CH3–CH(OH)–COOH + FeCl3 ¾® [CH3–CH(OH)–COO]3Fe + 3HCl. Методика проведения:в две пробирки вводят по 1 капле 0,1н раствора хлорного железа и добавляют по 2 капли водного раствора фенола. Растворы окрашиваются в фиолетовый цвет. В одну пробирку добавляют две 5% - ного раствора молочной кислоты, а в другую – столько же капель аналогичного раствора уксусной кислоты. В пробирке с молочной кислотой появляется зеленовато-желтое окрашивание, в пробирке с уксусной кислотой цвет раствора не изменяется. 2.4.4 Качественная реакция бензойной кислоты с хлоридом При добавлении к насыщенному раствору бензойной кислоты 5%-ного раствора хлорида железа (III) выпадает красновато-коричневый осадок бензоата железа: 3C6H5COOH + FeCl3 ¾® (C6H5COO)3Fe + 3HCl. Обнаружение сложного эфира Методика проведения: к раствору 100-500 мг сложного эфира в 3-5 см3 спирта приливают несколько капель раствора фенолфталеина и прибавляют по каплям 0,5н спиртовой раствор гидроксида калия. Возникшая в начале красная окраска вскоре исчезает. Эта проба на омыление дает положительный результат не только для сложных эфиров, но и для лактонов, ангидридов.
Углеводы |
||
|
Последнее изменение этой страницы: 2018-06-01; просмотров: 501. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |