Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
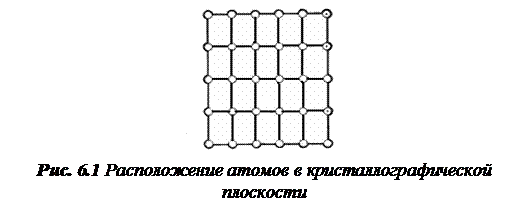
Строение металлов. Понятие о кристаллической решеткеМеталлы и сплавы — это твердые кристаллические вещества. Характерной особенностью кристаллического состояния вещества является правильное, закономерное расположение атомов (рис. 6.1) в пространстве. У металлов и сплавов атомы в кристалле расположены в строго определенном порядке и образуют так называемую пространственную решетку, в узлах которой находятся положительно заряженные ионы, а между ними перемещаются свободные электроны.
Металлы легко вступают во взаимодействие с неметаллами, отдавая валентные электроны. Это объясняется тем, что у металлов все валентные электроны, непрочно связаны с ядром и количество их невелико. Эти же свойства, металла лежат и в основе электропроводности, так как электроны, заряженные отрицательно, создают ничтожную разность потенциалов, что обеспечивает, их перемещение к положительно заряженному полюсу и тем самым появлению электрического тока. Таким образом, слабая связь валентных электронов с ядром определяет физические и химические свойства металлов. Металлы, как правило, хорошо проводят электричество и теплоту, обладают характерным металлическим блеском, непрозрачны, пластичны. Такими же свойствами обладают и металлические сплавы — более сложенные вещества, состоящие из нескольких элементов как металлов, так и неметаллов.
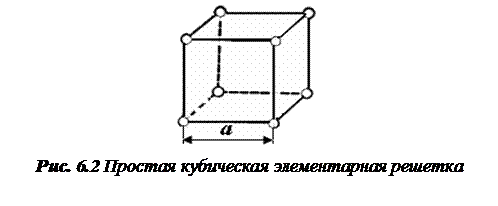
Все металлы условно подразделяют на черные и цветные. К черным металлам относят железо и сплавы на основе железа. К цветным металлам относят медь, никель, цинк, свинец, алюминий, магний, титан и др. Расположение атомов в, кристалле условно можно изображать различными схемами, но чаще всего, в виде пространственных, так называемых элементарных кристаллических ячеек, многократным повторением которых можно воспроизвести пространственную кристаллическую решетку. Расстояние между атомами, в кристаллической решетке называют параметрами решетки и обозначают а и с. Они измеряются в ангстремах Å (1Å=10-8см). Простейшей элементарной кристаллической решеткой является простая кубическая решетка с параметром а (рис. 6.2). Для металлов, наиболее распространенные типы кристаллических решеток (рис. 6.3, а — в): а — кубическая объемно-центрированная, которую имеют W, Mg, V, Cr, Feα ; б — кубическая гранецентрированная, которую имеют Pb, Feγ, Al, Cu, Ni; в — гексагональная плотноупакованная, которую имеют Тiα, Mg, Zn, Ве. В перечисленных решетках каждый атом окружен максимальным геометрически допустимым числом атомов, соответствующим плотнейшей упаковке шаров одного и того же размера. Некоторые металлы, например олово, индий, галлий, немеют тетрагональную решетку с параметрами а и с, которая в зависимости от расположения атомов в пространстве (как кубическая) может быть простой, объемно- и гранецентрированной. 
|
|||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 548. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |