
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Тема 6. Средняя энергия молекул
Каждая молекула характеризуется числом степеней свободы (i) – это количество независимых движений, которые может совершать молекула: 1) одноатомная молекула может совершать три поступательных движения вдоль направлений координатных осей: i=3(пост); 2) двухатомная молекула с жесткими связями может совершать три поступательных и два вращательных движения: i=3(пост)+ 2 (вращ)=5; 3) трехатомная молекула и более может совершать три поступательных и три вращательных движения: i=3(пост)+ 3 (вращ)=6; 4) если связи между атомами внутри молекулы не жесткие, она совершает колебательные движения – добавляются колебательные степени свободы. Полное число степеней свободы молекулы:
Например, молекула Н2 двухатомная с жесткими связями – число степеней свободы равно 5. Закон равнораспределения энергии по степеням свободы молекулы: на каждую поступательную и вращательную степень свободы молекулы приходится одинаковая порция энергии Тогда полная энергия молекулы, равна: где i – число степеней свободы молекулы. Энергия одного моля газа, равна: Энергия произвольной массы газа, равна: U Молярная теплоёмкость газа при постоянном объёме: Молярная теплоёмкость газа при постоянном давлении: Где R = 8,31 Дж/(моль×К), k = 1,38×10-23 Дж/К. Пример 6.1. Средняя кинетическая энергия молекул газа при температуреТ зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место только поступательное и вращательное движение, средняя энергия молекул азота (N2) равна:  £ (7/2)kT R (5/2)kT £ (3/2)kT £ (1/2)kT. Решение: молекула азота двухатомная, число степеней свободы равно 5, следовательно, энергия молекулы равна Пример 6.3. При комнатной температуре отношение СP/СV при постоянном давлении и объеме равно 8/6 для: ð гелия ð воздуха ð водяного пара ð кислорода Решение: чтобы решить это задание нужно найти число степеней свободы молекулы с приведенным отношением теплоемкостей:
посчитаем Число степеней свободы молекулы равно 6 – это трехатомная молекула, из вариантов ответов – это водяной пар Н2О. |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 757. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 .
. , а на каждую колебательную степень свободы двойная порция энергии
, а на каждую колебательную степень свободы двойная порция энергии 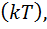 где k – постоянная Больцмана, Т – температура по шкале Кельвина.
где k – постоянная Больцмана, Т – температура по шкале Кельвина. ,
, , где R – универсальная газовая постоянная.
, где R – универсальная газовая постоянная. .
.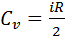 .
. .
. .
. ,выведем формулу для расчета i:
,выведем формулу для расчета i:  ,
,  ,
,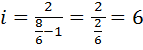 .
.