
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Упругие свойства твёрдых тел· Относительная продольная деформация при продольном растяжении (или сжатии) тела: где · Относительное поперечное сжатие при продольной деформации (рис.2.3): где · Коэффициент Пуассона материала: где
где F – сила, перпендикулярная поперечному сечению тела площадью S (рис. 2.3). · Закон Гука для деформации сжатия-растяжения: Здесь · Тангенциальное механическое напряжение
· Относительная деформация при сдвиге (относительный сдвиг) для малых деформаций (рис. 2.4):
Здесь x – абсолютный сдвиг параллельных слоев тела относительно друг друга; h – расстояние между слоями. · Закон Гука для деформации сдвига:
где G – модуль модуль сдвига. · Связь между модулем Юнга E и модулем сдвига G:
где · Закон Гука для деформации кручения:
где М – момент силы, закручивающий однородный круглый стержень на угол φ; · Потенциальная энергия растянутого или сжатого стержня - при однородной деформации:
- при неоднородной деформации:
где  · Объёмная плотность энергии упругой деформации
где Е – модуль Юнга;
Молекулярная физика · Относительная атомная масса элемента (они приводятся в таблице Д. И. Менделеева) – это масса
· Относительная молекулярная масса вещества – это масса
где · Количество вещества определяется числом структурных элементов (молекул, атомов, ионов и т. п.), содержащихся в системе или теле. Количество вещества выражается в молях (
где m – масса тела (системы); · Молярная масса вещества (масса моля):
где · Связь молярной массы
где · Масса m вещества равна связана с числом молекул N:
где · Массовая доля смеси газов:
где · Средняя молярная масса смеси газов:
где · Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона) связывает параметры газа – давление p, объём
где m – масса газа; · Универсальная газовая постоянная
· Концентрация частиц (молекул, атомов и т. п.) однородной системы – это число частиц в единице объёма:
Здесь N – число частиц; V – объём. · Закон Дальтона для смеси газов. Давление p смеси равно сумме парциальных давлений
где k – число компонент смеси. Основы термодинамики · Первое начало термодинамики. Количество теплоты δQ, сообщённое системе, идёт на приращение её внутренней энергии и dU на работу δA системы против внешних сил: δQ=dU+δA, или · Теплоёмкость тела:
где · Удельная теплоёмкость вещества – это теплоёмкость единицы массы:
где · Молярная теплоёмкость вещества – это теплоёмкость одного моля:
где · Связь между молярной
где · Молярная теплоемкость идеального газа при постоянном объёме
Здесь · Степени свободы; число степеней свободыi – это число независимых координат, однозначно определяющих положение тела (или молекулы) впространстве. Для одноатомных молекулi=3, так как трёх координат (x, y, z) достаточно для того, чтобы однозначно задать положение материальной точки в трёхмерном пространстве. При температурах, не слишком низких и не слишком высоких, для двухатомных молекул i=5; для многоатомных – i=6 (с учётом вращательных степеней свободы). · Показатель Пуассона (показатель адиабаты) – этоотношение теплоёмкости
· Молярные теплоемкости идеального газа при постоянном объёме
· Уравнение Майера
· Внутренняя энергия идеального газа
где · Работа, связанная с изменением объёма газа, в общем случае:
где V1– начальный объём газа; V2– его конечный объём.
где Q1 – количество теплоты, полученное рабочим телом (газом) от нагревателя; Q2 – количество теплоты, переданное рабочим телом охладителю, А – работа за цикл. · КПД цикла Карно (рис. 2.5):
где T1 – температура нагревателя; T2 – температура охладителя. · Энтропия по определению Клаузиуса. Функция состояния системы, дифференциал
Здесь δQ – теплота, полученная системой; Т – её температура. · Изменение энтропии в общем случае:
где 1 и 2 – пределы интегрирования, соответствующие начальному и конечному состояниям системы. Так как процесс равновесный, то интегрирование проводится по любому пути. · Изменение энтропии для процессов с идеальным газом (см. также табл. 3):
Таблица 2 |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 590. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 ,
, – абсолютное удлинение, l – начальная длина тела (рис. 2.3).
– абсолютное удлинение, l – начальная длина тела (рис. 2.3).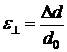 ,
, – изменение диаметра стержня при деформации.
– изменение диаметра стержня при деформации. ,
, – относительная продольная деформация;
– относительная продольная деформация;  – относительное поперечное сжатие.
– относительное поперечное сжатие. · Нормальное механическое напряжение:
· Нормальное механическое напряжение: ,
, , или
, или  .
. .
.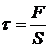 ,
, где F – касательная сила, действующая вдоль слоя тела площадью S (рис. 2.4).
где F – касательная сила, действующая вдоль слоя тела площадью S (рис. 2.4).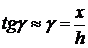 .
. ,
, ,
,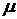 – коэффициент Пуассона материала.
– коэффициент Пуассона материала.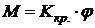 ,
, – постоянная кручения.
– постоянная кручения. ;
;
 ,
, .
. ,
, атома данного элемента, отнесённая к
атома данного элемента, отнесённая к  массы
массы  атома изотопа углерода
атома изотопа углерода  :
:
 молекулы данного вещества, отнесённая к
молекулы данного вещества, отнесённая к  , или
, или 
 – число атомов i-го химического элемента, входящего в состав молекулы данного вещества;
– число атомов i-го химического элемента, входящего в состав молекулы данного вещества;  – относительная атомная масса этого элемента.
– относительная атомная масса этого элемента. ). По закону Авогадро, один моль вещества содержит столько же структурных элементов, сколько содержится атомов в 12 граммах изотопа углерода
). По закону Авогадро, один моль вещества содержит столько же структурных элементов, сколько содержится атомов в 12 граммах изотопа углерода  . Количество вещества равно
. Количество вещества равно , или
, или 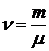 ,
, , или
, или  ,
, – масса одной молекулы;
– масса одной молекулы;  :
: ,
, .
. ,
, ,
, – масса i-го компонента смеси,
– масса i-го компонента смеси,  – масса всей смеси.
– масса всей смеси. ,
, – количество вещества i-го компонента смеси; k – число компонентов смеси.
– количество вещества i-го компонента смеси; k – число компонентов смеси. и термодинамическую температуру
и термодинамическую температуру  :
: , или
, или 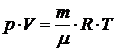 , или
, или  ,
, – универсальная газовая постоянная,
– универсальная газовая постоянная, 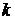 – постоянная Больцмана,
– постоянная Больцмана, 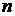 – концентрация молекул газа.
– концентрация молекул газа.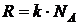 .
. .
.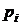 всех компонент смеси:
всех компонент смеси: ,
, .
. ,
, – количество теплоты, сообщённое телу,
– количество теплоты, сообщённое телу,  – соответствующее изменение температуры тела.
– соответствующее изменение температуры тела. ,
, – масса вещества;
– масса вещества;  ,
, и удельной
и удельной  теплоёмкостями:
теплоёмкостями: ,
, и при постоянном давлении
и при постоянном давлении 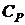 (по определению):
(по определению):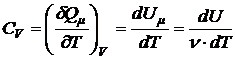 ;
;  .
.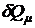 – теплота, сообщённая одному молю газа в соответствующем процессе;
– теплота, сообщённая одному молю газа в соответствующем процессе; 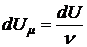 – изменение внутренней энергии одного моля газа;
– изменение внутренней энергии одного моля газа;  .
. (
(  , или
, или  ;
; , или
, или  .
. .
.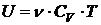 ,
, ;
; 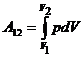 ,
, · Термический коэффициент полезного действия(КПД) в общем случае:
· Термический коэффициент полезного действия(КПД) в общем случае: ,
, ,
, которой в обратимом процессе равен приведённой теплоте, является энтропией:
которой в обратимом процессе равен приведённой теплоте, является энтропией: .
. ,
, .
.