Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
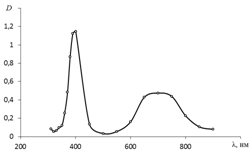
Анализ по Спектрам поглощенияАнализ в УФ-ВС области спектра Фотометрический анализ Анализ разделяют на колориметрию и спектрофотометрию. Колориметрия – метод анализа, основанный на измерении поглощения монохроматического излучения в видимой области спектра. Спектрофотометрия – метод анализа, основанный на применении монохроматического излучения, создаваемого дифракционной решеткой, как в видимой, так и в ближних ультрафиолетовой и инфракрасной областях спектра. Зависимость светопоглощения от длины волны излучения выражается кривой (спектром) поглощения света данным веществом. Спектр поглощения обычно представляют в виде графика, на котором по оси абсцисс откладывают длину волны l, а на оси ординат – оптическую плотность раствора D.
Если светопоглощение раствора подчиняется закону Бугера-Ламберта-Бера, то оптическая плотность раствора прямо пропорциональна концентрации вещества в растворе. В этом случае график зависимости оптической плотности от концентрации выражается прямой линией, идущей из начала координат.
Закон справедлив для разбавленных растворов при концентрации веществ менее 0,01 моль/л. При больших концентрациях частицы, поглощающие свет, настолько близко расположены друг к другу, что каждая частица влияет на распределение заряда соседних частиц, что приводит к изменению способности частиц поглощать свет данной волны и отклонению от закона Бугера-Ламберта-Бера. Значительное отклонение от закона Бугера-Ламберта-Бера связано с немонохроматичностью светового потока. Отклонения от закона связаны и с химическими процессами в растворе - диссоциацией и ассоциацией химических соединений, гидролизом, образованием гидроксокомплексов и гидроксидов, взаимодействием растворителем, образованием кислых солей, изменением состава комплексных соединений в связи со ступенчатым характером их образования и др., влиянием других веществ, присутствующих в растворе.  Отклонения могут быть связаны также с потерями на отражение и рассеяние света молекулами анализируемого вещества и растворителя, т.к. проходя через поглощающий слой (например, раствор) часть светового потока будет селективно поглощаться, часть - проходить сквозь раствор, а часть - отражаться. Потери на рассеяние и взаимодействие с молекулами растворителя и примесями снижают за счет использования растворов сравнения. При проведении анализа сравнивают два потока света, в которых интенсивность отраженного света будет одинакова: один, проходящий через исследуемый раствор, а другой – через раствор сравнения
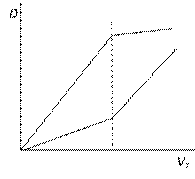
В качестве раствора сравнения используют раствор, в котором содержатся все компоненты, необходимые при анализе элемента, кроме анализируемого вещества. Оптическая плотность раствора равнения обычно автоматически принимается равной нулю прибором. Измеряемая величина оптической плотности, таким образом, зависит только от количества определяемого вещества. Количественное определение вещества методом фотометрии можно выполнять несколькими способами: по значению молярного коэффициента поглощения, методом градуировочного графика, фотометрическим титрованием, методом дифференциальной фотометрии. Определение по значению молярного коэффициента поглощения Готовят ряд стандартных растворов, выбирают длину волны, определяют оптическую плотность стандартных растворов. Из закона Бугера-Ламберта-Бера вычисляют среднее значение молярного коэффициента поглощения. Готовят исследуемый раствор, замеряют его оптическую плотность и вычисляют концентрацию через найденное значение ε. Метод градуировочного графика Готовят серию контрольных растворов с различным содержанием определяемого компонента и измеряют оптическую плотность при определенных длине волны (как правило, lmax) и толщине слоя (толщине кюветы). При данных длине волны и толщине фотометрируемого слоя должен соблюдаться закон Бугера-Ламберта-Бера. Интервал значений оптической плотности должен находиться в пределах максимальной воспроизводи-мости результатов измерений, т.е. D = 0,1–2. По полученным результатам строят график в координатах D - C. Вместо концентрации раствора можно использовать объем стандартного раствора или массу растворенного определяемого элемента. Затем отбирают аликвотную часть исследуемого раствора, прибавляют необходимые по анализу реактивы и измеряют оптическую плотность раствора. По значению оптической плотности раствора находят содержание определяемого компонента по градуировочному графику. Фотометрическое титрование О содержании вещества судят не по интенсивности светопоглощения, а по количеству затраченного реактива, т.е. задача фотометрического титрования – определить точку эквивалентности при помощи фотоэлемента по значению оптической плотности. Фотометрическое титрование применяют в следующих случаях: 1) если в результате титрования образуется окрашенное соединение; 2) если цвет индикатора изменяется постепенно; 3) при титровании окрашенных растворов; 4) при титровании веществ, поглощающих свет в ближних УФ и ИК областях; 5) при титровании очень разбавленных растворов. Точку эквивалентности находят по графику кривой фотометрического титрования в координатах D – VT по месту пересечения двух прямых (точка перегиба).
Фотометрическое титрование позволяет определять концентрацию вещества в пределах от 0,01 до 0,001 моль/л. Дифференциальная спектрофотометрия Данный метод применим для определения сравнительно больших содержаний вещества. В данном случае в качестве раствора сравнения используют какой-нибудь стандартный раствор с известным содержанием определяемого вещества. На приборе измеряется оптическая плотность, представляющая собой разность исследуемого и стандартного растворов. При Сст > Сис (Dcт > Dис) D = Dис - Dcт = εlCис - εlCст = εl(Cис - Cст). При Сст < Сис (Dcт < Dис) D = Dcт - Dис = εlCст - εlCис = εl(Cст - Cис). Оптическую плотность раствора сравнения измеряют по отношению к исследуемому раствору и значение оптической плотности берут с обратным знаком. |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 454. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |