Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Предотвращение контактной коррозии.⇐ ПредыдущаяСтр 14 из 14 Как было показано в разделах 3.2., 3.4., 3.6., контакт разнородных металлов в электролитических средах приводит к образованию гальванического элемента, в котором более электроотрицательный металл служит анодом и растворяется значительно быстрее, чем вне контакта с катодом. Если нельзя избежать подобных контактов, то необходимо помнить, что на плотность анодного тока и, следовательно, на скорость растворения анода существенно влияет соотношение площадей анода и катода. Например, мелкие детали болтовых или каких-либо других соединений, находясь в контакте с многократно превосходящим их по площади поверхности более "благородным" металлом основной конструкции, подвергаются значительному анодному растворению. Подобных сочетаний металлов в конструкциях следует избегать. В общем случае антикоррозионная защита крепежных деталей не должна уступать по качеству защите соединяемых узлов.
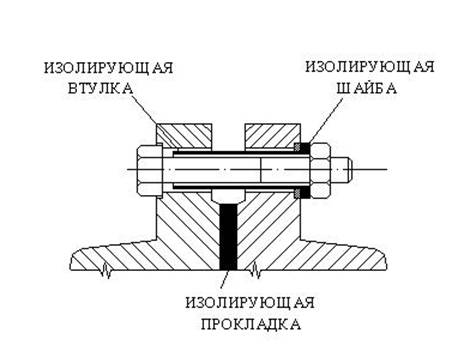
Применение крепежа, изготовленного из более "благородного" металла хотя и нежелательно, но при определенных обстоятельствах (например, при необходимости частого раскрытия соединений) допустимо и представляет гораздо меньшую опасность, чем описанный выше случай обратного сочетания контактирующих металлов. Основной способ защиты от контактной коррозии - изоляция разнородных металлов друг от друга с помощью неэлектропроводных материалов, которую необходимо предусматривать еще на стадии конструирования. Для этого используются различные органические или неорганические покрытия или изолирующие прокладки в виде шайб, втулок и т. д. Пример подобного исполнения болтового соединения приведен на рисунке 4.4.1.  Учет влияния напряженного состояния На скорость коррозии.
Как было показано в разделе 3.6., совместное воздействие агрессивной среды и внешних нагрузок или внутренних остаточных напряжений может значительно ускорить процесс разрушения металла. Более того, наличие напряжений способно изменить механизм и характер коррозионных поражений и привести к развитию специфических видов разрушения - коррозионного растрескивания, коррозионной усталости и т.д. Причиной возникновения в металле остаточных напряжений могут быть операции сварки и штамповки, а также выбранный режим термообработки. При наложении внешних нагрузок особое значение приобретает наличие в конструкции концентраторов напряжений, в которых в результате нерационального конструирования развиваются напряжения, превышающие условный предел коррозионной усталости (при динамических нагрузках) или критическое напряжение (при КРН) для данного материала в данной среде. Кроме того, само наличие участков с различным напряженным состоянием способно вызвать образование коррозионных гальванических элементов и ускорить растворение металла. Поэтому одна из основных задач проектировщика - обеспечить минимальные значения остаточных напряжений и как можно более равномерное распределение напряжений в конструкции. Наиболее часто встречающийся вид концентраторов напряжений - резкие переходы при сопряжении различных поверхностей. Такие переходы следует делать по возможности плавными, применяя выточки, галтели и т.д. Все прямоугольные вырезки исполняются с закругленными углами, а для любых отверстий предпочтительной является форма круга или эллипса. Немаловажное значение имеет и способ изготовления отверстий. Например, напряжения, возникающие при прожигании отверстий могут оказаться достаточными для того, чтобы стать причиной коррозионного растрескивания всей металлоконструкции. Во избежание такого развития событий необходимо либо произвести дополнительную термообработку изделия для снятия сварочных напряжений, либо использовать другой способ получения отверстий (сверление, резание, электрохимическую прошивку и т.п.). Другая ответственная зона концентрации напряжений - конструкции опор. Они должны быть спроектированы таким образом, чтобы по возможности рассредоточить напряжения от опорного узла по поверхности изделия. Например, введение промежуточного подкладного листа, служащего буфером между опорной балкой и наклонным полом грузового вагона, может резко уменьшить изгибающие напряжения в основном листе пола. Проектирование узлов трения, горячей посадки валов и любых других малоподвижных разъемных и неразъемных соединений следует проводить с учетом возможности возникновения фреттинг-коррозии и предусматривать меры по ее минимизации : сочетание мягкого металла с твердым, нанесение металлических и неметаллических покрытий, введение прокладок с высокой упругостью или с низким коэффициентом трения, применение смазок.
4.4.3. Учет распределения температуры между элементами конструкции
Температура является одним из основных внешних факторов как химической, так и электрохимической коррозии. Подробно влияние температуры на скорость растворения металлов в электролитических средах рассмотрено в разделе 3.6. Напомним, что за исключением случаев заметного участия в катодной реакции газообразных деполяризаторов, растворимость которых в открытых системах с ростом температуры падает, во всех остальных случаях скорость коррозионного процесса при повышении температуры существенно возрастает. Наибольшую опасность в процессе эксплуатации химической аппаратуры представляет, с этой точки зрения, возможность возникновения местных перегревов при неудачном распределении потока горячих газов или вследствие ухудшения условий теплообмена из-за образования накипи или осадочных слоев, затрудняющих отвод тепла. В результате температура перегретых участков может превысить критическую для данного материала в данной среде величину и скорость их разрушения резко возрастет. Во избежание подобных последствий необходимо либо предусмотреть меры по улучшению аэродинамики газового потока, либо ввести в конструкцию специальные дополнительные экраны, изготовленные из коррозионностойкого материала и предотвращающие прямое попадание струи горячего газа или жидкости на отдельные участки поверхности. Пример такого конструктивного решения приведен на рисунке 4.4.2. Однако, причиной существенного ускорения коррозионных процессов могут стать не только местные перегревы, но и любые заметные перепады температур между отдельными участками погруженного в электролит металла, даже если температура на всех участках поверхности находится в допустимых регламентированных пределах. Все дело в том, что величина стационарного электродного потенциала в значительной степени зависит от температуры и, следовательно, на участках, находящихся при различной температуре, устанавливаются различные потенциалы. А наличие разности потенциалов между участками одной металлической поверхности неизбежно приводит в этом случае к возникновению так называемого термогальванического коррозионного гальванического макроэлемента.
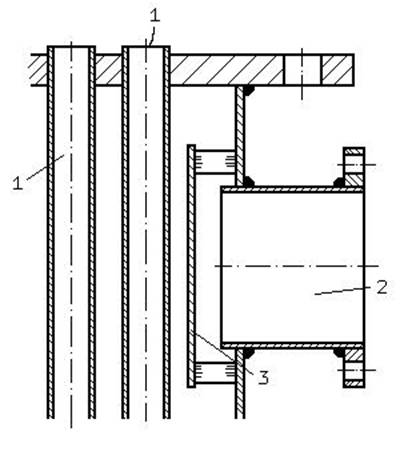
Работа такого макроэлемента и вызывает ускоренное растворение более нагретых(горячих) участков поверхности, которые выполняют роль анодов, в то время как более холодные становятся катодами. Отметим, что величина термогальванического тока во многих случаях соизмерима с током, возникающим при контакте двух разнородных металлов. Причем в большинстве случаев с ростом площади поверхности холодных электродов скорость разрушения горячих увеличивается. Поэтому наибольшую опасность представляет образование локальной зоны, нагретой до высокой температуры, окруженной обширной более холодной поверхностью. Таким образом, задача проектировщика заключается не только в том, чтобы предотвратить чрезмерный нагрев аппарата, но и в том, чтобы свести к минимуму возможность возникновения температурных перепадов. Для этого, например, в резервуарах нагрев или охлаждение которых осуществляется с помощью рубашек, устанавливают мешалки, обеспечивающие постоянство скорости движения жидкости мимо теплопередающей поверхности. А при конструировании различных теплообменных аппаратов и конденсаторов следует исключить возможность образования паровых подушек, препятствующих нормальному теплообмену (см. рис. 4.4.3.). Еще один способ защиты от термогальванической коррозии - использование специальных мер антикоррозионной защиты зон, подвергающихся перегревам.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Приведите классификацию методов защиты металлов от коррозии. 2. Приведите классификацию защитных покрытий и укажите области их применения. 3. Какие Вы знаете способы нанесения металлических защитных покрытий? В чем их преимущества и недостатки? 4. Какие компоненты входят в состав электролитов для электроосаждения металлических покрытий? Каково их назначение? 5. Назовите известные Вам виды неметаллических неорганических защитных покрытий для цветных и черных металлов. 6. Какие основные компоненты входят в состав лакокрасочных материалов? Каковы их функции? 7. Опишите возможные механизмы защитного действия лакокрасочных покрытий. 8. Какие виды электрохимической защиты Вы знаете? 9. В каких случаях применяют катодную и катодно-протекторную защиту? 10.Что такое защитный потенциал металла? 11.Что такое перезащита? 12. Какие материалы используют для изготовления протекторов? 13. В каких случаях необходима дренажная защита? На чем основано ее действие? 14. Какие виды дренажей вы знаете? 15. На чём основано действие анодной защиты? 16. Назовите области применения ингибиторов коррозии. 17. Опишите возможные механизмы действия анодных, катодных и парофазных ингибиторов коррозии. 18. Что представляет собой приведенная шкала потенциалов и как ей пользоваться? 19. Что такое ингибиторы травления? 20. Назовите области применения и недостатки летучих ингибиторов. 21. Какие контактные ингибиторы Вы знаете? Каков механизм их действия? 22. Какие еще способы обработки коррозионной среды Вы знаете? 23. Назовите основные принципы рационального конструирования. 24. Какие факторы необходимо учитывать при конструировании для уменьшения опасности коррозионных поражений? 25. Приведите примеры удачного и неудачного конструирования. Поясните их. 26. В заключаются особенности конструирования сварных соединений?
5. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ.
Пример 1. Определить, возможно ли окисление палладия в воздухе и кислороде при 850 С, если давление диссоциации его оксида при этой температуре (РО2 )равн.= 500 мм.рт.ст. Решение: Давление диссоциации оксида палладия по реакции РdO(т) = Pd(т) + 1/2 O2(г) (РО2)равн. = 500760. = 0,658 атм. Следовательно, процесс окисления Pd в воздухе при этой температуре невозможен, т.к. (РО2 )равн. = 0,658 атм. > (РО2 )возд. = 0,21 атм. К такому же результату приводит и расчет изменеения изобарного потенциала для этой реакции по уравнению: Gт = Gт + RT ln (1/РО2 0,5).= 1140 кал/моль; т.е. Gт > 0 В кислороде этот процесс возможен, т.к. (РО2)равн. <РО2 = 1атм.
Пример 2. Оценить коррозионную стойкость цинка на воздухе при температуре 400С. Образец цинка с поверхностью, равной 30 см2 ,до испытаний имел массу 21,4261 г. После 180-часового окисления на воздухе при температуре 400С его масса возросла до 21,4279 г. Плотность цинка принять равной 7,14 г/см3 . Решение: Находим положительный массовый показатель коррозии: Кm+ = (m2 - m1)/S = (21,4279 - 21,4261)/0,0030 180= 0,0033 г/м2час. Так как при окислении на воздухе Zn образует окисел ZnO, отрицательный массовый показатель коррозии находим по уравнению: Km-= Km+ AZn/AO= 0,0033 65,28/16,00 = 0,01362 г/м2час. Тогда глубинный показатель коррозии: П = Km-/Zn 8,76 = 0,01362 /7,14 8,76 = 0,0167 мм/год. Это по десятибалльной шкале коррозионной стойкости соответствует стойким металлам (балл 4).
Пример 3. Найти обратимый потенциал водородного электрода в нейтральном 1 M растворе NaCl при 25C и Р(H2) = 1 атм. Решение: В нейтральном растворе pH = - lgaH+ = 7,0. Подставляем это значение в уравнение потенциала водородного электрода, учитывая, что Р(H2) = 1 атм. : = RT/F 2,303 lgaH+ = - 0,0591 7,0 = - 0, 414 В.
Пример 4. Определить, возможна ли коррозия железа в воде при pH=7.0 и 25C за счёт водородной деполяризации. В этих условиях произведение растворимости Fe(OH)2 равно 1,65 10-15 , а для воды Кв = 1,008 10-14. Решение: Сопоставим обратимые потенциалы железа и водородного электрода при данных условиях. Активность образующихся при растворении железа ионов Fe2+ в воде: aFe2+= L Fe(OH)2 /(aOH-)2= 1,65 10-15/1,008 10-14 = 0,164. Тогда обратимый потенциал железа: (Fe) = (Fe) + RT/2F 2,303 lgaFe2+ = - 0,44 + 0,0591/2 lg0,164 = - 0,463 В. Потенциал катодного процесса водородной деполяризации, т.е. обратимый потенциал водородного электрода, в рассматриваемых условиях равен: (H) = RT/F 2,303 lg(aH+/(PH2)0,5) , причём lgaH+ = -pH = -7,0 , а PH2 = 5 10-7 атм, т.к. воздух содержит по объёму 5 10-7 % водорода. Тогда получаем: ___ ______ (H) = 0,0591 (lgaH+ - lgРH2) = 0,0591 (-7 - lg5 10-7 ) = -0,228 В. Так как (Fe) = -0,463 < = -0,228, то коррозия железа с водородной деполяризацией в рассматриваемых условиях термодинамически возможна.
Пример 5. .Рассчитать концентрационную поляризацию анода при электролизе 0,1 M водного раствора AgNO3 с серебряным анодом при t = 18C и iк = iа = 1 мА/см2, если известно, что в рассматриваемых условиях коэффициент активности ионов серебра = 0,731, эквивалентная электропроводность иона серебра = 44 Ом-1см2, а число переноса аниона NO3- n- = (1 - n+) = 0,526. Эффективную толщину диффузионного слоя принимаем равной 0,075 см. Решение : Рассчитываем концентрационную поляризацию анода по уравнению: а = RT/nF 2,303 lg(1 + iа/id) Предельная катодная плотность тока id = kd n F/(1 - n+) . , а коэффициент диффузии разряжающихся на катоде ионов серебра kd = RT/nF2. Активность ионов серебра: aAg+ = m/1000 = 0,1 0,731/1000 = 7,31 10-5 . Тогда предельная плотность катодного тока id = 44 8,313 291 7,31 10-5 / 96500 0,075 0,526= = 0,002 А/см2 = 2 мА/см2. Рассчитываем концентрационную поляризацию анода: а = 0,0577 lg(1 + 1/2) = 0,0102 В = 10,2 мВ.
Пример 6. Рассчитать объёмный, массовый и токовый показатели коррозии магния в 0,5N растворе NaCl. Размеры образца 20х20х0,5мм, полное погружение, t = 25C, Р = 760 мм.рт.ст. За 100 часов испытаний выделилось 330,1см3 водорода. Упругость водяного пара в рассматриваемых условиях p(H2O) = 23,8 мм.рт.ст. Решение : Полная поверхность образца: S = (2 2) 2 + (0,05 2) 4 = 8,4см2. Приближённая величина объёмногo показателя коррозии (без приведения объёма выделившегося водорода к нормальным условиям): Kоб.H2 = V/S = 330,1/8,4 100 = 0,393см3/см2 ч. Учтём поправки на температуру и давление (T = 273+25 = 298 K): Kоб.H2 = V 273 (P - p(H2O))/S T 760 = = 330,1 273 (760 - 23,8)/8,4 100 298 760= 0,349см3/см2 ч. Рассчитываем массовый показатель коррозии по уравнению: Km- = Kоб.H2 A(Mg)/n 0,8917 Атомная масса магния A(Mg) = 24,32, заряд ионов Mg n=2 ,тогда Km- = 0,349 24,32 0,8917/2 = 3,784 г/м2 ч. Токовый показатель коррозии рассчитываем по уравнению: i = Kоб.H2 2,3896 10-3 = 8,34 10-4 А/см2 = 0,834 мА/см2.
Пример 7. Дать на основании данных таблицы 5.1. характеристику склонности к межкристаллитной коррозии образцов стали при кипечении в 65 % HNO3. Таблица 5.1.
| |||||||||