
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Исследование химического равновесия
Цель работы: познакомитьсяс явлением химического равновесия, изучить влияние изменения концентрации реагирующих веществ и температуры на смещение химического равновесия.
Оборудование и реактивы: стакан или колба на 50 – 100 мл, пробирки, пипетки капельные, шпатели, колбочка на 50 мл с отогнутой вниз газоотводной трубкой, U-образная трубка с двумя хорошо подобранными резиновыми пробками или две пробирки, соединенные между собой стеклянной трубкой, два стакана на 200 – 250 мл, электроплитка, снег или лед, 0,1М растворы NH4CNS и FeCl3, концентрированные растворы NH4CNS и FeCl3, кристаллический NH4Cl, медные стружки, концентрированная азотная кислота.
6.1 Теоретические пояснения
Химические реакции бывают обратимые и необратимые. Необратимые протекают только в одном направлении, в сторону образования продуктов реакции до полного расходования исходных веществ. Обратимые реакции одновременно протекают в двух взаимно противоположных направлениях. Такие реакции не доходят до конца ни в одном из направлений, ни одно из реагирующих веществ не расходуется полностью. Состояние системы, характеризующееся одновременным протеканием с одинаковыми скоростями двух противоположно направленных химических процессов, называется химическим равновесием. В состоянии равновесия концентрации всех веществ остаются неизменными. Признаки химического равновесия: ˗ состояние системы неизменно во времени при отсутствии внешних воздействий; ˗ состояние системы изменяется под влиянием внешних воздействий, сколь бы малы они ни были; через некоторое время в такой системе вновь устанавливается равновесие, но уже при другом соотношении равновесных концентраций всех веществ;  ˗ состояние системы не зависит от того, с какой стороны она подходит к равновесию (со стороны прямой или обратной реакции); ˗ при снятии внешнего воздействия система вновь возвращается в исходное состояние. В изобарно-изотермических условиях (P; T=const) при равновесии изменение энергии Гиббса системы равно нулю (DG=0). Рассмотрим условную обратимую реакцию aA+bB⇄ cC+dD.
Закондействующих масс для нее запишется в виде:
где КС – константа равновесия; [A], [B], [C], [D] – равновесные концентрации веществ, моль/л; a, b, c, d – стехиометрические коэффициенты в уравнении реакции. Константа равновесия зависит от температуры и природы веществ, но не зависит от их концентраций Чем больше величина константы равновесия, тем в большей степени равновесие смещено в сторону образования продуктов реакции. Таким образом, константа равновесия характеризует глубину протекания процесса к моменту равновесия. Для реакций с участием газов константу равновесия (Кр)можно выразить и через парциальные давления газообразных веществ. Если газы не сильно отличаются по свойствам от идеальных, то между константой, выраженной через парциальные давления (Кр), и константой, выраженной через концентрации (Кс), существует связь: Kp=Kc×(RT)Dn, (6.2) где Dn– изменение числа моль газообразных веществ в ходе реакции в соответствии с ее стехиометрией. Константа равновесия при температуре Т связана с изменением стандартной энергии Гиббса реакции DG0 при той же температуре соотношением DG0= - RT×lnK, (6.3) где К – термодинамическая константа равновесия, безразмерная величина, выраженная через относительные парциальные давления.
где Р0 – стандартное атмосферное давление. В гетерогенных реакциях концентрация конденсированной фазы практически постоянна, она в неявной форме входит в константу равновесия. В выражение для константы равновесия концентрации конденсированной фазы не включаются. При изменении внешних условий равновесие смещается потому, что эти изменения по-разному влияют на скорости прямой и обратной реакций. Равновесие смещается в сторону той реакции, скорость которой становится больше. На равновесие влияет изменение температуры, концентрации веществ, давления в системе (если реакция идет с изменением числа моль газообразных веществ). Введение катализатора не смещает равновесие, так как он в равной мере изменяет скорость как прямой, так и обратной реакции. Катализатор лишь сокращает время достижения системой состояния равновесия. В общем случае направление смещения равновесия определяется принципом Ле Шателье: если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие сместится в том направлении, которое ослабляет это воздействие.
6.2 Методика проведения опыта
6.2.1 Опыт№1. Смещение химического равновесия при изменении концентрации веществ В небольшом стакане смешайте по 2мл разбавленных растворов FeCl3 и NH4CNS. Разбавьте полученный раствор дистиллированной водой так, чтобы он был светло-красным. В этом случае легко заметить как усиление, так и ослабление интенсивности окраски. Красный цвет раствора обусловлен роданидом железа (III), а точнее комплексным анионом [Fe(CNS)6]3-,который образуется в результате обратимой реакции: FeCl3+6 NH4CNS⇄ (NH4)3[Fe(CNS)6]+3 NH4Cl Fe3++6 (CNS)- ⇄ [Fe(CNS)6]3-. Раствор из стаканчика разлейте поровну в 4 пробирки. Одну из пробирок используйте в качестве контрольной. Во вторую пробирку добавьте 2 – 3 капли концентрированного раствора FeCl3, в третью – немного кристаллического NH4Cl, в четвертую добавьте 2 – 3 капли насыщенного раствора NH4CNS. Встряхните содержимое пробирок. Сравните окраску раствора в трех пробирках с контрольной пробиркой. По изменению интенсивности окраски можно судить о направлении смещения химического равновесия. Заполните таблицу 6.1.
Таблица 6.1 – Результаты опыта
Запишите выражение для константы равновесия данной реакции и на его основе, а также на основе принципа Ле Шателье объясните наблюдаемые явления.
6.2.2 Опыт №2. Влияние изменения температуры на смещение химического равновесия (опыт демонстрируется преподавателем) Оксид азота (IV) способен димеризоваться. В результате обратимой реакции 2NO2 ⇄ N2O4+54,39 кДж устанавливается химическое равновесие. Так как NO2 – газ темно-бурого цвета, а N2O4 – бледно-желтый, почти бесцветный газ, то по изменению окраски газовой смеси можно судить о концентрации ее компонентов, то есть о смещении равновесия в сторону прямой или обратной реакции. U-образную трубку заполняют оксидом азота (IV), который получают по реакции взаимодействия меди с концентрированной азотной кислотой. Для этого в колбочку кладут немного медных стружек и приливают к ним 5 – 10 мл концентрированной азотной кислоты. Затем закрывают колбу газоотводной трубкой, и опускают ее конец в U-образную трубку. Все операции осуществляются под тягой. После того, как U-образная трубка наполнится коричневым газом, ее концы плотно закрывают резиновыми пробками. Одно колено трубки помещается в стакан с горячей водой, другой – в воду со льдом или снегом. Наблюдается изменение окраски в обоих коленах. В каком направлении происходит смещение равновесия данной реакции при нагревании и охлаждении? Заполните таблицу 6.2.
Таблица 6.2 – Результаты опыта
Дайте объяснение наблюдаемым явлениям, исходя из принципа
6.3 Примеры решения задач
Пример 1 |
|||||||||||||||||||
|
Последнее изменение этой страницы: 2018-05-29; просмотров: 322. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |

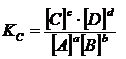 , (6.1)
, (6.1)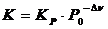 , (6.4)
, (6.4) раствор FeCl3
кристаллический NH4Cl
раствор NH4CNS
раствор FeCl3
кристаллический NH4Cl
раствор NH4CNS