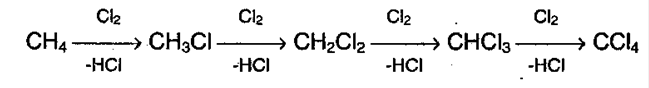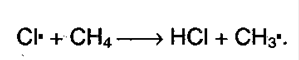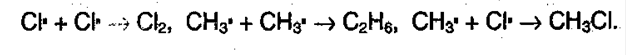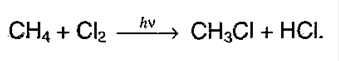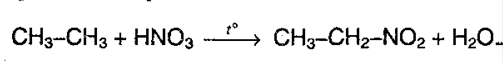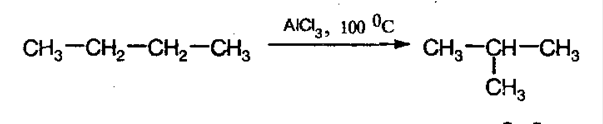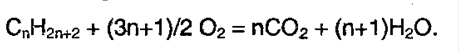Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Химические свойства алкановВ молекулах предельных углеводородов все атомы углерода находятся в состоянии sp3- гибридизации атомных орбиталей. Каждый атом углерода затрачивает на соединение с любым соседним атомом углерода не более одной валентности, причем все свободные (не затраченные на соединение с атомами углерода) его валентности насыщены водородом. Поэтому они не вступают в реакции присоединения. При обычных условиях алканы химически инертны, они не взаимодействуют с концентрированными серной и азотной кислотами, щелочами, перманганатом калия. Русский химик М.И. Коновалов назвал алканы «химическими мертвецами». Устойчивость объясняется прочностью связей и их неполярностью. Предельные углеводороды не склонны к реакциях разрыва связи (реакция присоединения), для них свойственно замещение. 1. Галогенирование алканов. Под воздействием кванта света начинается радикальное замещение (хлорирование) алкана. Общая схема:
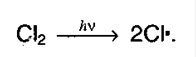
Реакция идет по цепному механизму, в которой различают: а) Инициирование цепи:
б) Рост цепи:
в) Обрыв цепи:
Суммарно можно представить в виде:
2. Нитрование(реакция М.И.Коновалова)алканов. Реакция протекает при 140 °С при действии 12-14% азотной кислоты:
Легче всего реакция протекает с третитичным атомом углерода, чем с первичным и вторичным. 3. Изомеризация алканов. При конкретных условиях алканы нормального строения могут превращаться в разветвленные:
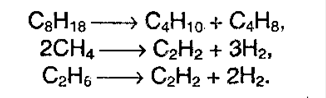
4. Крекинг алканов. При действии высоких температур и катализаторов высшие алканы могут рвать свои связи, образуя алкены и алканы более низшие:
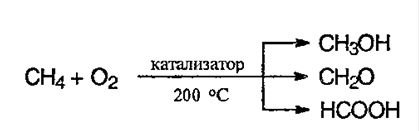
5. Окисление алканов. В различных условиях и при разных катализаторах окисление алкана может привести к образованию спирта, альдегида (кетона) и уксусной кислоты. В условиях полного окисления реакция протекает до конца – до образования воды и углекислого газа: 
Этиленовые углеводороды, алкены Общие сведения, номенклатура этиленовых углеводородов Алкены – ненасыщенные углеводороды, молекулы которых содержат одну двойную связь. Общая формула предельных углеводородов CnH2n.Простейший представитель ряда - этилен СH2=CH2. Согласно система-тической номенклатуре названия этиленовых углеводородов производят из названий соответствующих алканов с заменой суффикса -ан на –ен. Алкены простого строения называют заменяя суффикс -ан на -илен. Алкены применяются в качестве исходных продуктов в производстве полимерных материалов (пластмасс, каучуков, пленок) и других органических веществ. Таблица 5. Гомологический ряд этиленовых углеводородов
Углеводородные радикалы, образованные от алкенов: -CH = CH2 – винил и –СН2-СН = СН2 – аллил. Изомерия алкенов Для алкенов, начиная с бутена, характерно несколько видов изомерии: 1) изомерия углеродного скелета: CH2 = CH-CH2-CH3 (бутен-1) СН2-С(СН3)-СН3 (2-метилпропен-1) 2) изомерия положения двойной связи: CH2 = CH-CH2-CH3 (бутен-1) CH3-CH = CH-CH3 (бутен-2)
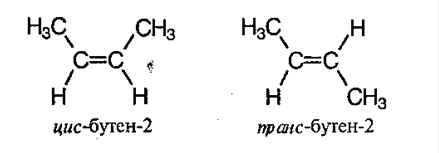
3) пространственная изомерия:
|
||||||||||||||||||
|
Последнее изменение этой страницы: 2018-05-27; просмотров: 377. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |