
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
ПРЕДЕЛЬНЫЕ И НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
Цель работы: ознакомление с предельными и непредельными углеводородами; особенностями строения и химических свойств алканов, алкенов и алкинов и их производных; проведение химических реакций для подтверждения строения и свойств изучаемых соединений.
ОСНОВНЫЕ ТЕОРЕТИЧЕСКИЕ СВЕДЕНИЯ
Предельные углеводороды, алканы Общие сведения, номенклатура предельных углеводородов Общая формула предельных углеводородов - Таблица 4. Гомологический ряд алканов.
Физические свойства алканов При обычных условиях С1-С4 – газы, С5-С17 – жидкости, начиная с С18 – твердые вещества. Алканы практически нерастворимы в воде, но, хорошо растворимы в неполярных растворителях, например, в бензоле. Так, метан СН4 (болотный, рудничий газ) – газ без цвета и запаха, хорошо растворимый в этаноле, эфире, углеводородах, но плохо растворимый в воде. Метан используют в качестве высококалорийного топлива в составе природного газа, в качестве сырья для производства водорода, ацетилена, хлороформа и других органических веществ в промышленных масштабах.  Пропан С3Н8 и бутан С4Н10 – газы, применяемые в быту, в качестве балонных газов, за счет легкой сжижаемости. Пропан используется в качестве автомобильного топлива, поскольку является более экологически чистым, чем бензин. Бутан – сырье для получения 1,3 –бутадиена, использующегося в производстве синтетического каучука. Получение алканов Алканы получают из природных источников – природного газа (80-90% — метан, 2-3% — этан и другие предельные углеводороды), угля, торфа, древесины, нефти и горного воска. Выделяют лабораторные и промышленные способы получения алканов. В промышленности алканы получают из битумного угля: nC + (n+1)H2 = CnH2n+2
или по реакции Фишера-Тропша : nCO + (2n+1)H2 = CnH2n+2 + H2O
К лабораторным способам получения алканов относят: 1. Гидрирование непредельных углеводородов при нагревании и в присутствии катализаторов (Ni, Pt, Pd): R1-C≡C-R2 (алкин) → R1-CH = CH-R2 (алкен) → → R1-CH2 – CH2 -R2 (алкан) 2. Взаимодействие воды с металлоорганическими соединениями: R-Cl + Mg → R-Mg-Cl + H2O → R-H (алкан) + Mg(OH)Cl 3. Электролиз карбоновых кислот: CH3COONa ↔ CH3COO— + Na+ 2CH3COO— → 2CO2↑ + C2H6 (этан) 4. Реакция декарбоксилирования: CH3COONa + NaOH → CH4 + Na2CO3 5. Реакция Вюрца: R1-Cl +2Na +Cl-R2 →2NaCl + R1-R2 и многие другие способы. |
||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-05-27; просмотров: 343. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
|||||||||||||||||||||||||||||||||||||||||||||||||
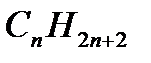 .Первые четыре вещества этого ряда имеют исторически сложившиеся названия. Названия углеводородов, начиная с пентана, образованы от греческих названий чисел. Для наименования предельных углеводородов принят суффикс –ан. Предельные углеводороды образуют гомологический ряд.
.Первые четыре вещества этого ряда имеют исторически сложившиеся названия. Названия углеводородов, начиная с пентана, образованы от греческих названий чисел. Для наименования предельных углеводородов принят суффикс –ан. Предельные углеводороды образуют гомологический ряд.