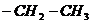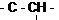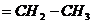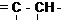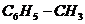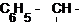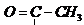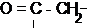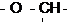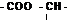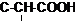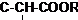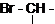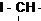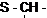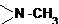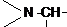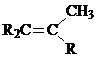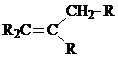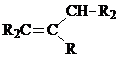Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
МАГНИТНОЕ ЭКРАНИРОВАНИЕ И ХИМИЧЕСКИЙ СДВИГЯдра водорода в органических молекулах окружены электронами. Вращение электронов создает свое поле, которое накладывается на внешнее поле, действующее на ядро. Иными словами, электроны заслоняют (экранируют) ядро от внешнего магнитного поля, поэтому напряженность поля в непосредственной близости к ядру отличается от напряженности внешнего магнитного поля. В результате изменения магнитного экранирования изменяется частота вращающегося поля, при которой наблюдается явление резонанса. Это изменение называется химическим сдвигом. Магнитное экранирование и, следовательно, химический сдвиг определяются положением данного протона в молекуле. Для эквивалентных протонов значение химического сдвига одинаково, и они дают один резонансный сигнал. Различающиеся окружением в молекуле протоны обладают различными химическими сдвигами и дают раздельные сигналы, что позволяет определять положение протона в молекуле. Положение резонансного сигнала зависит от напряженности постоянного внешнего поля (Н0), так как эта напряженность определяет силу, ориентирующую ось вращения протона. для выражения химических сдвигов необходима величина, не зависящая от Н0. За международный стандарт принято положение резонансного сигнала тетраметилсилана (СН3)4Si (ТМС). Вводимый в раствор вещества эталон должен обладать низкой реакционной способностью, хорошей растворимостью и давать один четкий сигнал в спектре. Кроме того, преимуществом ТМС является положение резонансного сигнала в более сильном поле, чем у подавляющего большинства органических веществ, а также большое количество протонов на единицу массы, что позволяет использовать эталон в минимальных количествах.  Пусть Нэ - напряженность поля, при которой наблюдается резонанс эталона; Н - напряженность поля, при которой наблюдается резонанс данного протона, а Н0 напряженность основного внешнего поля; отношение (Нэ – Н) / Н0 и будет безразмерной величиной, не зависящей от напряженности внешнего поля и характеризующей данный тип протона. Эта величина имеет порядок 10-6, поэтому для значений химического сдвига используют единицы δ, измеряемые в миллионных долях (м.д.):
Измерение напряженности поля значительно более сложно и менее точно, чем измерение частоты. В то же время для каждого данного типа протона резонансная частота линейно зависит от напряженности (h - постоянная Планка):
Поэтому для выражения химических сдвигов используется величина
где ν0 - рабочая частота; ν - резонансная частота данного протона; νЭ Непосредственные измерения дают величину ν – νЭ в единицах частоты (герц, Гц). Для перевода этой величины в шкалу δ ее необходимо разделить на основную рабочую частоту прибора (в мегагерц, МГц) и умножить на 106. Так, изменение величины δ на единицу соответствует изменению магнитного экранирования на 10-6 от частоты внешнего поля; например, для спектрометра с рабочей частотой 60 МГц 1 м. д. = 60 Гц. Получаемая шкала спектра ПМР имеет вид, представленный на рисунке 2.1.
Рисунок 2.1 – Спектр ПМР уксусной кислоты.
Нулевая отметка соответствует резонансному сигналу ТМС. Увеличение химического сдвига соответствует переходу в область более слабого поля, т. е. уменьшению степени магнитного экранирования данного протона. Важное значение имеет также интенсивность сигналов, так как поглощение энергии при данной частоте пропорционально числу протонов, для которых при этой частоте наблюдается явление резонанса. Это позволяет установить, сколько протонов образуют каждый сигнал. Иногда для измерения химических сдвигов в иностранной литературе применяется шкала τ, где τ = 10 - δ, т. е. положение резонансного сигнала от протонов ТМС принято за 10. В этой шкале увеличение значений химических сдвигов происходит одновременно с усилением поля.
ПОЛУЧЕНИЕ СПЕКТРОВ ПМР В связи с тем, что спектроскопия ПМР оперирует частотами радиоволн, соответствующие приборы часто называют радиоспектрометрами. Для получения спектра ПМР достаточно высокого разрешения используются в основном жидкие маловязкие образцы. Вещество помещают в виде раствора в тонкую (диаметром 5 мм) цилиндрическую ампулу длиной ≈150 мм. Ампула заполняется на 20 - 30 мм, для чего требуется около 0,4 м раствора. Концентрация этого раствора обычно составляет 0,2 моль/л, или 5—20 %, т. е. для приготовления пробы требуется 5 - 10 мг вещества. В специальных условиях спектр ПМР может быть получен для образца около 1 мг. Применяемый растворитель в идеальном случае не должен содержать собственных протонов (ССl4 и дейтерированные растворители: D2O, CDCl3, C6D6, CD3COCD3 и т. д.). В ампулу вводится также небольшое количество (≈1%) ТМС в качестве внутреннего эталона. Ампула с образцом помещается в мощное постоянное магнитное поле; напряженность поля в зависимости от рабочей частоты составляет 14—117,4 кГс (килогаусс). К однородности этого поля предъявляются очень высокие требования, так как ею в основном определяется качество получаемых спектров. Ампула в приборе вращается, чтобы исключить возможность проявления неоднородности образца. Очень важно отсутствие в образце нерастворимых частиц, которые могут вызвать местное изменение поля. В перпендикулярном направлении к основному прикладывается вращающееся магнитное поле, имеющее постоянную частоту (на пример, 40, 60, 100 или 360 МГц или более), и накладывается дополнительное вращающееся поле изменяющейся частоты (например, 0 -600 Гц для рабочей частоты 60 МГц). Поглощение энергии при данной частоте регистрируется специальным датчиком, преобразующим радиочастотный сигнал в электрический импульс, записываемый потенциометром. Время регистрации спектра составляет около 1 мин. Спектр представляет собой зависимость интенсивности поглощения энергии от величины δ, отражающей изменение частоты вращающегося поля. Обычно спектр выглядит как набор узких резонансных сигналов, соответствующих отдельным типам протонов. Для определения интенсивности (точнее, площади) сигналов современные приборы снабжены устройством для электронного интегрирования спектров, т. е. для записи интегральной кривой, преобразующей площади пиков в линейные отрезки. Легко измеряемое соотношение длин этих отрезков дает соотношение числа протонов, которым соответствуют отдельные сигналы. Например, в спектре ПМР уксусной кислоты (см. рис. 4-1) соотношение длин отрезков, соответствующих площади сигналов при δ 2,0 и 11,5 м.д., составляет 3 : 1, что указывает на число атомов водорода в уксусной кислоте (три эквивалентных протона метильной группы и один протон карбоксильной группы, сильно различающиеся по химическому сдвигу). Таким образом, спектр ПМР позволяет определить количество различающихся типов протонов и число протонов каждого данного типа. Пример 1. Соединение С5Н12 содержит в спектре ПМР единственный сигнал δ 0,82 м. д. Определите строение вещества. Решение. Из трех изомеров пентана СН3СН2СН2СН2СН3 (СН3)2СНСН2СН3 (СН3)4С н-пентан содержит три типа протонов с соотношением 6 : 4 : 2; 2-метилбутан – 4 типа (6 : 3 : 2: 1) и 2,2-диметилпропан – один тип протона; следовательно, соединение является 2,2-диметилпропаном. Пример 2. Соединение С6Н12 имеет в спектре ПМР один сигнал δ 1,42 м. д. Установите строение вещества. Решение. Согласно брутто-формуле, вещество содержит одну двойную связь или цикл. Единственным изомером, в котором все протоны эквивалентны (см. ниже), является циклогексан. Пример 3. Сколько сигналов и с каким соотношением интенсивностей содержит спектр ПМР 4-метилпентанон-2-ола-4 (СН3)2С(ОН)СН2СОСН3 Решение. Вещество содержит 4 типа неэквивалентных протонов в соотношении 6 : 1: 2 : 3; спектр ПМР (δ, м. д.): 1,2 (6Н, СН3); 2,15 (3Н, СН3СО); 2,6 (2Н, СН2); 3,95 (1Н, ОН). Возможность определения сравнительной интенсивности не скольких сигналов делает метод пригодным для количественного анализа. По точности (±5 %) он уступает УФ-спектроскопии, но превосходит ее простотой определения относительных концентраций веществ (путем сравнения длин соответствующих отрезков). В связи с тем, что современные радиоспектрометры имеют систему термостатирования ампул с образцом, значительным удобством метода ПМР является возможность проведения кинетических исследований непосредственно в ампуле прибора с количеством вещества всего 5—10 мг.
ШКАЛА ХИМИЧЕСКИХ СДВИГОВ На магнитное экранирование протона влияет множество факторов, в связи с чем зависимость между положением ядра в молекуле и соответствующим химическим сдвигом носит эмпирический характер. Основным из таких факторов является электронная плотность вокруг данного протона. Чем выше эта плотность, тем больше ее влияние на внешнее поле и, следовательно, тем в более сильном поле проявится резонансный сигнал. Влияние этого фактора соответствует тому, что протон, обладающий более кислыми свойствами (с меньшей плотностью электронной оболочки) резонирует в более слабом поле. На электронную плотность вблизи ядра существенно влияет индукционный эффект заместителя и присутствие соседних непредельных группировок, так как в последнем случае благодаря эффекту сопряжения электроны связи С—Н смешаются на соседнюю связь С—С. Изменения химических сдвигов групп СН3-, -СН2- и Таблица 2.1
Химические сдвиги группировок СН3—, — СН2 — и
Примечания. R-алкильная группа. По свободным связям (например, в группе — О—СН2 —) присоединены нормальные углеводородные радикалы.
Отметим, что химический сдвиг от протонов при двойной связи, ароматического ядра и в формильной группе достаточно характеристичен, и соответствующие сигналы относительно легко могут быть определены в спектре. Химические сдвиги от протонов при изолированных двойных связях и при сопряженной диеновой системе не имеют характеристических различий. Для протонов ароматического ядра существует определенная зависимость между химическим сдвигом и характером, а также взаимным расположением заместителей. Протоны незамещенного бензола имеют резонансный сигнал при δ 7,23 м. д. Если заместитель — сильный акцептор электронов (например, группы — NO2, — COOH) сигналы от протонов ядра смещаются в область слабого поля на 0—1 м. д. Если заместитель имеет неподеленную пару электронов (группы — ОН, —NH2, —NНR, —NR2), то сдвиг сигнала происходит в область сильного поля на 0,4—1,0 м. д. Заместители, обладающие положительным индукционным эффектом, значительно меньше влияют на положение резонансного сигнала. Химический сдвиг от протона в ароматическом ядре несколько изменяется также в зависимости от расположения этого протона относительно заместителя: наиболее сильно влияет заместитель в о-положении, меньше—в n-положении и еще меньше — в м-положении. Иногда, например, если заместитель — алкильная группа, химический сдвиг от протонов ядра не зависит от их положения, и они проявляются одним резонансным сигналом. Полициклические ароматические структуры дают, как правило, сложный сигнал в области δ 7,0—9,0 м. д. В основных гетероциклических ароматических системах химический сдвиг протонов составляет δ 6,9—8,5 м. д., т. е. попадает в ту же область, что у производных бензола. Однако в гетероциклах различие в положении резонансных сигналов в а- и β-положениях (а в пиридине и в γ-положении) к гетероатому довольно велико, причем α-протоны резонируют в самом слабом поле. Для групп ОН в спиртах и NH2 в аминах и амидах положение сигнала протона в спектрах ПМР нехарактеристично, поскольку оно в значительной степени зависит от степени участия группы в водородной связи. Однако определить, что сигнал принадлежит именно этим группам, экспериментально относительно легко, так как его положение зависит от концентрации и температуры, причем при разведении сигнал смещается в область сильного поля. Кроме того, такой сигнал исчезает при растворении в D2O за счет водородного обмена. Положение сигнала от протона группы СООН в карбоновых кислотах (δ 10—13 м.д.) более постоянно и меньше изменяется даже при сильном разведении достаточно характеристично. Если на магнитное экранирование данного протона действуют одновременно две группировки, вызывающие смещение химического сдвига сигнала в область слабого поля, то это смещение будет, соответственно, еще больше. Общая шкала химических сдвигов представлена в таблице 2.2. Таблица 2.2 Химические сдвиги протонов, м.д. (в шкале δ)
Примечания а) Циклогексан; б) С6Н5 – фенил; в) г)
Таким образом, по величине химического сдвига может быть определено положение протона в органической молекуле. Однако сигналы от протонов, незначительно отличающиеся по химическому сдвигу, могут перекрываться полностью или частично. Так, незначительно различающиеся по положению метиленовые группы в ациклических цепях или циклических системах часто сливаются в один широкий сложный сигнал.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 490. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

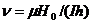
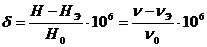
 - резонансная частота протонов эталона.
- резонансная частота протонов эталона.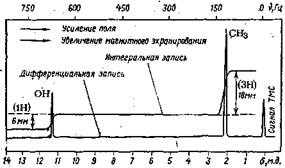
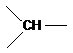 под влиянием соседних группировок представлены в таблице 2.1. Относительно легко различаются атомы водорода, находящиеся в α-положении к двойной связи (δ 1,7 - 2,1 м. д.), ароматическому ядру или карбонильной группе (δ 2,1 - 2,6 м. д.), и атомы водорода при углеродном атоме, содержащем в качестве заместителя атом галогена, кислорода или серы (δ 3,3 - 4,2 м. д.). Еще более сильная разница в магнитном экранировании протона наблюдается, если он присоединен к углеродному атому, участвующему в образовании кратной связи (δ, м. д.): 4,5—7,0 (=СН); 2,3—2,6 (≡СН); 6,5—8,0 (при ароматическом ядре); 8,5—11,0 [С(О)С]. В данном случае помимо перечисленных выше эффектов на магнитное экранирование протона существенное влияние оказывают кольцевые токи электронов, создаваемые непредельными группировками, особенно ароматической системой, тройной связью и карбонильной группой. Такие токи могут как усиливать прилагаемое поле, деэкранируя ядро (как в случае ароматических структур), так и уменьшать поле, как в случае протона при тройной связи.
под влиянием соседних группировок представлены в таблице 2.1. Относительно легко различаются атомы водорода, находящиеся в α-положении к двойной связи (δ 1,7 - 2,1 м. д.), ароматическому ядру или карбонильной группе (δ 2,1 - 2,6 м. д.), и атомы водорода при углеродном атоме, содержащем в качестве заместителя атом галогена, кислорода или серы (δ 3,3 - 4,2 м. д.). Еще более сильная разница в магнитном экранировании протона наблюдается, если он присоединен к углеродному атому, участвующему в образовании кратной связи (δ, м. д.): 4,5—7,0 (=СН); 2,3—2,6 (≡СН); 6,5—8,0 (при ароматическом ядре); 8,5—11,0 [С(О)С]. В данном случае помимо перечисленных выше эффектов на магнитное экранирование протона существенное влияние оказывают кольцевые токи электронов, создаваемые непредельными группировками, особенно ароматической системой, тройной связью и карбонильной группой. Такие токи могут как усиливать прилагаемое поле, деэкранируя ядро (как в случае ароматических структур), так и уменьшать поле, как в случае протона при тройной связи.