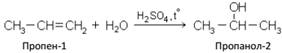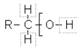Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
ГЛАВА 12. ГИДРОКСИЛЬНЫЕ СОЕДИНЕНИЯ И ИХ ПРОИЗВОДНЫЕПродукты замещения водорода в углеводородах гидроксильной группой (оксигруппой) называют спиртами. Общая формула спиртов Гидроксильные производные ароматических углеводородов называют ароматическими спиртами в том случае, если гидроксильная группа находится в боковой цепи, а фенолами – когда гидроксильная группа связана с углеродом ядра. По характеру углеводородного радикала алифатические спирты делятся на насыщенные и ненасыщенные. В зависимости от числа гидроксильных групп в молекуле различают: Одноатомные спирты
Двухатомные спирты
Трехатомные спирты
Углеродный атом способен удержать только одну гидроксильную группу; не может гидроксил состоять и при кратной углеродной связи, хотя из этих правил есть исключения.
ОДНОАТОМНЫЕ СПИРТЫ Изомерия Изомерия спиртов обусловлена строением радикала (изомерия углеродного скелета) и положением гидроксила в молекуле, в зависимости от того, с каким атомами углерода он связан (с первичным, вторичным или третичным) различают первичные, вторичные и третичные спирты:
Номенклатура Общая формула гомологического ряда предельных одноатомных спиртов:
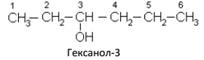
Названия спиртов образуют, добавляя окончание – ОЛ к названию углеводорода с самой длинной углеродной цепью, включающей гидроксильную группу. Нумерацию цепи начинают с того края, ближе к которому расположена гидроксильная группа. Кроме того, широко распространена радикально – функциональная номенклатура, по которой название спирта производится от соответствующего углеводородного радикала с обавлением слова «спирт», например:  Начиная с третьего представителя гомологического ряда – пропанола, у спиртов появляются изомеры:
В соответствии с международной номенклатурой цифрой после названия спирта обозначают, с каким по счету углеродным атомом связана гидроксильная группа, например:
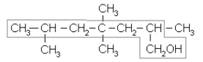
Правило составления названий алканолов с разветвленной цепью по Международной единой химической номенклатуре IUPAC (ИЮПАК) 1) Найти в молекуле самую длинную прямую углеродную цепь, связанную с гидроксильной группой:
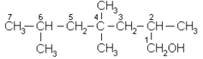
2) Пронумеровать атомы С в этой цепи так, чтобы атом С, связанный с группой –ОН, имел наименьший номер:
3) Назвать алкан, соответствующий самой длинной цепи, указав положение всех заместителей:
4) Обозначить гидроксильную группу суффиксом – ОЛ:
5) Цифрой указать положение группы – ОН:
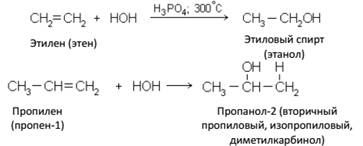
Получение спиртов 1. Гидратация алкенов Гидратация алкенов, протекает по правилу Марковникова:
Кроме прямой гидратации этилена (пропилена), существует также сернокислотная гидратация, протекающая в две стадии: – на первой стадии этилен поглощается серной кислотой:
– на второй стадии этилсерная кислота гидролизуется с образованием этилового спирта и серной кислоты:
При гидратации гомологов этилена в соответствии с правилом Марковникова образуются вторичные или третичные спирты:
2. Гидролиз галогеноалкинов При действии водного раствора NaOH атом галогена в галогеналкане замещается группой – OH:
Обратите внимание, что при действии спиртового раствора щелочи (KOH, NaOH) происходит отщепление галогеноводорода и образование алкена (см. 3 пункт “получение алкенов”):
3. Гидрирование альдегидов и кетонов Дегидрирование спиртов по своей химической сущности является окислением. Обратная реакция – гидрирование альдегидов и кетонов – является, таким образом, их восстановлением. В присутствии катализаторов (Ni, Pt, Pd, Co) альдегиды восстанавливаются до первичных спиртов, а кетоны – до вторичных спиртов:
4. Специфические способы получения метанола и этанола
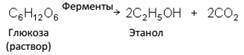
Этанол образуется при брожении (ферментации) углеводов – глюкозы или крахмала:
Физические свойства Рассмотрим электронное строение молекулы спирта:
Молекулы алканов представляют собой диполи. Они содержат полярные связи Полярность связи О – Н и наличие неподеленных пар электронов на атоме кислорода определяют физические свойства спиртов. В гомологическом ряду спиртов нет газообразных веществ.
Все алканолы легче воды, бесцветны, жидкие имеют резкий запах, твердые запаха не имеют. Метанол, этанол, пропанол неограниченно растворяются в воде; с увеличением числа углеродных атомов растворимость алканолов в воде уменьшается; высшие
Химические свойства Химические свойства алканов определяются особенностями их электронного строения:
наличием в их молекулах полярных связей О – Н, С – О, С – Н. Для алканолов характерны реакции, которые идут с расщеплением этих связей: реакции замещения, отщепления, окисления. I. Реакции замещения 1. Замещение атома водорода гидроксильной группы вследствие разрыва связи О – Н: А. Взаимодействие с активными металлами с образованием алкоголятов (алканолятов) металлов:
Эти реакции протекают только в безводной среде. В присутствии воды алкоголяты полностью гидролизуются:
Б. Взаимодействие с органическими и неорганическими кислотами с образованием сложных эфиров (реакция этерификации):
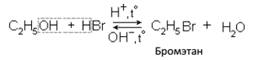
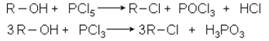
Реакции этерификации являются обратимыми реакциями. 2. Замещение гидроксильной группы вследствие разрыва связи С – О: А. Взаимодействие с галогеноводородами с образованием галогеналканов: Спирты можно превратить в галогенпроизводные действием и других реагентов, например хлоридов фосфора:
Б. Взаимодействие с аммиаком с образованием аминов. Реакции идут при пропускании смеси паров спирта с аммиаком при 300 °С над оксидом алюминия:
При избытке спирта алкильным радикалом могут замещаться 2 или 3 атома водорода в молекуле NH3:
II. Реакции отщепления 1. Дегидратация, т. е. отщепление воды Дегидратация спиртов может быть двух типов: межмолекулярная и внутримолекулярная. А. Межмолекулярная дегидратация спиртов с образованием простых эфиров R – O – R'. Эти реакции могут протекать с участием одного спирта или смеси двух и более спиртов:
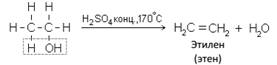
Б. Внутримолекулярная дегидратация спиртов с образованием алкенов. Протекает при более высокой температуре. В отличие от межмолекулярной дегидратации в процессе этих реакций происходит отщепление молекулы воды от одной молекулы спирта:
Дегидратация вторичных и третичных спиртов происходит по правилу Зайцева: «При образовании воды наиболее легко отщепляется водород от соседнего наименее гидрогенизированного атома углерода»
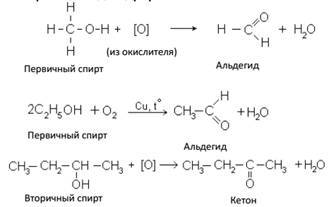
2. Дегидрирование (разрыв связей О – Н и С – Н): А. При дегидрировании первичных спиртов образуются альдегиды:
В организме человека этот процесс происходит под действием фермента алкогольдегидрогенозы. Б. При дегидрировании вторичных спиртов образуются кетоны: В. Третичные спирты не дегидрируются.
III. Реакция окисления 1. Горение (полное окисление) Спирты горят на воздухе с выделением большого количества тепла:
2. Неполное окисление под действием окислителей: кислорода воздуха в присутствии катализаторов (например, Cu), перманганата калия, дихромата калия и др. Реакции неполного окисления спиртов по своим результатам аналогичны реакциям дегидрирования:
Таким образом, реакции дегидрирования спиртов по своей химической сущности являются реакциями окисления. |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 476. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 .
.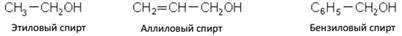

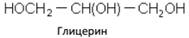


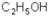 – этиловый спирт (этанол).
– этиловый спирт (этанол).