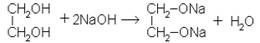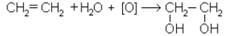Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
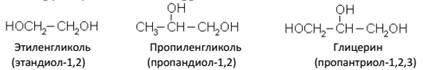
ПРЕДЕЛЬНЫЕ МНОГОАТОМНЫЕ СПИРТЫМногоатомные спирты содержат две и более спиртовые гидроксильные группы. Номенклатура. Физические свойства Двухатомные спирты называются гликолями или диолами, трехатомные – глицеринами или триолами. Положение гидроксильных групп указывают цифрами:
Отдельные представители (этиленгиколь, глицерин) Этиленгликоль (этандиол-1,2)Представитель предельных двухатомных спиртов – гликолей. Общая формула ряда гликолей Этиленгликоль (этандиол – 1,2) – сиропообразная жидкость сладкого вкуса, без запаха, ядовит. Хорошо смешивается с водой и спиртом, гигроскопичен. Его структурная формула:
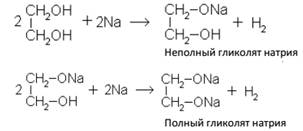
Химические свойства этиленгликоля в основном соответствуют свойствам одноатомных спиртов. Только реакции протекают как по одной, так и по двум гидроксильным группам. В реакции со щелочными металлами этиленгликоль образует неполный и полный гликоляты:
Этиленгликоль реагирует так же с едкими щелочами:
Этиленгликоль получают при окислении этилена раствором перманганата калия:
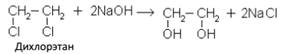
Его можно получить также при обработке дигалогенопроизводных углеводородов водным раствором щелочи:
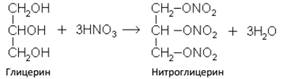
Водные и спиртовые растворы этиленгликоля применяются как не замерзающие при низких температурах растворы, заменяющие воду в радиаторах автомобильных и авиационных моторов в зимних условиях – антифризы. В последнее время применяется для получения лавсана – ценного синтетического волокна. Глицерин Простейший представитель трехатомных предельных спиртов – глицеринов. Это бесцветная, вязкая, гигроскопичная жидкость, сладкая на вкус. Смешивается с водой в любых отношениях. Хорошо растворяет многие вещества.  По химическим свойствам близок к этиленгликолю. Большое значение имеет реакция взаимодействия глицерина с азотной кислотой с образованием нитроглицерина:
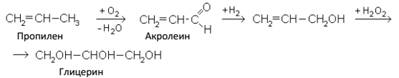
Нитроглицерин – исторически сложившееся название – неточно: у нитросоединений, нитрогруппа непосредственно присоединена к углеродному атому. Правильнее его было бы отнести к эфирам. Нитроглицерин – эфир глицерина и азотной кислоты – тринитрат глицерина. Нитроглицерин – тяжелая маслянистая жидкость, взрывчатое вещество (взрывается от легкого сотрясения и нагревания). Получают глицерин из жиров, а также синтетическим путем – из газов крекинга нефти (пропилена), т. е. из непищевого сырья.
Глицерин применяется для производства нитроглицерина, приготовления антифризов, в косметике (смягчает кожу), в кожевенной промышленности. Однопроцентный спиртовой раствор нитроглицерина используется как лекарство при сердечных заболеваниях (расширяет кровеносные сосуды).
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 385. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |

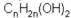 . Название гликоли получили вследствие сладкого вкуса многих представителей ряда (греч. “гликос”– сладкий).
. Название гликоли получили вследствие сладкого вкуса многих представителей ряда (греч. “гликос”– сладкий).