Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Фосфатидная кислота и фосфатидилглицеролы
Исходным соединением для всех фосфоацилглицеролов (т.е. фосфолипидов) служит, как уже упоминалось, фосфатидная кислота (Рис. 11.1). В свободном виде это соединение встречается в крайне незначительных количествах. С другой стороны, фосфатидная кислота является важнейшим промежуточным соединением в процессах биосинтеза триацилглицеролов и множества фосфолипидов. Крайне интересными фосфолипидами являются так называемые кардиолипины, которые представляют собой «двойные» фосфатидилглицеролы (Рис. 11.2). Главной особенностью кардиолипинов является то, что эти соединения локализуются, главным образом во внутренней мембране митохондрий.
Рисунок 11.1 – Структурная формула фосфатидной кислоты. Следует отметить, что второй углеродный атом (С2) глицерола в молекуле фосфатидной кислоты асимметричен и имеет L-конфигурацию
Кардиолипин – фосфолипид, входящий в состав митохондриальных мембран. Он образуется из двух молекул фосфатидной кислоты, которые соединены друг с другом «мостиком», представленным остатком глицерола.
Рисунок 11.2 – Кардиолипин («двойной» фосфоглицерид) содержится в больших количествах в мембранах митохондрий. Символами R с соответствующими индексами обозначены углеводородные цепи разных длинноцепочечных жирных кислот
Фосфатидилхолин (лецитин)
Лецитины, как и нейтральные жиры, содержат глицерол и остатки жирных кислот, но в их состав входят также фосфорная кислота и азотистое основание – холин. Лецитины широко представлены в клетках различных тканей, они выполняют как метаболические, так и структурные функции. Большинство данных фосфолипидов, как правило, содержит насыщенный ацильный радикал в положении С1 и ненасыщенный радикал в положении С2 глицерола.  При рН 7,0 остаток фосфорной кислоты в лецитинах, а также во всех других фосфолипидах несет отрицательный заряд. Кроме того, при рН, близких к нейтральным, азотистые основания в составе фосфолипидов (Рис. 11.3, 11.4, 11.6) могут нести один или несколько электрических зарядов. Таким образом, фосфолипиды содержат группировки двух разных типов, а именно полярные гидрофильные «головки» и неполярные гидрофобные хвосты. Такие соединения называют амфипатическими веществами.
Рисунок 11.3 – Структурная формула наиболее распространенного фосфолипида – фосфатидилхолина
Фосфатидилэтаноламин (кефалин)
Кефалины отличаются от лецитинов только тем, что у них азотистое основание холин представлено другим азотистым основанием – этаноламином.
Рисунок 11.4 – Структурная формула фосфатидилэтаноламина
Фосфатидилинозитол
В состав фосфатидилинозитола кроме глицерола, двух остатков жирных кислот и остатка фосфорной кислоты входит шестиатомный циклический спирт инозитол. Инозитол в этом соединении представлен одним из своих стереоизомеров – миоинозитолом. Кроме собственно фосфатидилинозитола, в клетках присутствует его фосфорилированная форма, представленная фосфатидилинозитол-4,5-дифосфатом, который также является важным компонентом клеточных мембран. Данное соединение обладает ярко выраженными физиологическими эффектами. В частности фосфатидилинозитол-4,5-дифосфат принимает участие в физиологической регуляции процессов секреции, осуществляемой с помощью секретогенных соединений, которые взаимодействуют с соответствующими рецепторами на базальной стороне экзокринных клеток. Например, в результате связывания ацетилхолина или холецистокинина со своими рецепторами на базальной стороне экзокринных клеток происходит активация внутриклеточной фосфатидилинозитол-специфичной фосфолипазы С, которая расщепляет фосфатидилинозитол-4,5-дифосфат с образованием инозитол-1,4,5-трифосфата и диацилглицерола. Последние, в свою очередь, инициируют, соответственно, высвобождение Ca2+ из эндоплазматического ретикулума в цитозол (инозитол-1,4,5-трифосфат) или активируют протеинкиназу С (диацилглицерол), что, в конечном итоге, обеспечивает выброс белковых продуктов из экзокринных клеток. Таким образом, оба этих соединения действуют как внутриклеточные вторичные мессенджеры передачи сигнала.
Рисунок 11.5 – Структурная формула фосфатидилинозитола
Фосфатидилсерин
В тканях находится также родственный кефалину фосфолипид, содержащий вместо этаноламина остаток аминокислоты серина.
Рисунок 11.6 – Структурная формула фосфатидилсерина
Сфингомиелины
Сфингомиелины в больших количествах встречаются в нервной ткани. При гидролизе сфингомиелинов образуются жирная кислота, фосфорная кислота, холин и сложный аминоспирт сфингозин.
В составе этих соединений глицерол отсутствует. При взаимодействии сфингозина с жирной кислотой (посредством амидной связи) образуется базовая структура сфингомиелинов, получившая название церамида. Церамид обнаруживается также в составе гликолипидов.
Рисунок 11.7 – Структурные формулы церамида и сфингомиелина
Благодаря присутствию фосфохолина в составе сфингомиелинов, последние часто относят к фосфолипидам. Однако, вследствие того, что гидрофобная часть этих молекул представлена церамидом, сфингомиелины более целесообразно считать сфинголипидами.
Сфинголипиды (гликосфинголипиды)
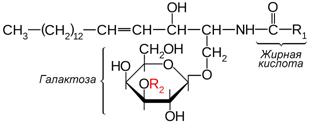
Гликолипиды широко представлены в тканях, особенно в нервной ткани, в частности в ткани мозга. Они локализованы преимущественно на наружной поверхности плазматических мембран, где их углеводные компоненты входят в число других углеводов клеточной поверхности. Главной формой гликолипидов в животных тканях являются гликосфинголипиды. Они построены из церамида и одного или нескольких остатков моносахаридов. На основании строения углеводного компонента гликолипидов их делят на цереброзиды и ганглиозиды. Двумя простейшими соединениями, относящимися к цереброзидам, являются галактоцереброзид (галактозилцерамид) и глюкоцереброзид (глюкозилцерамид). Как следует из названия этих гликолипидов, они включают церамид и только один углеводный остаток. Галактозилцерамид – главный гликосфинголипид мозга и других нервных тканей, в небольших количествах встречается также во многих других тканях. В его состав обычно входят различные С24-жирные кислоты. Галактозилцерамид также присутствует в виде сульфопроизводного сульфогалактозилцерамида, который в больших количествах содержится в миелине. Простые гликосфинголипиды, входящие в состав тканей, отличных от нервной, представлены главным образом глюкозилцерамидом, хотя в небольших количествах глюкозилцерамид обнаруживается также в нервной ткани.
Рисунок 11.8 – Структура галактоцереброзида (R2 = H) и его cульфатида – сульфогалактоцереброзида (R2 = SO2–4)
Более сложными гликосфинголипидами являются ганглиозиды, которые образуются из глюкозилцерамида посредством присоединения к нему дополнительных остатков моносахаридов. Ганглиозиды – это гликосфинголипиды, содержащие, кроме того, еще один или несколько остатков сиаловой кислоты. В тканях человека доминирующей сиаловой кислотой является нейраминовая кислота, которая часто ацетилирована (лабораторная работа № 10). Остатки N-ацетилнейраминовой кислоты встречаются также в олигосахаридных боковых цепях некоторых мембранных гликопротеидов. В сером веществе мозга ганглиозиды составляют около 6% мембранных липидов. Они обнаруживаются также, хотя и в меньших количествах, в мембранах клеток других (не нервных) тканей. Например, ганглиозид GМ1 является рецептором холерного токсина в эпителии кишечника человека. Ганглиозиды – важные компоненты расположенных на поверхности клеточных мембран специфических рецепторных участков. Так, они находятся в тех специфических участках нервных окончаний, где происходит связывание молекул нейромедиатора в процессе химической передачи импульса от одной нервной клетки к другой. Наиболее простым по строению ганглиозидом, встречающимся в нервной ткани, является ганглиозид GМ3 (аббревиатура GМ3 означает: G – ганглиозид, М – моносиаловое соединение, индекс 3 – порядковый номер фракции, элюирующейся при хроматографическом разделении ганглиозидов). Ганглиозид GМ3 состоит из церамида, одного остатка глюкозы, одного остатка галактозы и одного остатка нейраминовой кислоты. Структура более сложного ганглиозида GМ1, образующегося из GМ3, показана на Рис. 11.9 и на Рис. 10.2. (лабораторная работа №10).
Рисунок 11.9 – Структура ганглиозидов GМ3 и GМ1
Как видно из рисунка, ганглиозиды GМ1 и GМ3 содержат только по одному остатку N-ацетилнейраминовой кислоты. В то же время другие ганглиозиды могут содержать от одного до пяти остатков сиаловой кислоты: их называют, соответственно, моно-, ди-, трисиалоганглиозиды и т.д.
Амфипатические свойства липидов
Как известно триацилглицеролы и воска нерастворимы в воде, поскольку состоят преимущественно из гидрофобных (углеводородных) цепей. Однако жирные кислоты (в первую очередь их соли), фосфолипиды, сфинголипиды, желчные кислоты в виде солей и, в меньшей степени, холестерол содержат кроме гидрофобных «хвостов» полярные «гидрофильные» группы. Таким образом, одна часть их молекул гидрофобна (нерастворима в воде) а другая – гидрофильна (растворима в воде). Такие молекулы называют амфипатическими соединениями (Рис. 11. 10).
Рисунок 11.10 – Структура амфипатических (амфифильных) соединений фосфатидилхолина и сфингомиелина. В верхней части рисунка приводится схематическое изображение амфипатического липида, где волнистые линии обозначают два гидрофобных «хвоста», а шарик иллюстрирует гидрофильную «головку»
Представляет особый интерес поведение фосфолипидов и гликолипидов в водной среде. При смешивании амфипатических веществ с водой, их молекулы спонтанно организуются таким способом, который удовлетворяет одновременно двум противоположным свойствам разных частей молекул. Они организуются так, что их гидрофильные «головки» погружаются в воду, в то время как гидрофобные «хвосты» в контакт с водой не вступают, а контактируют только между собой, с воздухом или неполярными средами, например, маслом. Благодаря двойственной природе амфипатических соединений, в зависимости от среды они способны образовывать разнообразные надмолекулярные структуры, к которым относятся монослои, мицеллы, обращенные мицеллы, бислойные структуры, липосомы и др. При встряхивании в воде или водных растворах фосфолипиды и гликолипиды спонтанно формируют мицеллы, в которых углеводородные «хвосты» липидов спрятаны внутри структуры, а заряженные гидрофильные «головки» располагаются на поверхности частиц, взаимодействуя с водным окружением (Рис. 11.11). С другой стороны, в неполярных растворителях фосфолипиды образуют мицеллы, в которых гидрофобные хвосты направлены наружу, а гидрофильные головки вовнутрь (обращенные мицеллы).
Рисунок 11.11 – Фосфолипиды и гликолипиды способны в водной фазе спонтанно образовывать мицеллы. На рисунке приведено строение типичной мицеллы. Гидрофобные «хвосты» полярных липидов формируют внутри мицеллы неполярную область, тогда как заряженные «головки», расположенные на поверхности структуры, придают мицелле стабильность в водной среде. В неполярных растворителях у обращенных мицелл гидрофобные хвосты направлены наружу, а гидрофильные головки вовнутрь
Фосфолипиды способны также растекаться по поверхности водной фазы, образуя слой толщиной в одну молекулу – монослой. В таких системах углеводородные «хвосты» обращены к воздушной среде избегая, таким образом, контакта с водой, а гидрофильные «головки» погружены в полярную водную фазу (Рис. 11. 12). Соответственно на поверхности раздела фаз масло – воздух молекулы полярных липидов располагаются таким образом, чтобы полярные группы находились в воздушной среде, а неполярные гидрофобные группы – в масляной фазе.
Рисунок 11.12 – Фосфолипиды и гликолипиды способны образовывать монослои и бислои. При образовании бислойных структур гидрофобные «хвосты» полярных липидов формируют внутреннюю неполярную область, а заряженные «головки» расположенные на каждой стороне бислоя контактируют с водой и обеспечивают его стабилизацию в водных растворах
Возможен также способ организации полярных липидов, удовлетворяющий их амфипатическим свойствам, посредством образования бимолекулярного слоя, или иначе липидного бислоя. В действительности, в водной среде большинство фосфолипидов и гликолипидов образуют именно бислойные структуры, а не мицеллы. Такое предпочтительное образование структуры бислоев имеет огромное значение в биологии. Бислои, образованные полярными липидами, считают основой структуры биологических мембран. Действительно, размеры мицелл обычно невелики – менее 20 нм в диаметре. Бимолекулярные слои, напротив, достигают макроскопических размеров, вплоть до миллиметра (106 нм). Именно фосфолипиды и гликолипиды являются ключевыми компонентами биологических мембран потому, что они легко образуют бимолекулярные слои. В зависимости от природы содержащихся в них жирных кислот липидные бислои имеют толщину от 6 до 7 нм. Важным является и то, что эти бислои, несмотря на жидкое состояние, могут выполнять функцию барьеров проницаемости. В лабораторных условиях такие бислойные структуры несложно получить либо путем сильного встряхивания водных суспензий фосфолипидов, либо их обработкой ультразвуком; при этом образуются особые структуры – липосомы – замкнутые везикулы, окруженные непрерывным липидным бислоем. В настоящее время липосомы служат предметом интенсивных исследований, поскольку по своим свойствам они очень сходны с природными мембранами. Кроме того, липосомы находят применение в медицинской практике, особенно при использовании их в комбинации с тканеспецифичными антителами.
Липосомы могут служить переносчиками лекарств к определенным органам. Например, при введении в кровоток липосомы захватываются клетками ретикулоэндотелиальной системы, локализованными главным образом в костном мозге и селезенке. Указанное обстоятельство позволяет использовать липосомы для доставки специфических лекарственных средств в ретикулоэндотелиальную систему и таким образом направленно воздействовать именно на эту ткань. С этой целью липосомы «нагружают» раствором лекарственного препарата и затем вводят в кровь. В экспериментах на животных было показано, что использование липосом в качестве переносчиков лекарств значительно снижает токсичность препаратов и увеличивает их эффективность. При определенных условиях липосомы могут сливаться с плазматическими мембранами клеток. Это позволяет в экспериментальных условиях изменять липидный состав клеточных мембран и изучать значение таких изменений.
Теоретическая часть
Нуклеиновые кислоты
Нуклеиновые кислоты (ДНК и РНК) являются важнейшими информационными макромолекулами клетки, которые, с химической точки зрения, представляют собой полимеры, построенные из многих тысяч и даже миллионов нуклеотидов, соединенных между собой 3¢-5¢-фосфодиэфирными связями. В зависимости от вида нуклеиновой кислоты различают дезоксирибонуклеотиды (содержат 2¢-дезокси-D-рибозу и входят в состав ДНК) и рибонуклеотиды (содержат D-рибозу и входят в состав РНК). Кроме того, в зависимости от химической природы азотистых оснований (пуриновых или пиримидиновых), входящих в состав нуклеотидов их подразделяют на пуриновые и пиримидиновые нуклеотиды, соответственно. Следует иметь в виду, что биологическая роль нуклеотидов не ограничивается их участием в качестве мономеров в процессах биосинтеза ДНК и РНК. В частности, пуриновые рибонуклеотиды выполняют функции универсальных источников энергии (например, АТР и GTP), сигнальных молекул (сАМР, сGMP), они входят в состав важнейших коферментов (FAD, NAD+, NADP+) и служат переносчиками метильных групп (S-аденозилметионин); пиримидиновые нуклеотиды функционируют в качестве макроэргических интермедиатов в углеводном обмене (UDP-глюкоза, UDP-галактоза) и в синтезе липидов (CDP-ацилглицерол).
|
|||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 728. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
||||||||||||||||||||||||||||||||||||