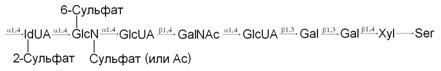Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Кератансульфат I и кератансульфат II
Кератансульфаты состоят из повторяющихся дисахаридных компонентов Gal–GlcNAc и содержат сульфаты в 6-м положении остатков GlcNAc и иногда – Gal.
Полисахарид в кератансульфате I присоединен к полипептидной цепи связью GlcNAc–Asn. Большие количества кератансульфата I присутствуют в роговице глаза. Кератансульфат II – протеогликан скелета связан с гиалуроновой кислотой рыхлой соединительной ткани. Его полисахаридные цепи присоединяются к полипептидной цепи с помощью связи GalNAc–Thr(Ser).
Гепарин
Гепарин представляет собой классический протеогликан, в котором несколько полисахаридных цепей связаны с общим белковым ядром. Он обнаруживается в гранулах тучных клеток и, следовательно, локализован внутриклеточно. Гепарин обладает и другими структурными и функциональными особенностями, и некоторые из них имеют значение для медицины. Характерные особенности структуры гепарина (и гепарансульфата) представлены на рисунке ниже.
В составе гепарина повторяющийся дисахаридный компонент состоит из глюкозамина (GlcN) и уроновой кислоты. Большинство аминогрупп остатков GlcN присутствует в N-сульфированной форме, но имеется и небольшое количество ацетилированных аминогрупп. GlcN содержит также С6-сульфатный эфир. Из общего количества остатков уроновой кислоты около 90% приходится на долю IdUA и лишь 10% составляет GlcUA.
Гепарансульфат
Гепарансульфат является компонентом поверхностей клеточных мембран, тем самым, представляя собой внеклеточный протеогликан. Полипептидный остов гепарансульфатного протеогликана содержит дополнительный аминокислотный компонент, отличный от такового в гепарине. В процессе модификации его полисахаридных цепей дезацетилирование остатков GlcNAc происходит слабее, и поэтому он содержит меньше N-сульфатов. Поскольку 5-эпимераза (как отмечалось выше при описании модификаций гепарина) использует в качестве субстрата N-сульфатные заместители, гепарансульфат отличается от гепарина меньшим количеством остатков IdUA и большим содержанием GlcUA. В соответствии с этим преобладающей уроновой кислотой в гепарансульфате является GlcUA, в то время как в гепарине – IdUA. 
Дерматансульфат
Дерматансульфат представляет собой протеогликан, широко распространенный в тканях животных. По структуре он сходен и с хондроитинсульфатом, и с гепарансульфатом.
Его отличие от хондроитинсульфата состоит в том, что вместо GlcUA, соединенной с GalNAc b1,3-связью, он содержит IdUA, соединенную с GalNAc a1,3-связью. Образование IdUA, как и в случае гепарина и гепарансульфата, происходит путем 5-эпимеризации GlcUA. Как и при образовании гепарина, реакция эпимеризации тесно сопряжена с сульфированием гексозамина. Таким образом, дерматансульфат содержит 2 вида повторяющихся дисахаридных единиц: IdUA–GalNAc и GlcUA–GalNAc.
Функции гликозамингликанов и протеогликанов Связывание гликозоаминогликанов с другими внеклеточными макромолекулами вносит значительный вклад в структурную организацию соединительнотканного матрикса. Гликозоаминогликаны могут взаимодействовать с внеклеточными макромолекулами, белками плазмы, компонентами клеточной поверхности и внутриклеточными макромолекулами. Связывание гликозаминогликанов носит обычно электростатический характер, обусловленный их выраженной полианионной природой, однако некоторые реакции связывания являются более специфичными. В целом гликозаминогликаны, содержащие IdUA, такие, как дерматансульфат и гепарансульфат, связывают белки с большим сродством, чем гликозаминогликаны, содержащие в качестве единственной уроновой кислоты GlcUA. Взаимодействие с внеклеточными макромолекулами. Все гликозамино-гликаны, за исключением тех, в которых отсутствуют сульфатные (гиалуронат) или карбоксильные группы (кератансульфаты), при нейтральных значениях рН электростатически связываются с коллагеном. Присутствие IdUA способствует более прочному связыванию, и протеогликаны взаимодействуют с коллагеном сильнее, чем соответствующие гликозаминогликаны. С каждым коллагеновым мономером связывается от 2 до 5 полисахаридных цепей. Все растворимые коллагены (I, II и III типов) связывают хондроитинсульфатные протеогликаны. Хондроитинсульфат и гепарансульфат специфически связываются с эластином. Как отмечалось выше хондроитинсульфатные и кератансульфатные цепи в составе соответствующих протеогликанов при посредстве связывающих белков образуют агрегаты с гиалуроновой кислотой. С одной молекулой гиалуроната может связываться до 100 протеогликановых молекул. Взаимодействие с белками плазмы крови. В состав поверхности стенки артериальных сосудов входят протеогликаны, содержащие гиалуронат, хондроитинсульфат, дерматансульфат и гепарансульфат. Из них с липопротеинами плазмы крови взаимодействует дерматансульфат. Кроме того, дерматансульфат, по-видимому, является главным гликозаминоглика-ном, синтезируемым гладкомышечными клетками артерий. Поскольку именно эти клетки пролиферируют при атеросклеротических поражениях артерий, дерматансульфат может играть значительную роль в образовании атеросклеротических бляшек. Хотя гепарин синтезируется и запасается в тучных клетках, он всегда тесно связан с кровеносными сосудами. В силу своего высокого отрицательного заряда (обусловленного остатками IdUA и сульфата) гепарин интенсивно взаимодействует с некоторыми компонентами плазмы. Он специфически связывает факторы свертывания крови IX и XI. Более важной для антикоагулянтной активности гепарина является его способность взаимодействовать с a2-гликопротеином плазмы, называемым антитромбином III. Стехиометрическое связывание с гепарином (1:1) значительно усиливает инактивирующее действие антитромбина III на сериновые протеазы, в частности на тромбин. Гепарансульфат, сходный с гепарином по структуре, также обладает способностью ускорять действие антитромбина III, но по эффекту значительно уступает гепарину. Гепарин может специфически связываться с липопротеинлипазой, присутствующей в стенках капилляров, и вызывать высвобождение этого фермента в кровоток (антилипидемическое действие гепарина). Сходным образом связывается с гепарином и поступает в кровоток печеночная липаза, но это связывание происходит с меньшим сродством, чем в случае липопротеинлипазы. Гликозаминогликаны и молекулы клеточной поверхности. Гепарин обладает способностью связываться с многими типами клеток, включая тромбоциты, клетки эндотелия артерий и гепатоциты. Хондроитинсульфат, дерматансульфат и гепарансульфат связываются с разными участками клеточной поверхности, например фибробластов. Именно в этих участках гликозаминогликаны и протеогликаны подвергаются деградации. Гиалуронат, по-видимому, участвует в процессах слипания клеток друг с другом, что играет столь важную роль в росте и развитии многоклеточных организмов. Некоторые протеогликаны, вероятно, служат рецепторами и переносчиками макромолекул, в том числе липопротеинов, липаз и антитромбина. Протеогликаны могут принимать участие в регуляции роста клеток, в межклеточных взаимодействиях и защите рецепторов клеточной поверхности. Гликозаминогликаны и внутриклеточные макромолекулы. Протеогликаны и их гликозаминогликановые компоненты кроме взаимодействия с ферментами, участвующими в их биосинтезе и деградации, оказывают влияние на синтез белка и внутриядерные функции. В частности, гепарин может действовать на структуру хроматина и активировать ДНК-полимеразу in vitro. В какой степени эти эффекты являются физиологическими, неясно. Гликозаминогликаны присутствуют в значительных количествах в ядрах различных типов клеток. Хондроитинсульфаты, дерматансульфаты и гепарин могут активировать или ингибировать кислые гидролазы лизосом. Эти ферменты способны формировать природные комплексы с гликозаминогликанами с образованием защищенных или неактивных форм. Многочисленные гранулы, служащие для запасания или секреции продуктов, такие, как базофильные гранулы тучных клеток, содержат сульфированные гликозаминогликаны. Гликозаминогликан-пептидные комплексы, присутствующие в этих гранулах, могут играть роль в высвобождении биогенных аминов.
теоретическая часть
Липиды
Липиды составляют вместе с белками и углеводами основную массу органического вещества живой клетки. В высокой концентрации липиды (особенно фосфолипиды) обнаруживаются в различных органах животных и человека: в головном и спинном мозге, крови, печени, сердце, почках и других органах. Эти соединения входят в состав всех структурных элементов клетки, в первую очередь клеточных (плазматических) мембран и мембран субклеточных частиц. С участием липидов протекают такие важнейшие биохимические процессы, как передача нервных импульсов, активный перенос через мембраны, транспорт жиров в плазме крови и многие ферментативные процессы, особенно те, которые связаны с транспортом электронов и системой окислительного фосфорилирования. Многообразие функций липидов в жизни клетки определяет ту важную роль, которую они выполняют в энергетических процессах, в защитных реакциях организма, его развитии и старении, в развитии различных патологических состояний и т.д. В структурном отношении липиды и многие жироподобные вещества (называемые иногда липоидами) представляют собой весьма гетерогенную группу органических соединений, которые, тем не менее, так или иначе связаны с длинноцепочечными карбоновыми (высшими жирными) кислотами. Наиболее общими свойствами липидов являются: во-первых, их нерастворимость в воде (хотя среди липидов имеются такие, которые способны образовывать в полярных растворителях относительно устойчивые эмульсии; во-вторых, их растворимость в неполярных растворителях – эфире, хлороформе, бензоле.
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 516. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |