
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Перевод формул концентраций
Свойства растворов зависят от соотношения между количествами их составных частей, то есть от концентрации, под которой понимают количество лекарственного средства, растворенного в определенном количестве растворителя.  В рецептах концентрацию растворов обозначают следующими способами:
1. Указывают концентрацию лекарственного вещества в процентах (которая показывает весовое количество растворенного вещества в граммах в 100 мл раствора). Rp.: Solutionis Kalii iodidi 2% 200 ml Da. Signa.
2. Указывают количества лекарственного вещества и растворителя. Rp.: Kalii iodidi 4,0 Aquae purificatae 200 ml Misce. Da. Signa.
3. Указывают количество лекарственного вещества и общий объем раствора, который достигается добавлением прописанного растворителя (обозначается с помощью лат. ad -- до). Rp.: Kalii iodidi 4,0 Aquae purificatae ad 200 ml Misce. Da. Da. Signa.
4. Указывают отношение количества прописанного лекарственного вещества к общему количеству получаемого раствора с помощью лат. ex -- из. Rp.: Solutionis Kalii iodidi ex 4,0 -- 200 ml Da. Signa.
Несмотря на разные способы прописывания растворов калия йодида, его объем равен 200 мл, количество лекарственного вещества составляет 4,0 г. 5. Указывают степень разведения лекарственного вещества, например, 1:1000, 1:5000, 1:10000 и объем этого раствора. Rp.: Solutionis Furacilini (1:5000) 200 ml Da. Signa.
Из всех приведенных способов чаще всего применяется способ обозначения концентрации раствора в процентах. Решение задач
1. Вычислите массовую долю 1 моль/л раствора хлороводородной кислоты, плотность которого 1,013г/мл.
Дано: Решение: См (HCI) = 1 моль/л См * Мм 1*36,46 ρ(HCI) = 1,013г/моль ω = -------------- = -------------- = 3,61% Мм (HCI) = 36,46 г/моль 10* ρ 10*1,013 ______________
ω(HCI) -? Ответ: ω(HCI) = 3,61%
2. Рассчитайте молярную концентрацию эквивалента раствора азотной кислоты, если титр этого раствора равен 0,006500 г/мл.
Дано: Решение: Т (HNO3) = 0,006500г/мл Мм (HNO3) = 63,05 г/моль 1000 * Т 1000* 0,006500 С1/z = ---------- = --------------------- = М1/z 63,05 ___________________ С1/z (HNO3) -? = 0,1030 моль/л
М1/z = Мм(HNO3) = 63,05 г/моль
Ответ: С1/z (HNO3) = 0,1030 моль/л
3. Рассчитайте процентную концентрацию раствора натрия хлорида с молярной концентрацией 0,15 моль/л. Мм (NaCI) = 58 г/моль.
Дано: Решение: См (NaCI) = 0,15 моль/л Мм* См 58*0,15 Мм (NaCI) = 58 г/моль ω = ------------ = ----------- = 0,87% ρ(NaCI) = 1 г/мл 10ρ 10*1 __________________ ω (NaCI) - ? Ответ: ω (NaCI) = 0,87%
4. Рассчитайте объем 49%-ной серной кислоты с ρ = 1,6 г/мл необходимый для приготовления 10 л раствора с молярной концентрацией эквивалента 1 моль/л. Мм (Н2SO4) = 98 г/моль.
Дано: Решение:
ω (Н2SO4конц.) = 49% m (Н2SO4) = C1/z * Mм * V = ρ (Н2SO4конц.) = 1,6 г/мл 1*49*10 = 490 г V (Н2SO4разб.) = 10 л 98 C1/z(Н2SO4разб.) = 1 моль/л Мм ((Н2SO4) = ------- = 49 г/моль Мм (Н2SO4) = 98 г/моль 2
V (Н2SO4конц.) - ? m * 100% 490*100 m (р – ра конц.) = -------------- = ----------- = 1000 г ω 49
m (р – ра конц.) 1000 V (Н2SO4конц.) = -------------------- = --------- = 625 мл ρ (Н2SO4конц.) 1,6
Ответ: V (Н2SO4конц.) = 625 мл
5. Определите титр, молярную концентрацию эквивалента и молярную концентрацию раствора калия перманганата, если в 200 мл раствора содержится 15,6 г калия перманганата. Мм (КМпО4) = 158 г/моль, z (КМпО4) = 5.
Дано: Решение: V (KMnO4) = 200 мл m 15,6 m (KMnO4) = 15,6 г Т = ---- = ------- = 0,07800 г/мл Мм (КМпО4) = 158 г/моль V 200 z (КМпО4) = 5
См - ? m (KMnO4) 15,6 С1/z - ? См = ------------------------ =------------- = 0,5 моль/л Т - ? Мм (КМпО4) * V 158 * 0,2 С1/z = См * z = 0,5*5 = 2,5 моль/л
Ответ: Т= 0,07800 г/мл См = 0,5 моль/л С1/z = 2,5 моль/л 6. Рассчитайте объем 96%-ной серной кислоты с ρ = 1,84 г/мл необходимый для приготовления 1 л раствора с молярной концентрацией эквивалента 0,25 моль/л. Мм (H2SO4) = 98г/моль.
Дано: Решение: ω конц = 96% m = C1\z* M1\z* Vразб ρ конц = 1,84 г/мл m = 0,25* 49 * 1 = 12,25 г V разб.= 1 л Мм 98 C1\z = 0,25 моль/л M1\z = ------- = ------- = 49 г/моль Мм (H2SO4) = 98г/моль 2 2
V конц -? m вещества ω = ---------------- * 100% m раствора
m вещества 12,25 m раствора = --------------- * 100% = ------------ * 100% = 12,76 г ω 96
m раствора 12,76 Vконц = -------------- = --------- = 6,9 мл ρ 1,84
Ответ: объем конц. H2SO4 равен 6,9 мл.
7. Какой объем 96%раствора серной кислоты с ρ = 1,84 г/мл необходимо взять для приготовления 1 л 0,5 моль/л раствора? Мм (H2SO4) = 98г/моль.
Дано: Решение: ω конц = 96% ρ конц = 1,84 г/мл V разб.= 1 л Мм 98 C1\z = 0,5 моль/л M1\z = ------- = ------- = 49 г/моль Мм (H2SO4) = 98г/моль 2 2
10 ρ конц ω конц 10*1,84*96 V конц -? С1\z Н2SO4 96% = ---------------------- = ------------------- = M1\z(H2SO4) 49
= 36 моль/л
Vразб *Cразб 1000 * 0,5 V конц. = ------------------------ = ----------------- = 13,8 мл Cконц 36 Ответ: конц. H2SO4) надо взять 13,8 мл для приготовления разбавленного раствора.
8. Рассчитайте массу навески натрия тетрабората, необходимую для приготовления 200 мл раствора с молярной концентрацией эквивалента 0,1 моль/л. Определите титр, молярную концентрацию эквивалента и поправочный коэффициент раствора, если для его приготовления была взята навеска натрия тетрабората массой 3,7995 г. Мм (Na2B4O7 • 10 H2O) = 381,4 г/моль.
Дано: Решение: С1/Z (буры) = 0,1 моль/л m теор. (буры) = С1/Z (буры) * М1\z * V(буры) V(буры) = 200 мл = 0,2 л m практ. (буры) = 3,7995 г Мм(бура) 381,4 Мм(Na2B4O7•10H2O)=381,4г/моль М1\z = -------- = -------- = 190,7 Z 2 m теор. (буры) = ? Т~0,1 моль/л буры = ? С1/Z~0,1 моль/л буры = ? m теор. (буры) = 0,1 * 190,7 * 0,2= 3,814 г К ~0,1 моль/л буры = ? m практ. (буры) 3,7995 Т~0,1 моль/л буры =---------------- = ------- = 0,01900г/мл V(бура) 200
m практ. 3,7995 K = --------- = ----------------= 0,9962 m теор. 3,814
С1/Z~ 0,1 = С1/Z 0,1 * Кп
С1/Z~ 0,1 = 0,1 * 0,9962 = 0,0996 моль/л
Ответ: m теор. (буры) = 3,814 г Т~0,1 моль/л буры = 0,01900г K =0,9962 С1/Z~ 0,1 = 0,0996 моль/л 9. Проведите стандартизацию рабочего раствора хлороводородной кислоты - определите титр, молярную концентрацию эквивалента и поправочный коэффициент ~0,1 моль/л раствора хлороводородной кислоты, если на титрование 10 мл раствора тетрабората натрия с молярной концентрацией эквивалента ~0,1 моль/л и поправочным коэффициентом равным 1,0120 ушло 9,8 мл раствора хлороводородной кислоты. М.м (НС1)= 36,46 г/моль.
Дано: V~0,1моль/л буры = 10 мл K буры = 1,0120 V (НС1) = 9,8 мл М.м (НС1) = 36,46 г/моль
С1/Z~0,1моль/л НС1 = ? Т~0,1моль/л НС1 = ? КНС1 = ?
НС1 – это стандартизируемый рабочий раствор (исследуемый раствор). Бура – это исходное вещество метода ацидиметрии, по которому устанавливают концентрацию кислоты. Метод количественного определения – метод ацидиметрии (так как титрование проводят кислотой). Способ прямого титрования. В основе метода лежит реакция: 2 HCl + Na2B4O7 + 5 H2O = 2 NaCl + 4 H3BO3
Вещества взаимодействуют по закону эквивалентов: С1/Z ~0,1моль/л (НС1) • V~0,1моль/л (НС1) = С1/Z~0,1моль/л буры • V~0,1моль/л буры
С1/Z~0,1моль/л буры • V~0,1моль/л буры С1/Z~0,1моль/л (НС1) = -------------------------------------------- V~0,1моль/л (НС1) С1/Z~0,1моль/л буры = С1/Z т. буры • Кп~0,1моль/л буры
С1/Z~0,1моль/л буры = 0,1 моль/л • 1,0120 = 0,1012 моль/л
0,1012 • 10 С1/Z~0,1моль/л НС1 = ------------------=0,1033 моль/л 9,8
С1/Z~0,1 моль/л (НС1) • M1/Z (НС1) T~0,1 моль/л НС1 = ------------------------------------ 1000
0,1033 • 36,46 T~0,1 моль/л НС1 = -------------------- = 0,003766 г/мл 1000
С1/Z ~0, 1моль/л (НС1) Кп~0,1 моль/л НС1 = ------------------------ С1/Z 0,1 моль/л (НС1)
0,1033 Кп~0,1 моль/л НС1 = ---------- = 1,0330 0,1
Ответ: С1/Z~0,1моль/л НС1 =0,1033 моль/л T~0,1 моль/л НС1 = 0,003766 г/мл Кп~0,1 моль/л НС1 = 1,0330
10. Рассчитайте массовую долю химически чистой хлороводородной кислоты в фармацевтическом препарате, если для приготовления 200 мл разведения взяли 2 мл хлороводородной кислоты с ρ = 1,123 г/мл, а на титрование 10 мл полученного раствора было затрачено 7,5 мл раствора гидроксида натрия с молярной концентрацией эквивалента ~ 0,1 моль/л и поправочным коэффициентом равным 1,0262. Мм НСl = 36,46 г/моль.
Дано: Vнав (НС1). = 2 мл Vк. (НС1) = 200 мл Vаликвота (НС1) = 10 мл V(NаОН) = 7,5 мл K (NаОН) = 1,0262 М.м (НС1) = 36,46 г/моль ρ(НС1) = 1,123 г/мл
ω НС1 = ? НС1 – это исследуемый раствор, так как не известна его концентрация NаОН – это титрант, так как известен его поправочный коэффициент Метод количественного определения – метод алкалиметрии, вариант нейтрализации Способ прямого титрования. В основе метода лежит уравнение реакции: HCl + NаОН = NaCl + H2O Т раб./ опр. * V раб. * К раб. ω НС1 = ----------------------------- *100% mнав.НС1
С1/Z т. раб. • M1/Z опр. Т т. раб./ опр. = ----------------------- 1000 M1|z HCl = Mм HCl = 36,46 г/моль 0,1 * 36,46 Т т. раб./ опр. = --------------- = 0,003646 г/мл 1000
2 * 1,123 = 2,246 г – 200мл mнав.НС1 – 10 мл
mнав.НС1 = 2,246 *10 : 200 = 0,1123 г
0,003646 * 7,5 * 1,0262 ω НС1 = ----------------------------- *100% = 25,02% 0,1123 г Массовая доля показывает, что в 100 г раствора хлороводородной кислоты содержится 25,02 г х.ч. хлороводорода.
Ответ: ω (НС1) = 25,02%
ХИМИЧЕСКАЯ ПОСУДА Лабораторная посуда– специальные и специализированные емкости различного конструктивного исполнения, объема, и изготовляемые из разнообразных материалов, устойчивых в агрессивных средах. При необходимости лабораторная посуда обладает необходимой термостойкостью, прозрачностью и другими нужными физическими свойствами. Химическая посуда тонко- и толстостенная изготавливается из стекла разных марок. Посуда из толстого стекла не выдерживает нагрева, нагревать можно только тонкостенную посуду, термостойкость которой зависит от состава стекла. Основным требованием, предъявляемым к стеклянной посуде, является ее химическая и термическая устойчивость. Химическая устойчивость – это свойство стекла противостоять разрушающему действию кислот, щелочей и других веществ. Термическая устойчивость – это способность посуды выдерживать резкие колебания температуры. Лучшим стеклом считается пирекс, потому что оно обладает термической и химической устойчивостью, имеет малый коэффициент расширения. Поэтому особотермостойкие изделия (стаканы, реторты, пробирки) изготавливают из пирексового стекла. Пирексное стекло содержит 80% оксида кремния (IV). Температура его размягчения + 620 ºС. Для проведения опытов при высоких температурах используют кварцевую посуду. Кварцевое стекло содержит 99,95% оксида кремния (IV), температура его размягчения +1650 ºС. Тонкое кварцевое стекло вследствие очень низкого коэффициента термического расширения выдерживает резкое охлаждение (даже водой!) с любой температуры. Лабораторную посуду изготавливают в основном из стекла типов ТУ (термически устойчивое), ХУ-1 и ХУ-2 (химически устойчивое). Содержание оксида кремния (IV) в обычном лабораторном стекле составляет примерно 70%. Перед применением лабораторной посуды она должна быть хорошо вымыта и простерилизована. Для этого ее моют ершами с мыльно – содовым раствором. Чистую посуду промывают проточной водой, затем водой очищенной. При необходимости достижения стерильности лабораторную посуду заворачивают в плотную бумагу и стерилизуют в аэростериле при 160—180 °C 45—60 мин. или в автоклаве при температуре 120 °C 20—30 мин. Посуда считается чистой, если на ее стенках не образуется отдельных капель и вода оставляет равномерную тончайшую пленку. Сушат стеклянную посуду на деревянных колышках, укрепленных на вертикально установленной доске; в сушильных шкафах. |
||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 390. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
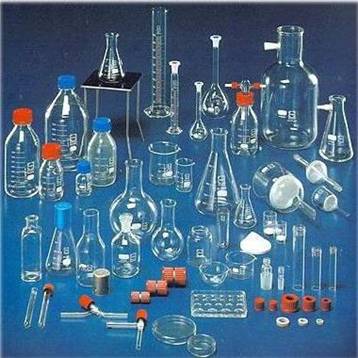 Рис.18. Химическая посуда
Рис.18. Химическая посуда