
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Определение коэффициента переносаВ условиях равновесия ток не протекает через электрод. При равенстве рабочего потенциала и стандартного окислительно-восстановительного потенциала электрода идет непрерывное движение зарядов на электроде через границу электрод/раствор при том, что катодный и анодный ток равны. Абсолютная величина этих токов называется током обмена, с положительным знаком. Ток обмена (i0) равен по модулю катодному и анодному току. Но это равенство нарушается, если происходит смещение потенциала электрода от равновесного. Так, в случае анодного перенапряжения ускоряется движение зарядов в направлении, приводящем к увеличению анодного тока. При этом замедляется движение зарядов, создающих катодный ток. Для учета асимметрии активационного барьера вводят коэффициент переноса (α). Коэффициент переноса (α) – доля перенапряжения, которая увеличивает скорость катодного процесса (0 ≤ α ≤ 1), а величина (1 – α) отвечает доле перенапряжения, которая увеличивает анодный ток.
При том, что измеряемый ток определяется как
А ток обмена частично равен катодному и анодному току при равенстве Е=Е0, получаем уравнение электрохимической кинетики уравнение Батлера – Фольмера:
Чем больше ток обмена, тем более обратим процесс и тем меньше перенапряжение. Эта величина служит критерием обратимости электродной реакции. Для нахождения коэффициента переноса катодного и анодного процесса наиболее часто используют уравнение Тафеля, связывающего перенапряжение и измеряемый ток:
где 
В циклической вольтамперометрии уравнение приводят к следующему виду:
где
Таблица 1. Значения коэфициента переноса.
Из полученных данных видно, что коэффициенты переноса для процессов окисления выше, чем для процессов восстановления. Следовательно, что скорость окисления выше, чем скорость восстановления и процесс идет необратимо. |
||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 891. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
|||||||||||||||||||||||


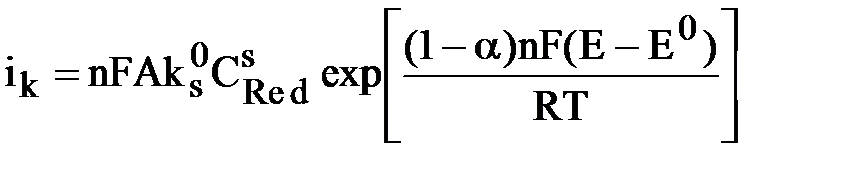

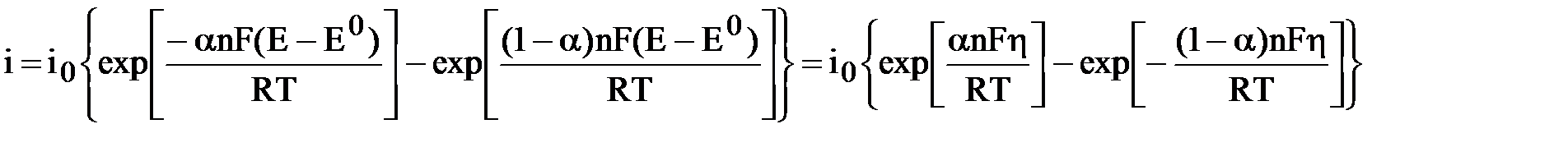 η = E0 – E – катодное перенапряжение стадии разряда – ионизации
η = E0 – E – катодное перенапряжение стадии разряда – ионизации ,
, и
и  для катодного процесса
для катодного процесса и
и  для анодного процесса
для анодного процесса ,
,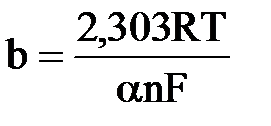 (для катодного процесса) и
(для катодного процесса) и  (для анодного процесса).
(для анодного процесса).