Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Сірководнева (сульфідна) класифікація катіонів на групи
Таблиця 7 Класифікація аніонів на групи
Обладнання, необхідне для проведення якісного аналізу.
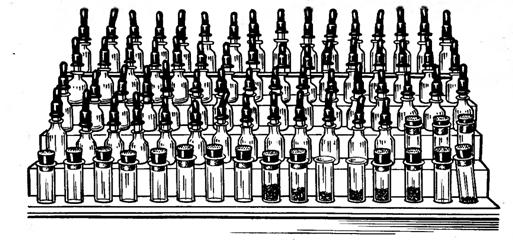
1.11.1. Реактивні склянки. Найзручніше користуватись невеликими склянками місткістю 20-50 мл, в яких зберігаються розчини всіх потрібних реагентів. Зручно такі склянки використовувати в комплекті з піпетками, поміщеними в щільну гумову пробку (рис.6). Таким чином вміст склянок досить надійно ізолюється від повітря, пилу, бруду тощо. Відбирати вміст склянки можна лише за допомогою піпетки. Не слід наливати розчин прямо зі склянки. Після відбору розчину піпеткою її треба повернути на місце, щоб не переплутати пробок із піпетками з різних склянок. Останнє може призвести до забруднення реактивів. Не слід також торкатися піпеткою стінок пробірки, предметного скла і т.п., так як при цьому також можливе забруднення. 
Рис.6 Штатив з набором реактивів
Склянки з реактивами розміщуються у визначеному порядку в штативі для реактивів. Кожен штатив встановлюється на робочому столі і служить для індивідуальної роботи. Категорично забороняється виймати склянки з штатива, так як це може призвести до порушення порядку в їх, розміщенні. Склянки з недостатньо стійкими, отруйними, дурнопахнучими, сухими речовинами, а також концентровані кислоти та основи зберігаються у витяжній шафі і служать для загального користування.
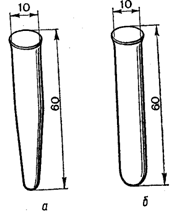
Пробірки. Для індивідуальної роботи студенту надається комплект пробірок – як звичайних, так і центрифужних (рис. 7), які зберігаються в штативі. Пробірки перед використанням ретельно миють, а тоді ополіскують дистильованою водою. В деяких випадках вимиті пробірки сушать. При дослідженні реакцій, що супроводжуються виділенням газів (CO2, SO2, H2S), отвір пробірки закривають пробкою з газовідвідною трубкою. Кінець останньої занурюють у розчин реагенту.
Рис. 7. Центрифужна (а) і звичайна (б) пробірки Стакани та тиглі. Випаровування розчинів зразків, висушування препаратів, їх розчинення зручно проводити в хімічних стаканах (рис. 8) чи фарфорових чашках (тиглях). Скляні стакани не можна нагрівати на відкритому вогні. Краще це робити на електричній плитці, попередньо поклавши на нагрівник шматок азбестової матерії. Прожарювання, плавлення зразків проводять лише у фарфорових тиглях у муфельних печах.
Рис. 8. Хімічний стакан
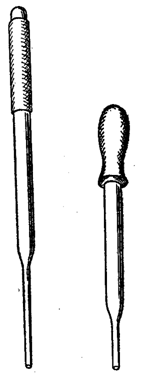
Піпетки. Піпетки (рис. 9) використовуються для відбору певної частини (аліквоти) розчинів досліджуваної речовини чи реагенту, інколи – для відділення розчину над осадом. Гумовою грушею заповнюють піпетку, попередньо занурену носиком у відповідний розчин. Невірне користування піпеткою може бути причиною багатьох неправильних висновків стосовно складу досліджуваної речовини. Тому слід пам'ятати й дотримуватись найпростіших правил: ü Піпетки перед використанням ретельно миють, а тоді промивають дистильованою водою. ü Після роботи не слід класти піпетку на стіл чи штатив, а негайно її вимити й помістити в чисту пробірку.
Рис. 9. Піпетки для якісного аналізу
Миття посуду. Хімічний посуд повинен бути чистим. Його миють йоржиками розчинами соди, лугу, миючими засобами. Полоскання здійснюють теплою, тоді холодною та дистильованою водою. Посуд вважається чистим, якщо з внутрішньої частини вода витікає, не залишаючи краплин. При наявності краплин посуд слід мити знову. Іноді для миття використовують хромову суміш, якою заливають посуд. Залишки хромової суміші добре промивають водою. При роботі з хромовою сумішшю слід бути дуже обережним.Висушують посуд у сушильній шафі.
|
||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-11; просмотров: 634. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |