
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Строение коллоидной частицы.На примере Колло частица состоит из ядра мицеллы (AgI), след слой адсорбционный потенциалопределяющих ионов Ag; адсорбционный слой противоионов Согласно правилу Пескова – Фаянса, на поверхности ядра мицеллы адсорбируются ионы, им в составе ядра, т.е. адсорбируются ионы, находящиеся в избытке. Если получ р-р при избытке иодида калия, то адсорбироваться будут ионы йода. Ионы йода достраивают кристаллич решетку ядра, образуя адсорбционный слой, и придают ядру отриц заряд: m[AgI]nI־. Эти ионы, адсорбирующиеся на поверхности ядра и придающие ему заряд, называются потенциалопределяющими ионами В р-ре находятся также ионы противоположные по знаку потенциалопределяющим ионам, их называют противоионами. В данном случае это катионы К+, которые электростатически притягиваются потенциалопределяющими ионами адсорбционного слоя, образуя гранулу: {m [AgI]nI־ (n – x)K+}x־ – гранула.{m [AgI]nI־ (n - x)K+}x־xK+ - мицелла.Таким образом, мицелла – электрически нейтр коллоидная частица, способн к самостоят существованию. Она определ все основные св-ва коллоидной системы. Сост мицелла из ядра кристаллич или аморфного строения, адсорбционного (неподвижного относительно частицы) и диффузного (подвижного) слоев. При пропускании пост тока через коллоидный раствор к электродам движ не мицеллы, кот электронейтральны, а только гранулы. Наличие одноименного заряда у всех частиц золя явл фактором его устойчивости. Заряд препятствует слипанию и укрупнению колл частиц, т.е. коагуляции. Стабильность (устойчивость) колл частиц объясняется тем, что на поверхн ядер адсорбируется определ вид потенциалопределяющих ионов. Те электролиты, ионы кот явл потенциалопределяющими, следсчитать стабилизаторами, а ионы, кот адсорбируются поверхностью ядер, - стабилизирующими ионами. При этом на ядре адсорбируются те ионы стабилизатора, кот сод элементы, общие с ядром.  Св-ва коллоидных систем. Молекулярно-кинетические св-ва. Молекулярно - кинетич наз св-ва, которые обусловлены хаотическим тепловым движ частиц. Применительно к коллоидным р-рам к этим св-вам следует отнести броуновское движение, диффузию и седиментацию. Броун движ — беспорядочное, хаотичное движ колл частиц. Назв дано по имени англученого Р. Броуна. Броун движ дисперсных частиц происх вследствие непрерывного колебат движ молекул дисперсионной среды. Интенсивность движ тем выше, чем больше темпер, меньше вязкость среды и выше степень дисперсности. Диффузия - самопроизвольный процесс перемещения в-ва в результате беспорядочного тепл движчастиц, вследствие кот происходит выравнивание концентрации р-ра. Скорость диффузии зависит от формы и размеров частиц, темпер и вязкости среды. Скорость диффузии коллоидных частиц меньше скорости диффузии частиц в истинных р-рах. Осмотич давление коллоидных р-ров значительно ниже, чем в истинных р-рах той же концентрации. Объясняется это тем, что колл частицы как по величине, так и по массе в огромное число раз больше обычных молекул. Вследствие этого и кол-во их в колл р-ре во столько же раз меньше, чем в молекул р-ре, а осмотич давление коллоидов пропорционально числу частиц в ед объема. Седиментация — распредел коллоидных частиц по высоте. В нижних слоях р-ра концентрация частиц дисперсной фазы значительно выше, чем в верхних. Если коллоидную систему, им указанное распределение частиц, вывести из этого равновесия, то через некот время она снова придет в прежнее состояние. Скорость установления седиментационного равновесия сравн мала, однако оно сохран в системе в течение неопределенно долгого времени.Отличител св-вом коллоидных систем явл их способность рассеивать свет. Коллоидные частицы обладают св-вом рассеивать во всех направлениях падающие на них лучи света. Путь светового луча внутри р-ра при наблюдение сбоку обозначается в виде светлой полосы, как путь луча, проходящего сквозь щель в ставне в затемненную комнату. Это явление известно под назвм эффектом Тиндаля. Им пользуются для отличия колл р-ров от истинных, так как последние явл-«оптически пустыми», потому что их мелкие частицы не рассеивают свет. Оптич- св-ва дисперсных с-м использ- на практике для изучения их стр-ры, определ- размеров, формы частиц и их концентрации. |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 505. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
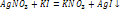
 и диффузионный слой противоионов
и диффузионный слой противоионов