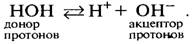Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Показатели качества полуфабрикатов и готовых изделий(по данным Н. Н. Федорова и др., 1986)
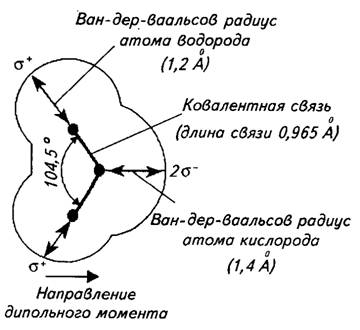
В ряде отраслей пищевой промышленности все большее внимание уделяется электронно-ионной обработке, предусматривающей силовое воздействие электрических полей на электрозаряженные частицы, что ускоряет производственные процессы и улучшает качество готовой продукции. Активацию хлебопекарных прессованных дрожжей проводят путем электронно-ионной обработки в специальной установке. В комплект установки входят источник высокого напряжения, ионизационная камера и электроизмерительные приборы. Такая обработка увеличивает зимазную активность дрожжей. Эффект достигается при силе тока коронного разряда 50 мкА, длительности обработки 15 мин на расстоянии 15 мм между объектом и электродами. Некоторые способы обработки биологических объектов основаны на использовании активированной воды — воды с временно измененными физико-химическими свойствами, приобретенными в результате физического воздействия магнитного или электрического поля, ультразвука, резкого диспергирования и дегазации.  Значительный интерес у исследователей вызывает электрохимическая активация биологических объектов, находящихся в водной среде. Электрохимическая активация основана на изменении свойств воды под действием постоянного электрического тока. Вода и продукты ее диссоциации — водородные и гидроксильные ионы являются важными факторами, определяющими структуру и биологические свойства белков, нуклеиновых кислот, липидов, а также мембран и многих других клеточных компонентов. Прочность связей между молекулами воды обусловлена электрической полярностью ее молекул и объясняет специфическое расположение электронов в атомах кислорода и водорода, составляющих молекулу воды (рис. 3.6). Атом кислорода объединяет пару своих электронов с электронами атомов водорода путем перекрывания 1s-орбиталей атомов водорода с гибридными sр3-орбиталями атома кислорода. Каждая из образующихся при этом связей имеет на одну треть ионный и на две трети ковалентный характер. Методами оптической спектроскопии и рентгеноструктурного анализа были точно определены углы и длины связей в молекуле воды. Средний угол связи Н—О—Н составляет 104,5°, что незначительно отличается от величины 109,5° — угла, соответствующего идеальному тетраэдрическому расположению четырех возможных sр3-орбиталей атома кислорода. Это отклонение от идеального угла объясняют стремлением неспаренных электронов атома кислорода оттолкнуть спаренные электроны (среднее межатомное расстояние Н—О равно 0,965 А).
Рис. 3.6. Кристаллографическая модель молекулы воды 177 Такое расположение электронов в молекуле воды придает ей электронную асимметрию. Более электроотрицательный атом кислорода стремится притянуть электроны атомов водорода, оставляя водородные ядра обнаженными. В результате каждый из двух атомов водорода обладает частичным положительным зарядом (обозначенным σ+), а атом кислорода несет частичный отрицательный заряд (σ –), локализованный в области необобществленных орбиталей. Таким образом, молекула воды в целом хотя и не имеет суммарного заряда, представляет собой электрический диполь. Степень разделения положительного и отрицательного зарядов в полярных молекулах характеризуется дипольным моментом, мерой которого является способность молекулы ориентироваться в электрическом поле. Исходя из величины дипольного момента воды, было вычислено, что каждый атом водорода несет частичный положительный заряд, равный примерно +0,33 ∙ 10–10 электростатической единицы, атом кислорода — отрицательный заряд, равный примерно – 0,66 • 10–10. При электрохимической активации водные растворы и смеси переходят в метастабильное состояние, вызванное структурно-энергетическими и электрохимическими изменениями под воздействием электрического поля. В результате жидкие системы в течение периода релаксации проявляют аномальные свойства в физико-химических превращениях. Несмотря на огромное количество экспериментальных данных, убедительно свидетельствующих о появлении аномальных свойств у обработанной воды, до сих пор не существует единой теории активации воды, так как не ясна сама природа этого явления. Поэтому теоретическое изучение свойств активированной воды находится пока в стадии гипотез. Появление аномальных свойств у активированных жидких водных сред может быть обусловлено как изменением состояния самой воды, так и влиянием растворенных в ней компонентов. Последние весьма сильно и разнообразно влияют на структуру воды, вызывая заметное изменение ее свойств. Присутствие полярных растворенных веществ, например NaCl, вызывает определенные изменения в структуре жидкой воды, так как каждый ион Na+ и Сl– окружен оболочкой водных диполей. Геометрия таких гидра-тированных ионов отличается от геометрии «мерцающих скоплений», образованных за счет водородных связей. При растворении NaCl в воде в концентрации, близкой к его концентрации в биологических жидкостях, в трехмерной структуре жидкой воды происходят значительные изменения. Соли как бы ломают структуру воды. Одни ионы, например Fe3+, Ca2+, Na+, SО42–, ослабляют трансляционное движение окружающих их молекул воды, тогда как другие — К+, CI–, J– — усиливают их подвижность. Особый интерес вызывает электрохимическая обработка водных систем с разделением анодного и катодного пространств диафрагмой. При этом получают две фракции активированной жидкости: кислотная у анода (анолитная фракция) и щелочная у катода (католитная фракция). Эти фракции ведут себя в ряде случаев, как щелочи и кислоты. Согласно концепции Бренстера—Лоури кислота рассматривается как донор протонов, а основание — как акцептор протонов. Кислотно-основная реакция всегда включает в себя сопряженную кислотно-основную пару, состоящую из донора протонов и соответствующего ему акцептора протонов:
Вода слабо диссоциирует, образуя ионы гидроксония (Н3О+) и гидрсильные ионы (ОН–). Ионы гидроксония гидратированы в воде и реально существуют в виде ионов H9О4+ (рис. 3.7).
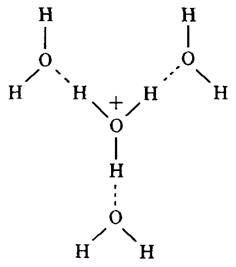
Протоны могут «перескакивать» от Н3О+ на соседнюю молекулу Н2О с очень большой скоростью. Эти «перескоки» протонов обусловливают высокую электрическую подвижность протонов в воде, значительно превосходящую скорость диффузионного перемещения самих ионов Н3О+. Способность протонов легко проходить сквозь массу связанных водородными связями молекул воды имеет большое значение для функционирования биологических систем. В разбавленных водных растворах отношение концентраций ионов Н+ и ОН– выражается следующей зависимостью: Кw = [Н+][ОН–] = 1 • 10–14 (при 25 °С). Концентрацию водородных ионов в биологических системах выражают через рН, величина которого численно равна отрицательному логарифму концентрации ионов Н+ (pH = lg[H+]). Каталитическая активность ферментов находится в значительной зависимости от рН. При электролизе воды с инертным анодом на электродах происходят окисление и восстановление молекул воды согласно реакциям: катод: 2Н2О + 2е– → Н2 + 2ОН–; анод: 2Н2О – 4е– → 02 + 4Н+. Таким образом, в приэлектродных зонах образуются различные окислительно-восстановительные системы, рН которых существенно различаются. При электролизе энергия затрачивается на осуществление химических реакций, повышение кинетической энергии атомов, молекул, ионов, которые проявляются в виде выделения теплоты. Часть энергии расходуется на увеличение потенциальной энергии компонентов электролита. Вода под действием постоянного тока изменяет свою активность. Происходит временное отклонение (электрохимическая активация) потенциальной энергии от термодинамического равновесного значения. При униполярной обработке воды без перемешивания катодной и анодной зон электрохимическая активация сохраняется достаточно долго после отключения внешнего источника энергии, подаваемой к электролизеру. Не менее важен вопрос о появлении в активированной воде свободных радикалов. В силу своей природы свободные радикалы несут в себе большой запас энергии, полученный ими при разрыве межмолекулярных связей. Они чрезвычайно реакционноспособны, легко взаимодействуют с компонентами водной смеси. Эти изменения после активации обусловлены изменением потенциальной энергии, которая расходуется на химические превращения веществ и выделение теплоты. Свойства такой воды изменяются, при этом целенаправленно можно регулировать рН. Электрохимическая обработка — самый мощный из известных методов активации и легкоуправляемый процесс. Это объясняется тем, что изменение потенциальной энергии приэлектродной среды в ту или иную сторону достигается в результате направленного потока электронов из электрода в среду и наоборот. Существование неустойчивых химически активных соединений в системе после активации определяет в значительной мере его реакционную способность в различных технологических процессах. Известны результаты исследований по использованию электроактивированной воды при гидротермической обработке зерна: действие католита на крахмал и белки зерна пшеницы приводит к укреплению клейковины муки и повышению степени повреждения крахмальных зерен. Электрохимическая активация способствует снижению кислотности молока, уменьшению кислотного числа жиров; при низком значении рН электроактивированная вода инвертирует сахарозу в водных растворах. Одной из отраслей пищевой промышленности, где эффективно могут быть использованы принципы электрохимической активации с целью рационального расхода сырья, интенсификации процессов приготовления теста, улучшения биотехнологических свойств бродильной микрофлоры, полуфабрикатов и их реологических характеристик, повышения качества и пищевой ценности продуктов, является хлебопекарная. Оказываемое мощное воздействие на дрожжевые клетки — живой организм обусловлено наличием чрезвычайно тонких и чувствительных элементов — сложных белков-ферментов, которые в естественных условиях способствуют протеканию биохимических реакций. Кроме того, активация, по-видимому, повышает производительность биомембран и способствует более интенсивному действию ферментов. Такая обработка влияет на энергетическое состояние компонентов биохимических реакций без изменения их химического состава и окружающей среды. Этот эффект обусловлен трансмембранным потенциалом, который возникает при электрохимической активации. Энергия активирующего воздействия оказывает влияние на скорость и направление процессов, протекающих с преодолением энергетического барьера, а именно на реакции переноса заряда через биологические мембраны. Активная кислотность среды оказывает существенное влияние на живые организмы. Оптимальное значение рН способствует интенсификации жизнедеятельности микроорганизмов, ускоряет процесс регенерации отдельных клеток. Наиболее рациональное значение рН для перестройки дрожжевых клеток в фазе активации равно 5,0. Для установления и поддержания рН используют различные приемы: в жидких фазах используют серную, соляную или молочную кислоту, а также минеральные соли. Для достижения в зоне рН 5,0 используют электрохимический активатор. Дрожжевую суспензию при соотношении воды и дрожжей 5:1с гомогенностью 112 конгломератов в 1 см3 суспензии подвергают электрохимическому воздействию (плотность тока 5,5—6,6 мА/м2, период обработки 1—2 мин, рН 4,8—5,2). При этих параметрах конгломераты дрожжевых клеток полностью разрушаются. Этот процесс обусловлен следующим. При электролизе изменяется диэлектрическая проницаемость водной фазы и снижается величина поверхностного натяжения на границе раздела жидкой и твердой фаз. Подводимая энергия затрачивается не только на проведение химических реакций, но и на увеличение потенциальной энергии. Молекулы воды, ассоциации клеток, гидратированные ионы и микрочастицы совершают колебательные движения. При их резонансе возникают кванты энергии, способные деформировать связи, изменять структурную характеристику системы, разрушать конгломераты. В результате электрохимического воздействия подъемная сила дрожжей улучшается на 2—4 мин за счет увеличения одиночных клеток. Незначительный эффект обусловлен отсутствием питательных веществ в смеси и потреблением дрожжевыми клетками собственного гликогена. При микроскопировании дрожжей установлено, что после электрохимической активации и выдержки в течение 10—15 мин объем дрожжевых клеток уменьшается. Эффективной является выдержка дрожжевых клеток в питательной смеси, представляющей водный раствор ячменного, ячменно-кукурузного или кукурузного гидролизата, полученного из дробленого зерна. Питательную смесь, содержащую дрожжевые клетки, предварительно подвергают электрическим воздействиям. Зерно ячменя и кукурузы в хлебопекарном производстве не используется из-за низких хлебопекарных свойств. Однако при дополнительной обработке такого зерна можно получить продукты, представляющие интерес для интенсификации технологического процесса. Одним из доступных способов обработки этого сырья является получение из него ферментативных гидролизатов. Гидролизаты получают следующим образом. Дробленое зерно (ячменя, или ячменя и кукурузы в соотношении 1:1, или кукурузы) смешивают с водой температурой 45—50 °С в соотношении 1:4. Добавляют ферментный препарат амилосубтилин Г10х в количестве 0,1 % к массе дробленого зерна, нагревают до температуры 80—85 °С и выдерживают в течение 10—15 мин. Затем охлаждают до температуры 52—55 °С и добавляют ферментную композицию МЭК-1 в количестве 0,08 % к массе дробленого зерна. Смесь выдерживают, соблюдая следующие температурные паузы: 52—55 °С — 20—25 мин; 61—63 °С — 30—40; 70—72 °С — 30—40 мин. После этого гидролизат нагревают до 75—77 °С и фильтруют. Затем подвергают термообработке при 100 °С, центрифугируют и подают на вакуум-упаривание при температуре 57—60 °С и разрежении 0,05—0,06 МПа. Такая обработка позволяет извлечь из нехлебопекарного зерна доступные для дрожжей питательные вещества (табл. 3.8). Таблица 3.8 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 527. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||