
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Вольтамперометрия с линейной разверткой потенциала для твёрдых вращающихся электродовСтр 1 из 9Следующая ⇒ УДК 547 ББК 24 Г 77 Методические разработки предназначены для студентов 2 курса агрономического факультета КазГАУ
Составители: доц. Сагитова Р.Н. доц. Давлетшина Л.Н. проф. Фаизов Т.Х.
Методические разработки утверждены и рекомендованы к печати на заседании кафедры общей химии от 09.02.12, протокол № 7 и учебно-методической комиссии агрофака от 20.02.12., протокол № 9. Рецензенты: Проф. Гайсин И.А., КазГАУ Проф. Гильманшина С.И., К(П)ФУ
©Казанский государственный аграрный университет, 2012 Вольтамперометрия– группа электрохимических методов анализа, в которых контролируемый параметр — потенциал индикаторного электрода, меняется во времени, а измеряемой величиной является ток, протекающий через индикаторный электрод. Электролиз раствора анализируемого вещества в вольтамперометрии проводят, постепенно повышая напряжение и, фиксируя при этом силу тока. В электролитической ячейке используется легкополяризующийся индикаторный электрод (ИЭ) и неполяризующийся электрод сравнения (ЭС). Потенциал электрода сравнения не меняется во времени, следовательно, все значимые электрохимические процессы, связанные с изменением потенциала и силы тока, будут происходить на индикаторном электроде. В качестве индикаторных электродов используют электроды из ртути (стационарные ртутные электроды – висящая ртутная капля или плёночные ртутные электроды), платины, графита, стеклоуглерода. Метод анализа с использованием ртутного капающего электрода называют полярографией. Каломельный электрод или хлоридсеребряный электрод используются как электроды сравнения.  Результаты электролиза раствора в вольтамперометрии представляют в виде поляризационных кривых
Двухэлектродная (а) и трёхэлектроднаая ячейка для вольтамперометрических измерений.
Для обеспечения постоянной ионной силы и достаточной электропроводности раствора в ячейку помещают раствор индиферрентного электролита (фона) с концентрацией 0.05 – 1.0 моль/л, который не принимает участия в электродной реакции. Вольтамперометрия с линейной разверткой потенциала для твёрдых вращающихся электродов
Вольтамперограммы, полученные с помощью вращающегося или капающего электрода при монотонном изменении (линейной развертке) напряжения, имеют вид, схематически представленный на рисунке. Участок увеличения тока называют волной. Волны могут быть анодными, если электроактивное вещество окисляется, или катодными, если оно восстанавливается.
Типичная кривая сила тока – потенциал (вольтамперограмма) при линейной развертке потенциала для вращающегося электрода с постоянной площадью или ртутного капающего электрода. h – высота волны (предельный диффузионный ток Id, мкА) Е1/2 – потенциал полуволны, В
На вольтамперограмме можно выделить три участка. А – пологий участок, ток с изменением потенциала изменяется слабо. Небольшой ток, протекающий на начальном участке вольтамперограммы, называется остаточным,значительную часть которого составляет ток заряжения двойного электрического слоя. Величина остаточного тока имеет порядок Б – резкий подъём тока за счет электрохимической реакции (диффузионный ток).При увеличении потенциала достигается потенциал, при котором начинается электрохимическая реакция, то есть электроактивное вещество (деполяризатор) начинает разряжаться на поверхности электрода
Сила тока возрастает, на поляризационной кривой наблюдается резкий подъём, электрод деполяризуется. Концентрация ионов-деполяризаторов (восстанавливающихся или окисляющихся ионов) вокруг электрода резко падает, создается обедненный слой, который пополняется ионами за счет процессов механической конвекции и диффузии. Создаются условия, характерные для стационарной диффузии, поэтому ток называетсядиффузионным В – пологий участок, после завершения электрохимической реакции, ток практически не меняется, предельный диффузионный токконтролируется условиями конвективной (стационарной) диффузии. Характеристики вольтамперограммы:
1. Предельный диффузионный ток I , мкА. Для вращающихся электродов с постоянной площадью величина предельного диффузионного тока Id, мкА, и пропорциональная ему высота волны h, мм, линейно зависят от концентрации деполяризатора в растворе:
где n – число электронов, участвующих в электрохимической реакции; D – коэффициент диффузии, см2∙с-1; с – концентрация моль/л; S – площадь поверхности электрода (см 2);
F – число Фарадея (Кл/моль)
Для ртутного капающего электрода аналогичная зависимость описывается уравнением Ильковича:
где n – число электронов; D – коэффициент диффузии, см2∙с-1; m – скорость вытекания ртути, мг/с; с – концентрация ммоль/л t – время жизни капли ртути, с (2 – 3 с)
2. Потенциал полуволны (Е1/2, В)не зависит от силы тока, а, значит, и концентрации окисляющегося или восстанавливающегося вещества; характеризует природу деполяризатора и непосредственно связан с величиной Е0 данной окислительно-восстановительной системы:
n – число электронов; F – число Фарадея, Кл/моль;
Форма волны для обратимой электрохимической реакции описывается уравнением:
n – число электронов; F – число Фарадея, Кл/моль.
Потенциал полуволны является качественной характеристикой иона в растворе, и определение потенциала полуволны составляет основу качественного вольтамперометрического анализа.
|
||
|
Последнее изменение этой страницы: 2018-04-11; просмотров: 557. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 . Для их регистрации электролитическую ячейку с вращающимся или стационарным индикаторным электродом и электродом сравнения присоединяют к специальному прибору – вольтамперометру. Используют двух- или трёхэлектродную ячейку. Двухэлектродная ячейка включает индикаторный электрод (ИЭ) и электрод сравнения (ЭС). При регистрации вольтамперограмм может протекать довольно заметный электрический ток, поэтому рекомендуют применять трёхэлектродную ячейку, в которую для токоотвода от индикаторного электрода дополнительно вводят вспомогательный электрод (ВЭ) (платиновая проволочка).
. Для их регистрации электролитическую ячейку с вращающимся или стационарным индикаторным электродом и электродом сравнения присоединяют к специальному прибору – вольтамперометру. Используют двух- или трёхэлектродную ячейку. Двухэлектродная ячейка включает индикаторный электрод (ИЭ) и электрод сравнения (ЭС). При регистрации вольтамперограмм может протекать довольно заметный электрический ток, поэтому рекомендуют применять трёхэлектродную ячейку, в которую для токоотвода от индикаторного электрода дополнительно вводят вспомогательный электрод (ВЭ) (платиновая проволочка).


 А (∼0.1 мкА).
А (∼0.1 мкА). (один из вариантов электрохимической реакции)
(один из вариантов электрохимической реакции)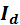 .
.
 – круговая частота вращения электрода (рад/с);
– круговая частота вращения электрода (рад/с); – кинематическая вязкость раствора (см 2/с);
– кинематическая вязкость раствора (см 2/с);
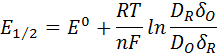
 - потенциал полуволны, В
- потенциал полуволны, В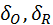 - толщина диффузного слоя
- толщина диффузного слоя - стандартный окислительно-восстановительный потенциал системы (В)
- стандартный окислительно-восстановительный потенциал системы (В) ,
, 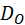 - коэффициенты диффузии,
- коэффициенты диффузии, 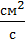 ;
; – температура, К;
– температура, К; - универсальная газовая постоянная,
- универсальная газовая постоянная, 

 - ток (мкА) или высота волны (мм) в любой точке восходящего участка вольтамперограммы;
- ток (мкА) или высота волны (мм) в любой точке восходящего участка вольтамперограммы; – предельный диффузионный ток (мкА) или высота волны (мм) при 250С на участке потенциалов предельного диффузионного тока;
– предельный диффузионный ток (мкА) или высота волны (мм) при 250С на участке потенциалов предельного диффузионного тока;