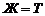Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Диаграммы двухкомпонентных конденсированных системКраткие теоретические сведения Диаграммы состояния конденсированных систем описывают межфазные равновесия а) между жидкостью и твердым веществом – процессы плавления, растворения, кристаллизации, образования или разрушения химических соединений; б) между разными твердыми фазами - процессы изменения кристаллической структуры вещества или полиморфные превращения, образования твердых растворов; Уравнение правила фаз Гиббса записывается в следующем виде:
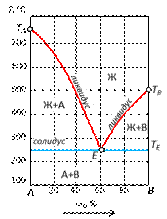
где S – число степеней свободы системы, т.е. число параметров состояния, которые можно изменять в определенных пределах без изменения фазового состава системы; K – число компонентов системы, т.е. минимальное число составных частей системы, необходимое для ее полного описания; F – количество фаз системы, т.е. число ее гомогенных частей, разделенных между собой поверхностями раздела. Диаграммы состояния конденсированных систем обычно изображаются в изобарических координатах. По оси абсцисс указан состав системы в мольных или массовых долях (процентах) по компоненту В. По осям ординат указана шкала температур. По линиям А и В показаны температурные точки, характерные для чистых веществ: температуры плавления и полиморфных превращений.
Рис. 16. Простейшая диаграмма состояния двухкомпонентной конденсированной системы Каждый элемент диаграммы имеет свое графическое обозначение в виде поля или сочетания линий диаграммы. К элементам диаграммы относят: 1) растворимость жидкостей – полная/неполная; 2) наличие твердых растворов замещения/внедрения; 3) наличие полиморфных превращений; 4) наличие химических соединений постоянного или переменного состава и характер плавления этих соединений – с разложением или без него.  Общая характеристика диаграммы складывается из описания наличия/отсутствия определенных элементов диаграммы. Любая диаграмма состояния имеет следующие основные линии: ликвидус, солидус, эвтектика. Ликвидус является самой верхней линией диаграммы и разделяет поле жидкой фазы и поля, содержащие твердую и жидкую составляющие. На ликвидусе начинается процесс кристаллизации и заканчивается процесс плавления вещества. Ликвидус показывает зависимость температуры начала кристаллизации от состава системы. Ликвидусу соответствует равновесие
Солидус отграничивает поля, содержащие жидкую фазу от других полей диаграммы. Поля диаграммы, расположенные ниже солидуса, не содержат жидкой фазы и не имеют границы с полями, в составе которых есть одна или несколько жидких фаз. На солидусе заканчивается процесс кристаллизации вещества и начинается процесс плавления. |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 452. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
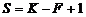 ,
,