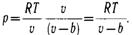Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Уравнение состояния реальных га-зов. В реальных газах в отличие от иде- альных существенны силы межмолеку- лярных взаимодействий (силы притяже- ния, когда молекулы находятся на значи- тельном расстоянии,и силы отталкивания при достаточном сближении их друг с другом) и нельзя пренебречь собствен- ным объемом молекул. Наличие межмолекулярных сил от- талкивания приводит к тому, что молеку- лы могут сближаться между собой толь- ко до некоторого минимального расстоя- ния. Поэтому можно считать, что свобод- ный для движения молекул объем будет равен у — Ь, где b— тот наименьший объем, до которого можно сжать газ. В соответствии с этим длина свободного пробега молекул уменьшается и число ударов о стенку в единицу времени, а следовательно, и давление увеличива- ется по сравнению с идеальным газом в отношении v/(v — b), т.е.
Силы притяжения действуют и том же направлении, что и внешнее давле- ние, и приводят к возникновению молеку- лярного (или внутреннего) давления. Сила молекулярного притяжения каких- либо двух малых частей газа пропорцио- нальна произведению числа молекул в каждой из этих частей, т. е. квадрату плотности, поэтому молекулярное давле- ние обратно пропорционально квадрату удельного объема газа: рмол = а/vквадрат, где а — коэффициент пропорциональности, зависящий от природы газа. Отсюда получаем уравнение Ван- дер-Ваальса A873 г.): (p + a/v'2)(v-b)=RT/(v-b) При больших удельных объемах и сравнительно невысоких давлениях ре- ального газа уравнение Ван-дер-Ваальса практически вырождается в уравнение состояния идеального газа Клапейрона, ибо величина a/v2 (по сравнению с р)  и b (по сравнению с и) становятся прене- брежимо малыми. Уравнение Ван-дер-Ваальса с ка- чественной стороны достаточно хорошо описывает свойства реального газа, но результаты численных расчетов не всег- да согласуются с экспериментальными данными. В ряде случаев эти отклонения объясняются склонностью молекул ре- ального газа к ассоциации в отдельные группы, состоящие из двух, трех и более молекул. Ассоциация происходит вслед- ствие несимметричности внешнего элек- трического поля молекул. Образовавши- еся комплексы ведут себя как самостоя- тельные нестабильные частицы. При столкновениях они распадаются, затем вновь объединяются уже с другими мо- лекулами и т. д. По мере повышения тем- пературы концентрация комплексов с большим числом молекул быстро уменьшается, а доля одиночных молекул растет. Большую склонность к ассоциа- ции проявляют полярные молекулы вод яного пара
|
||
|
Последнее изменение этой страницы: 2018-05-27; просмотров: 325. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |