Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Газовые смеси, способы задания, вычисление параметров состояния, кажущейся молекулярной массы и газовой постоянной смеси, определение парц давлгазовые смеси. В качестве примера можно назвать продукты сгорания топлива в двигателях внутреннего сгорания, топках печей и па- ровых котлов, влажный воздух в сушиль- ных установках и т. п. Основным законом, определяющим поведение газовой смеси, является закон Дальтона: полное давление смеси иде- альных газов равно сумме парциальных давлений всех входящих в нее компо- нентов:
давление, которое имел бы газ, если бы он один при той же температуре занимал весь объем смеси. Способы задания смеси. Состав га- зовой смеси может быть задан массовы- ми, объемными или мольными долями. Массовой долей называется отношение массы отдельного компонента Mi к массе смеси М: gi= Mi/M. Массовые доли часто задаются в процентах. Например, для сухого воз- духа gN2«77%; gO2«23%. Объемная доля представляет собой отношение приведенного объема газа V, к полному объему смеси V: ri=Vi/V Приведенным называется объем, который занимал бы компонент газа, ес- ли бы его давление и температура равня- лись давлению и температуре смеси. Для вычисления приведенного объема запишем два уравнения состоя- ния j-ro компонента: PiV=MtRiT; pVi = MiRiT. Первое уравнение относится к состоянию компонента газа в смеси, когда он имеет парциальное давление р, и занимает пол- ный объем смеси, а второе уравнение — к приведенному состоянию, когда давле- ние и температура компонента равны, как и для смеси, р и Т. Из уравнений следует, что Иногда бывает удобнее задать со- став смеси мольными долями. Моль- ной долей называется отношение количества молей Ni, рассматриваемого компонента к общему количеству молей  смеси N. В соответствии с законом Авогадро объемы моля любого газа при одинако- вых р и Т, в частности при температуре и давлении смеси, в идеально газовом состоянии одинаковы. Поэтому приве- денный объем любого компонента может быть вычислен как произведение объема моля Vмю на число молей этого компо- нента, т. е. Vi= VмюNi, а объем смеси — по формуле V=VмюN Тогда Vi/V = ri = = Ni/N, и, следовательно, задание смеси идеальных газов мольными долями рав- нозначно заданию ее объемными долями. Газовая постоянная смеси газов pV = MRcмT, D.45) где что смесь идеальных газов также подчиняется уравнению Клапейрона. Кажущаяся молекулярная масса смеси.
Соотношение между объемными и массо- Выми долями
8Первое нач термодинамики. Сущность, формулировки Первое начало термодинамики- один из трех основных законов термодинамики, представляющий собой закон сохранения энергии для систем, в которых существенное значение имеют тепловые процессы. Согласно первому началу термодинамики, термодинамическая система (например, пар в тепловой машине) может совершать работу только за счёт своей внутренней энергии или каких-либо внешних источников энергии. Первое начало термодинамики объясняет невозможность существования вечного двигателя 1-го рода, который совершал бы работу, не черпая энергию из какого-либо источника.Сущность первого начала термодинамики заключается в следующем: При сообщении термодинамической системе некоторого количества теплоты Q в общем случае происходит изменение внутренней энергии системы U и система совершает работу А: Q = U + A Уравнение (1.4), выражающее первое начало термодинамики, является определением изменения внутренней энергии системы (U), так как Q и А — независимо измеряемые величины. Внутреннюю энергию системы U можно, в частности, найти, измеряя работу системы в адиабатном процессе (то есть при Q = 0): Аад = — U, что определяет U с точностью до некоторой аддитивной постоянной U0: U = U + U0 Первое начало термодинамики утверждает, что U является функцией состояния системы, то есть каждое состояние термодинамической системы характеризуется определённым значением U, независимо от того, каким путём система приведена в данное состояние (в то время как значения Q и А зависят от процесса, приведшего к изменению состояния системы). При исследовании термодинамических свойств физической системы первое начало термодинамики обычно применяется совместно со вторым началом термодинамики. |
||
|
Последнее изменение этой страницы: 2018-05-27; просмотров: 406. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
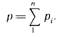 Парциальное давление р, —
Парциальное давление р, —