Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Каскадный механизм мобилизации и синтеза гликогенаСтр 1 из 6Следующая ⇒ Углеводы, их классификация. Углеводы (У) – это органические соединения, содержащие альдегидную или кето- группы, и являющиеся производными многоатомных спиртов. Термин «углеводы» предложен в 1844г. К. Шмидтом, т.к. в то время полагали, что их общая формула представляет собой: Сх(Н2О)n – т.е. углерод + вода. Дальнейшие исследования показали, что это не так. Например: формула дезоксирибозы С5Н1oО4. Поэтому позднее было предложено этот класс веществ называть глицидами. Углеводы широко распространены в природе. В растениях их содержание ≈ 80%, в тканях животных всего ≈ 2%. Для животных организмов их значение велико. Функция углеводов. - энергетическая: при окислении У выделяется энергия, используемая в биохимических реакциях (при распаде 1г У выделяется ≈ 4,1% ккал). - пластическая: продукты обмена У являются источниками для синтеза Ж, Б, НК, АК. - опорная: целлюлоза оболочек растительных клеток образует опорные ткани растений. - защитная: У учувствует в построении клеточных мембран. Классификация углеводов Моносахариды – это производные многоатомных спиртов, у которых одна гидрокси-группа (ОН) замещена на карбонильную (С=О альдегидную или кето) группу. Если карбонильная группа находится в конце цепи, то моносахарид представляет собой альдегид и называется альдозой, при любом другом положении моносахарид является кетоном и называется кетозой. Номенклатура: наименования моносахарам дают в зависимости от числа атомов С + окончание – оза. Три атома углерода - триоза, 4 - тетроза, 5 - пентоза, 6 - гексоза, 7 - гептоза, и т.д. Н2С – ОН Н2С – ОН Н С = О  | | | С = О ! НС – ОН " НС* – ОН | | | Н2С – ОН Н2С – ОН Н2С –ОН дегидроксиацетон трехатомный спирт глицеральдегид (кетотриоза) (глицерин) (альдотриоза). - Моносахараобладают оптической активностью и пространственной изомерией. N=2ª, где N – число изомеров, а - количество хиральных атомов. Т.о. у альдотриозы м.б. 2=2¹ изомера. - Если ОН-гр. у последнего хирального атома С находится слева, то это L – ряд, а если справа, то это моносахара Д-ряда. У нас изображен Д – глицеральдегид.
- Если раствор этого соединения вращает плоскость поляризованного луча вправо, то обозначает «+», а если влево, то знаком «-». Направление угла вращение заранее непредсказуемо: например природная глк (+), а фрк (-). - Формулы моносахаридов м.б. линейными и циклическими. Их называют соответственно формулами Фишера и Хеуорса.
- В зависимости от того, ОН-гр. какого из углеродов атомов участвует в образовании полуацетеля, могут образоваться пяти- или шестичленные циклы, которые по аналогии с органическими соединениями называются фуранозными или пиранозными структурами. - В циклических молекулах пентоз и гексоз появляется еще один хиральный атом и новая пара изомеров (α- и ß- формы). Если Он-группа у С1 располагается над плоскостью, то это ß- форма, а если под плоскостью, то это α -форма. Олигосахариды – это сложные молекулы, содержащие в своем составе от 2-х до 10 мономеров звеньев. Различают дисахариды, трисахариды и т.д. Дисахариды– это сложные молекулы, которые при гидролизе распадаются на 2 молекулы моносахаридов. Мальтоза – состоит из 2-х молекул α-глюкозы, соединенных 1"4 гликозидной связью
Изомальтоза –состоят из 2-х молекул α -Д-глюкозы, (1"6) гликозидной связью α -Д-глюкопиранозил (1"6) α –Д-глюкопираноза Целлобиоза – состоит из 2-х молекул ß-глюкозы, соединенных 1"4 глик. связью
Лактозасостоит изß-галактозы и α-глюкозы, соединенных (1"4) гликозидной связью Сахароза – состоит из α-глюкозы и ß-фруктозы, соединенных 1"2 гликозидной связью
α -Д-глюкоиранозил (1"2) ß –Д-глюкофуранозаранозид Трисахариды – раффиноза (фруктоза+глюкоза+галактоза) Полисахариды (полиозы) – это глициды, содержащие от 10 до несколько тысяч мономеров. По строению высшие полиозы делят на следующие группы: I. Гомополисахариды, состоящие из остатков одного какого-либо моносахарида: а) из остатков глюкозы — крахмал, гликоген, декстран, целлюлоза и др.; б) из остатков маннозы, галактозы, ксилозы, L-арабинозы — маннаны, галактаны, ксиланы, арабаны; в) из остатков галактуроновой кислоты — пектиновые вещества; г) из остатков глюкозамина — хитин насекомых и грибов II. Гетерополисахариды, состоящие из остатков различных моносахаридов и их производных: а) гемицеллюлозы (компоненты крови); б) камеди, слизи; в) мукополисахариды или протеиногликаны (свободные и связанные с белками, например, в гликопротеинах: гепарин, хондроитинсульфаты, групповые вещества крови). По биологическим функциям высшие полиозы делят на следующие группы: I. Структурные полисахариды, играющие опорнуюроль в организмах растений и животных: целлюлоза и пектиновые вещества растений, хитин насекомых и грибов. П. Резервные полисахариды, являющиеся источником энергии для живых организмов: крахмал, гликоген, инулин.
Крахмал [C6 H10O5]n; Мr 105–107Да. Это резервный гомополисахарид, состоит из 2-х гомополисахаридов; амилозы – линейной формы, и амилопектина – разветвленной формы. Доля амилозы ≈10-30%, сод. до 1 тысяч остатков глк. в амилопектине (его доля в крахмале ≈90-70%) глюкозных остатков в 20-30 раз больше. Остатки глк в амилозе и линейных участках амилопектина соединяется 1"4 гликозидной связью; в точках разветвления 1"6 гликозидной связью. амилоза
Гликоген[C6 H10 O5]n – главный энергетический резерв человека и животных. Формула аналогична формуле крахмала. Mr 105–108Да . Особенно много его в печени (до 10%) и мышцах (до 4% от сухой массы). Состоит также из амилопектина, только молекула более компактная, т.к. имеет более разветвленную структуру. Крахмал и гликоген при кислотном гидролизе распадаются сначала на декстрины, затем на дисахариды – мальтозу и изомальтозу, затем на две глюкозы. Целлюлоза (клетчатка) – это структурный полисахарид растительного происхождения, состоящий из ß-D–глюкопиранозных остатков, соединенных 1"4 гликозидной связью. Mr=1-2млн Да. В организме человека и животных не переваривается; т.к. отсутствует фермент ß–глюкозидаза. В присутствии в пище оптимального количества целлюлозы формируются каловые массы.
Обмен углеводов Складывается из: 1) расщепления полисахаридов в ЖКТ до моносахаров, которые всасываются из кишечника в кровь; 2) синтеза и распада гликогена в тканях; 3) анаэробного и аэробного расщепления глк; 4) взаимопревращения гексоз; 5) аэробного метаболизма ПВК; 6) глюконеогенеза - синтеза глк из неуглеводных компонентов – ПВК, лактата, АК, глицерина и др. источников. Основной метаболит в обмене углеводов – это глюкоза. Её источники: 1) углеводы пищи 2) гликоген 3) ПВК, АК, глц и т.д.
Переваривание углеводов (крахмала). 1. Ротовая полость. Слюна содержит фермент амилазу α, ß, γ (различаются по конечным продуктам их ферментативного действия). α–амилаза – это эндоамилаза, которая действует на 1"4 внутренние связи полисахаров ß- и γ-амилазы – это экзоамилазы – расщепляют концевые 1"4 связи ß–амилаза – дисахарид мальтозу; γ- амилаза – один за другим концевые остатки глк. Амилаза слюны представлена только α–амилазой, поэтому результатом ее действия являются крупные обломки гликогена и крахмала – декстрины и в небольшом количестве мальтоза. 2. Желудок. Далее пища, более или менее смоченная слюной, поступает в желудок. В результате кислой среды желудка (рН 1,5–2,5) α–амилаза слюны инактивируется. В глубоких слоях пищевого комка действие амилазы продолжается и происходит расщепление полисахаридов с образованием декстринов и мальтозы. В самом желудке распада У нет, т.к. здесь отсутствует специфические энзимы. 3. Основной этап расщепления У происходит в 12 перстной кишке. В просвет кишечника выделяется панкриатическая α-амилаза (рН–7). Панкреатическая амилаза расщепляет только 1"4 гликозидные связи. Но, как известно, молекула гликогена разветвленная. В точках ветвления 1"6 гликозидной связи, на нее воздействует специфические ферменты: (глюкоза) олиго-1,6-глюкозидаза и (крахмал) амило-1,6-глюкозидаза. В кишечнике под действием этих 3-х ферментов У расщепляются до дисахаридов (мальтоза и др.). На связи в дисахаридах эти ферменты не воздействуют. Для этих целей в кишечнике существует свои ферменты: их название – корень дисахарида + аза: мальтаза, сахараза и т.д. В результате суммарного воздействия этих ферментов образуется смесь моносахаридов – глюкоза, галактоза, фруктоза. Основную массу составляет глюкоза. 4.Всасывание глюкозы происходит за счет активного транспорта с Na+. Глк + Na+ образует комплекс, который поступает внутрь клетки, здесь комплекс распадается, Na+ выводится наружу. Другие моносахара всасываются диффузно (т.е. по градиенту концентрации). Поступающая из просвета кишечника глк большей частью (> 50%) с кровью воротной вены поступает в печень, остальная глк через общий кровоток транспортируется в другие ткани.
Транспорт глк в клетки носит характер облегченной диффузии, но во многих клетках регулируетсягормоном поджелудочной железы инсулином (исключение – мозг и печень – здесь содержание глк прямо пропорционально концентрации глк в крови). Действие инсулина приводит к перемещению белков переносчиков из цитозоля в плазматическую мембрану. Затем с помощью этих белков глк транспортируется в клетку по градиенту концентрации. Инсулин т.о. повышает проницаемость клеточной мембраны для глк. Концентрация глк в крови в норме поддерживается на постоянном уровне и составляет 3,33 – 5,55 мкмоль/л, что соответствует 80-100 мг в 100 мл. крови.
Влияние инсулина на перемещение транспортёров глюкозы из цитоплазмы в плазматическую мембрану. 1 - связывание инсулина с рецептором; 2 - участок инсулинового рецептора, обращённый внутрь клетки, стимулирует перемещение транспортёров глюкозы. 3,4-транспортёры в составе содержащих их везикул перемещаются к плазматической мембране клетки, включаются в её состав и переносят глюкозу в клетку.
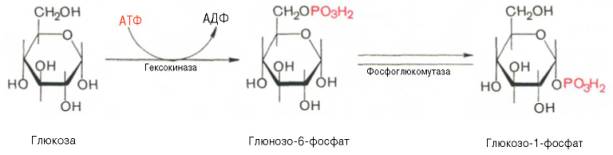
ТЕМА: УГЛЕВОДЫ II Цель:Сформировать и закрепить у студентов системные знания об основных путях метаболизма глюкозы, о клеточных и нейро-гуморальных механизмах регуляции углеводного обмена. ПЛАН ЛЕКЦИИ 1. Биосинтез гликогена. 2. Распад гликогена. 3. Синтез глюкозы из глицерина. 4. Механизм фосфорилитического отщепления остатка глюкозы от гликогена. 5. Каскадный механизм мобилизации и синтеза гликогена. 6. Анаэробный гликолиз, стадии, энергетический баланс. Синтез и распад гликогена. Наиболее важным углеводом организма человека является глюкоза. Она поступает с пищей, в глюкозу превращаются углеводы в печени, из глюкозы могут образоваться все остальные углеводы в организме. Она является универсальным топливом. Глюкоза превращается в гликоген в печени, и гликоген служит источником глюкозы в организме. Биосинтез гликогена – гликогенез происходит в процессе пищеварения (в течении 1-2 часов после приема углеводной пищи). Особенно активно гликогенез происходит в печени и мышцах: 1– 2. Фосфорилирование глк
Катализирует реакцию фермент гексокиназа. В печени также есть фермент глюкокиназа класс Трансферазы. Клеточная мембрана проницаема для глк, но не проницаема для фосфорилирования, фосфорилированная глк как бы запирается в клетке.
3. Через фосфодиэфирную связь глюкоза соединяется с УДФ. УДФ–глк. является активированной формой глк, непосредственно включающейся в реакцию полимеризации. УДФ – глюкоза переносит глюкозный остаток на затравочное количество гликогена, уже имеющегося в мышцах или печени. Глюкозо-1-фосфат + УТФ < = > Н4Р2О7 + (пиррофосфат) 4.
5. УДФ + Н3РО4нуклеозиддифосфаткиназа УТФ ост. АТФ При этом АТФ → АДФ
Т.о. строятся линейныеотрезки гликогена, т.е. образуется 1→4 гликозидные сязи. Образование разветвлений в молекуле гликогена происходит под действием специфического гликогенветвящего фермента амило(α1,4→α1,6)трансгликозилазы, которые переносят короткие фрагменты (по 2-3 глюкозных остатка) с одного участка гликогена на другой и образует 1,6-гликозидные связи (точка ветвления). Путем чередования действия этих двух ферментов наращивается молекула гликогена. Е гликогенсинтетаза находится в организме в двух формах: фосфорилированная или неактивная форма, которая называется гликогенсинтетаза Д; нефосфорилированная или активнаягликогенсинтетаза I. Переход этих форм друг в друга происходит с помощью двух ферментов: Киназы гликогенсинтетазы Фосфотазы гликогенсинтетазы АТФ киназа АДФ
Нефосфорил-я, активнаяфосфорилир.неактивная гликогенсинтетазаI фосфотаза гликогенсинтетаза Д Фн Среднее содержание гликогена в печени колеблется в пределах 5-7% а) при нормальном смешанном питании глк превращается в - гликоген 3% - жиры 30% - окисляется до СО2, Н2О – 70% б) при обильном углеводном питании глк превращается в - гликоген 10% - жиры 40% - окисляется до СО2, Н2О – 50% в) при голодании в течении суток почти весь гликоген без остатка утилизируется и его не удается обнаружить в печени обычными биохимическими реакциями. Содержание гликогена в печени зависит от его синтеза (гликогенеза) или распада (гликогенолиза). Распад гликогена (гликогенолиз) происходит двумя путями гликоген _____________________________________________________________
Фосфоролиз (+Фн) гидролиз (+Н2О) Глюкоза-1-фосфат глюкоза Глюкоза-6-фосфат
Лактат (гликолиз) Гидролиз гликогена (крахмала) происходит в ЖКТ под действием специфических амилаз. Энергетически более выгодным является второй путь расщепления гликогена – фосфоролиз. Фосфоролитический распад играет ключевую роль в мобилизации полисахаридов.
(C6H10O5)n + H3PO4гликогенфосфорилаза (C6H10O5)n–1 + Глюкозо-1-фосфат,
где (С6Н10О5)n означает полисахаридную цепь гликогена, а (С6Н10О5)n ту же цепь, но укороченную на один глюкозный остаток. В этой реакции от нередуцирующего конца отщепляется один остаток глюкозы и соединяется в фосфорной кислотой, процесс повторяется многократно, пока весь полимер не будет расщеплен до точки ветвления. Образуется остаточный декстрин. Другой фермент изоамилаза,разрывает 1→6 гликозидные сязи, далее для действия фосфорилазы отрывается новый участок полисахаридной цепи. Фосфоролиз энергетически более выгоден, т.к. в результате образуется глюкоза уже в активированном состоянии – глюкоза-1-фосфат, которая легко вступает в различные реакции. Гликоген Фн 1
Глюкоза-1-фоосфат 2 Глюкоза-6-фосфат
Анаэробный гликолиз Синтез глюкозы (лактат) Синтез глюкозы из глицерина 1. глк-1-ф фосфоглюкомутаза глк-6-ф 2. глк-6-ф + Н2О глк-6-фосфотазапечени глк + H3PO4 Механизм фосфорилитического отщепления остатка глюкозы от гликогена. Гликогенфосфорилаза или просто фосфорилаза существует в двух формах: А и В. Форма А более активна, чем В. Отличаются они друг от друга тем, что: фосфорилаза А это тетрамер, состоящий из 4-х субъединиц с Мr=360000Да фосфорилаза В – димер, содержащий две субъединицы, его Мr=180000Да. Превращение неактивной формы в активную протекает по схеме: 2 фосфорилазы В + 4 АТФ акт.киназа фосфорилазы Вфосфорилаза А + 4 АДФ Под действием адреналина и глюкогона запускается каскад реакций, который заканчивается распадом гликогена. Каскадный механизм мобилизации и синтеза гликогена
Неактивная киназа фосфорилазы превращается в активную под влиянием фермента цАМФ-зависимой протеинкиназы. Активная форма последней образуется при участии цАМФ, которая в свою очередь образуется из АТФ под действием фермента аденилатциклазы, стимулируемой, в частности, адреналином и глюкагоном. Увеличение содержания адреналина в крови приводит в этой сложной цепи реакций к превращению фосфорилазы В в фосфорилазу А и, следовательно, к освобождению глюкозы в виде глюкозо-1-фосфата из запасного полисахарида гликогена. Обратное превращение фосфорилазы А в фосфорилазуВ катализируется ферментом фосфатазой (эта реакция практически необратима). При отсутствии потребности организма в дополнительной глюкозе распад гликогена прекращается. Под действием специфических ферментов происходит инактивирование фосфорилазы А и активирование гликогенсинтазы I, начинается синтез гликогена. Т.о. активирование 1-го фермента каскада – аденилатциклазы приводит к увеличению распада гликогена и подавлению его синтеза. Гликолиз В клетках организма человека и других высших организмов образование энергии происходит не только в просе окислительного фосфорилирования (аэробным путем), но и в ходе распада питательных веществ без участия О2 (анаэробным путем). Главным источником получения энергии анаэробным путем служат гексозы, прежде всего α-Д-глюкоза. Гликолиз – это анаэробный распад глк до 2-х молекул молочной кислоты (лактата), протекающих в гиалоплазме клетки. Суммарное уравнение анаэробного гликолиза
Это экзергонический процесс (выделяется энергия). Освобождающаяся в результате гликолиза энергия аккомулируется в фосфатных связях АТФ. По имени авторов, изучавших этот процесс более проблемно, гликолиз называют путем Элебдена-Мейергофа-Парнаса. Отдельные стадии гликолиза катализируются 11-ю ферментами. Анаэробный гликолиз можно подразделить на две стадии:
СТАДИЯ 1.↓ Р-ция фосфорилирования глк, т.е. перенос остатка ортофосфата на глюкозу за счет АТФ. Реакция катализируется ферментом гексокиназой:
Образование глюкозо-6-фосфата в гексокиназной реакции сопровождается освобождением значительного количества свободной энергии системы и процесс практически необратим. Глк-6-ф в отличии от глк, не проходит через мембрану и как бы «запирается в клетке». Гексокиназа существует в виде четырех изомеров. Первые три преобразуют различные виды гексоз, включая глк. Гексокиназа IV (глюкокиназа) фосфорилирует только глк, имеется в печени, включается в работу при значительных концентрациях глк в крови воротной вены. Остальные изоформы существуют во всех органах и тканях. Гексокиназа ингибируется глюкозо-6-фосфатом, т.е. последний служит одновременно и продуктом реакции, и аллостерическим ингибитором.
2.↓↑ Изомеризация глюкозо-6-фосфата в фруктозо-6-фосфат:
Эта реакция протекает легко в обоих направлениях, и для нее не требуется каких-либо кофакторов.
3.↓ Образовавшийся фруктозо-6-фосфат фосфорилируется за счет второй молекулы АТФ:
Данная реакция аналогично гексокиназной практически необратима и является наиболее медленно текущей реакцией гликолиза, так как здесь происходит резкое падение свободной энергии. Фермент фосфофруктокиназа по своей природе аллостерический фермент. Она ингибируется АТФ и стимулируется АМФ. При значительных величинах отношения АТФ/АМФ активность фосфофруктокиназы угнетается и гликолиз замедляется. Напротив, при снижении этого коэффициента интенсивность гликолиза повышается. Во время работы мышцы происходит интенсивное потребление АТФ и активность фосфофруктокиназы повышается, что приводит к усилению процесса гликолиза. Фосфофруктокиназа – это «ключевой» фермент гликолиза, он лимитирует скорость всего процесса гликолиза. 4.↓↑ Под влиянием ферментаальдолаза фруктозо-1,6-дисфосфат расщепляется на две фосфотриозы:
Эта реакция обратима. При повышении температуры реакция сдвигается в сторону большего образования триозофосфатов дигидроксиацетонфосфата (ДАФ) и глицеральдегид-3-фосфата (ГАФ)). 5.↓↑Реакция изомеризации триозофосфатов.
Равновесие данной реакции сдвинуто в сторону дигидроксиацетонфосфата. Образуется ≈95% дигидроксиацетонфосфата и 5% глицеральдегид-3-фосфата. В последующие реакции гликолиза включается только глицеральдегид-3-фосфат. По мере его потребления в ходе дальнейших превращений дигидроксиацетонфосфат превращается в глицеральдегид-3-фосфат.
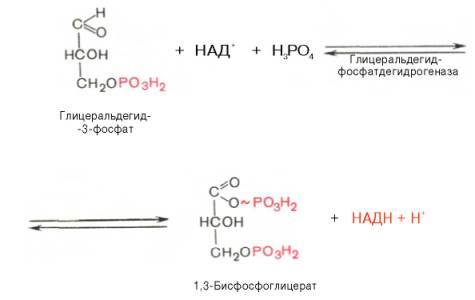
СТАДИЯ 6.↓↑Окисление глицеральдегид-3-фосфата в присутствии ферментаглицеральдегид-фосфатдегидрогеназы, кофермента НАД и неорганического фосфата (гликолити-ческая оксидоредукция) с образованием 1,3-бисфосфоглицериновой кислоты и восстановленной формы НАД (НАДН2).
Реакция обратима, продукты реакции блокируют фермент, поэтому необходимо использовать их непрерывно в ходе реакции.
7. ↓↑Передача богатого энергией фосфатного остатка (фосфатной группы в положении 1) на АДФ с образованием АТФ и 3-фосфоглицериновой кислоты (3-фосфоглицерата):
Р-ция экзергоническая, происходит значительное падение свободной энергии, равновесие сдвинуто влево. Реакция обратима – это первая реакция гликолиза где образуется АТФ. В отличие от окислительного фосфорилирования образование АТФ из высокоэнергетических соединений называется субстратным фосфорилированием.
8.↓↑Реакция изомеризации. Сопровождается внутримолекулярным переносом оставшейся фосфатной группы. Реакция легкообратима, протекает в присутствии ионов Mg2+.
9. ↓↑ Реакция дегидратации. Катализируется ферментом енолазой, при этом 2фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту (фосфоенолпируват). В результате образуется еще 1 макроэргическая связь. Реакция обратима.
Енолаза активируется двухвалентными катионами Mg2+ или Мn2+ и ингибируется фторидом.
10. ↓2-ая реакция гликолитического фосфорилирования. Реакция необратима, т.к. характеризуется резким падением свободной энергии, разрывом высокоэргической связи и переносом фосфатного остатка от фосфоенолпирувата на АДФ (субстратное фосфорилирование). Синтезируется еще одна молекула АТФ.
Активируется в присутствии ионов Mg2+, одновалентных катионов щелочных металлов (К+ или др.).
11. Восстановление пировиноградной кислоты до молочной кислоты. Реакция протекает при участии фермента лактатдегидрогеназы и кофермента НАДН2, образовавшегося в шестой реакции:
Продукт реакции лактат является «тупиком» в обмене веществ, т.к. не вступает ни в один биохимический процесс, кроме обратного превращения в ПВК. При накоплении лактата в клетке нарушается ее рН и останавливается гликолиз. Т.о. Анаэробный гликолиз – это распад глюкозы до ПВК (с 1-ой до 10 р-ции). При потребности в большем количестве энергии происходит дальнейшее окисление ПВК (ее окислительное декарбоксилирование, преобразование в ацетил-КоА и полное окисление в ЦТК. Энергетический баланс и биологическая функция гликолиза. Распад АТФ происходит в 1-ой и 3-ей реакциях, на стадии фосфорилирования глк и фрк. Если учесть, что весь дигидроксиацетон (5-я реакция), превращается в альдегид, то дальше происходят биохимические превращения двух триоз, а значит образование 4-х молекул АТФ в двух стадиях гликолитического фосфорилирования, т.е. образование двух молекул АТФ на одну молекулу глюкозы. Три фермента – гексокиназа, фосфофруктокиназа, пируваткиназа (три необратимые реакции) лимитируют скорость гликолиза. Кроме того, контроль гликолиза осуществляется также ЛДГ и ее изоферментами. Воздействуя на них можно регулировать эту скорость. Хотя анаэробный гликолиз дает малый выход энергии (2 молекулы АТФ на 1 мол глк), это единственный процесс в клетках организма, образующий энергию в отсутствии кислорода. Поэтому в кризисных ситуациях (гипоксия) роль анаэробного гликолиза неоценимо велика, т.к. гликолиз протекает во всех клетках и тканях. В этом биологическая роль гликолиза.
Энергетическая ценность аэробного гликолиза. При окислении 1 молекулы глюкозы в аэробных условиях (с 1-10 реакции) образуется 2 молекулы АТФ. 10-я реакция заканчивается образованием ПВК. Причем при распаде 1 молекулы глюкозы образуется 2 молекулы ПВК. В реакциях окислительного декарбоксилирования 2-х ПВК 2 мол. НАД·H2 · 3 ═ 6 мол АТФ В ЦТК 6 мол. НАД·H2 · 3 ═ 18 мол АТФ 2 мол. ФАД·H2 · 2 ═ 4 мол АТФ Субстр. Фосфорилир-е = 2 мол АТФ В гликолизе 2 мол АТФ 32 молекулы АТФ образуется при окислении 1 молекулы глюкозы в аэробных условиях.
ТЕМА: УГЛЕВОДЫ III Цель:Дать представление о основных путях тканевых превращений глюкозы, механизмы регуляции углеводного обмена, патологии, возникающие в результате его нарушения. ПЛАН ЛЕКЦИИ 1. Глюконеогенез, обходные пути необратимых реакций 2. Пентозофосфатный цикл окисления глюкозы. 3. Регуляция углеводного обмена. 4. Патология углеводного обмена.
Глюконеогенез – это синтез глюкозы из неуглеводных продуктов: молочной и пировиноградной кислоты, так называемых гликогенных аминокислот, глицерина и т.д. Главное место процесса печень, в меньшей степени почки и слизистая жкт. Глюконеогенез протекает при длительном голодании. Можно было бы считать, что глюконеогенез это процесс обратный анаэробному гликолизу. Но 3 реакции гликолиза (гексокиназная, фосфофруктокиназная и пируваткиназная) необратимы, путь обратный гликолизу «снизу вверх» невозможен, поэтому в процесс глюконеогенеза на 3 этапах существуют обходные пути необратимых реакций и используются другие ферменты. I Обходной путь (путь синтеза глюкозы из пирувата) Образование фосфоенолпирувата из пирувата в обход пируваткиназы
1 - пируваткарбоксилаза; 2 - малатдегидрогеназа (митохондриальная); 3 -малатдегидрогеназа (цитоплазматическая); 4 - фосфоенолпируваткарбоксикиназа. Синтез фосфоенолпирувата осуществляется в несколько этапов. 1.(№10) Первоначально пируват проникает в митохондрии, под влиянием пируваткарбоксилазы и при участии СО2 и АТФ карбоксилируется с образованием оксалоацетата (ЩУК):
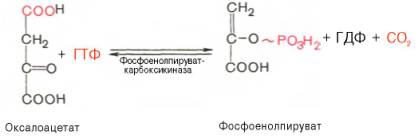
2. Затем оксалоацетат возвращается в цитоплазму и в результате декарбоксили-рования и фосфорилирования под влиянием ферментафосфоенолпируваткарбоксилазы превращается в фосфоенолпируват. Донором фосфатного остатка в реакции служит гуанозинтрифосфат (ГТФ):
Далее идут обратимые реакции гликолиза до следующей необратимой реакции. Фосфоенолпируват, образовавшийся из пирувата, в результате ряда обратимых реакций гликолиза превращается во фруктозо-1,6-бисфосфат. II Обходной путь (обход фосфофруктокиназной реакции(№3), которая необратима) 1. Глюконеогенез идет в обход этой эндергонической реакции. Превращение фруктозо-1,6-дифосфата (бисфосфата) во фруктозо-6-фосфат, катализируется специфи-ческой фосфатазой:
2. В последующей обратимой стадии биосинтеза глюкозы фруктозо-6-фосфат превращается в глюкозо-6-фосфат. фруктозо-6-фосфата глюкозофосфатизомеразаглюкозо-6-фосфата III. Обходной путьгексокиназной реакции(№1)
Гликолиз и глюконеогенез.
Круглыми стрелками указаны «обходные» пути глюконеогенеза при биосинтезе глюкозы из пирувата и лактата; цифры в кружках обозначают соответствующую стадию гликолиза. Свободная глюкоза поступает из ткани в кровь. Гликолиз и гликонеогенез тесно взаимосвязаны. При максимальной активности мышц в них накапливается молочная кислота, она диффундирует в кровь и в печени превращается в глюкозу (глюконеогенез), которая в процессе своего распада используется как энергетический субстрат, необходимый для деятельности мышечной ткани. Взаимосвязь между процессами гликолиза в мышечной ткани и глюконеогенезом в печени может быть представлена в виде схемы:
|
||||||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 558. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |

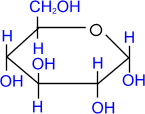 α, D- глюкопираноза
α, D- глюкопираноза 



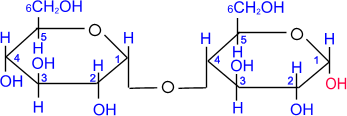 α -Д-глюкопиранозил (1"4) α –Д-глюкопираноза
α -Д-глюкопиранозил (1"4) α –Д-глюкопираноза ß-целлобиоза (1"4)
ß-целлобиоза (1"4)  ß-Д галактопиранозил (1"4) Д-глюкопираноза
ß-Д галактопиранозил (1"4) Д-глюкопираноза