
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Классификация экстракторов.I. В зависимости от вида контакта между жидкими фазами: 1. Дифференциально-контактные, в которых характер изменения фаз приближается к непрерывному. 2. Ступенчатые – в которых изменение состава фаз происходит скачкообразно (ступенчато) и в каждой ступени осуществляется перемешивание и разделение (сепарация фаз). II. Экстракторы без механических перемешивающих устройств(колонныеаппараты: распылительные, полочные, насадочные, тарельчатые, ситчатые). III. Механические экстракторы–экстракторы с подводимой внешнейэнергией (роторно-дисковые, пульсационные или вибрационные, центробежные и аппараты с мешалками из группы смесительно-отстойных экстракторов. Адсорбция Адсорбция–процесс поглощения одного или нескольких компонентовиз газовой смеси или раствора твердым веществом. Механизм процесса адсорбции отличается от абсорбции, вследствие того, что извлечение веществ осуществляется твердым поглотителем. Адсорбция широко применяется в химической технологии: - для осушки газов и их очистки с выделением ценных компонентов; - для извлечения растворителей из газовых или жидких смесей; - для осветления растворов; - для очистки газовых выбросов и сточных вод. Адсорбат–вещество,поглощаемое в процессе адсорбции. Адсорбент –твердое вещество,которое поглощает один или несколькокомпонентов из газовой смеси или раствора в процессе адсорбции. В качестве адсорбентов применяются твердые вещества с большой удельной поверхностью, обычно относимой к единице массы вещества (активированные угли, силикагели, цеолиты, синтетические ионообменные смолы – иониты).  Требования к промышленным адсорбентам: a. большая адсорбционная способность поглощать большие количества адсорбтива при малой его концентрации в газовой или жидкой фазах; b. высокая селективность - избирательное поглощение только одного компонента из смеси; c. химическая инертность по отношению к компонентам разделяемой смеси; d. высокая механическая прочность; e. способность к регенерации для последующего повторного использования; f. низкая стоимость. Приведём наиболее распространённые промышленные сорбенты. Активные углиполучаются термической обработкой без доступа воздуха различных углеродсодержащих веществ: древесины, углей, плодовых косточек – с последующей активацией. В зависимости от назначения в активных углях могут преобладать микропоры либо, наряду с ними, и мезопоры. Приготовленные из неполярного материала, активные угли хорошо сорбируют неполярные вещества, например, многие органические соединения, в частности углеводороды. Активные угли отличаются невысокой механической прочностью. Силикагелии алюмогелипредставляют собой продукты термической обработки (обезвоживания) гелей кремниевой и алюминиевой кислот. Эти сорбенты хорошо поглощают полярные вещества, в частности воду, и поэтому часто используются для осушки газов. Механическая прочность селикагелей и алюмогелей значительно выше чем у активных углей. Цеолиты– природные, а в последнее время всё в большей степени синтетические алюмосиликаты – слабополярные сорбенты, пригодные для сорбции как полярных, так и неполярных веществ. Цеолиты отличаются высокой однородностью пор, а потому и высокой селективностью, т.е. способностью адсорбировать из сплошной среды молекулы определённого размера. Это позволяет использовать набор цеолитов с различными размерами пор для поочерёдной сорбции различных (от мелких молекул к крупным) поглощаемых компонентов из исходной смеси. При физической адсорбциимолекулы адсорбтива не вступают смолекулами адсорбента в химическое взаимодействие: адсорбируемые молекулы сохраняют свою индивидуальность, а теплота адсорбции относительно невелика (примерно до ~ 60,000 кДж/кмоль). Малые значения величины теплоты и времени адсорбции дают возможность вести процесс физической адсорбции в условиях его обратимости, т.е. последовательно проводить стадии адсорбции и выделения поглощенных компонентов из адсорбента – десорбции. При химической адсорбции (хемосорбции)молекулы адсорбтивавступают в химическое взаимодействие с адсорбентом; выделяемая при этом теплота адсорбции значительно превосходит теплоту физической адсорбции, а время задержки молекул адсорбтива в адсорбенте велико, в результате чего обратный процесс (десорбция) сильно тормозится и практически неосуществим. Истинная плотность адсорбента –масса единицы объёма плотногоадсорбента (без учета пор). Кажущаяся плотность адсорбента –масса единицы объёма пористогоматериала адсорбента. Насыпная плотность адсорбента-масса единицы объёма слояадсорбента, включая объём пор в гранулах адсорбента и между гранулами адсорбента. Периодические процессы адсорбции могут проводиться по четырех-, трех- и двухфазному способам. Четырехфазный способ работы адсорбера–состоит из4хстадий: 1) собственно адсорбция; 2) десорбция поглощенного компонента острым водяным паром; 3) сушка адсорбента; 4) охлаждение адсорбента. Трехфазный способ работы адсорбера–применяется при отсутствииодной из 2х – последних стадий (охлаждения или сушки). Например, без стадии охлаждения адсорбент охлаждается отработанным воздухом, поступающим из аппарата, который находится на стадии адсорбции; без стадии сушки после проведения адсорбции слой адсорбента продувают горячим инертным газом; что исключает возможность увлажнения адсорбента и необходимость его сушки, а затем адсорбент охлаждают холодным воздухом, и цикл повторяется. Двухфазный способ работы адсорбера-осуществляется безобособления стадий сушки и охлаждения адсорбента; при этом различают двухфазный способ: 1) с совмещением сушки и охлаждения со стадией адсорбции; 2) без стадии сушки. Несмотря на сложность и своеобразие процесса, основные закономерности для процесса адсорбции имеют сходство с абсорбцией. Так, для адсорбции, как и для абсорбции будет справедливо уравнение материального баланса (2.62):
где ХН – начальное содержание сорбтива, отнесенное к единице веса сорбента; ХК – конечное содержание сорбтива, по окончании цикла работы аппарата. Следует иметь в виду, что при проведении процесса адсорбции адсорбент находится чаще всего в неподвижном состоянии, а газ профильтровывается через его слой. В уравнении (2.62) под L следует понимать не часовой расход адсорбента, а количество его, которое загружено в аппарат. В последнее время стали применять адсорберы непрерывного действия, в которых адсорбент движется навстречу газовой смеси. В этом случае уравнение вполне идентично уравнению материального баланса процесса абсорбции. Количество адсорбированного вещества за время τ может быть по аналогии с процессом абсорбции найдено из уравнения (2.63):
где β – коэффициент адсорбции; F – поверхность адсорбента, м2; ΔC –движущая сила выражаемая разностью концентраций. Адсорберы –аппараты для проведения процессов адсорбции.Различаютследующие типы адсорберов: с неподвижным слоем поглотителя, с движущимся слоем поглотителя, с кипящим слоем поглотителя; непрерывного и периодического действия; вертикальные и горизонтальные. Целью расчета периодически действующих адсорберовявляетсяопределение основных габаритов адсорбера: диаметра и высоты. Диаметр адсорбера с неподвижным слоем адсорбента(2.64):
где Определение высоты адсорбера связано с определением высоты слоя адсорбента (2.65):
где u – скорость движения зоны массопередачи, м/с; Целью расчета непрерывнодействующих адсорберовявляетсяопределение основных габаритов адсорбера (диаметра, высоты) и расхода адсорбента. Диаметр адсорбера непрерывного действияопределяется аналогичноадсорберу периодического действия, фиктивную скорость парогазовой смеси w0 рассчитывают исходя из необходимости обеспечить заданный гидродинамический режим. Высота слоя адсорбента(2.66):
где GV - объемный расход паро-газовой смеси, м3/с; noy - число единиц переноса; S – площадь сечения слоя, м2; KyV - объемный коэффициент массопередачи, кг/(м3·с·ед.движ.силы). Расход адсорбента(2.67):
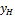 , ,  - начальная и конечная относительные концентрации парогазовой смеси кг компонента/кг смеси; - начальная и конечная относительные концентрации парогазовой смеси кг компонента/кг смеси;  - относительная равновесная концентрация извлекаемого компонента в отработанном адсорбенте, кг компонента/кг адсорбента; - относительная равновесная концентрация извлекаемого компонента в отработанном адсорбенте, кг компонента/кг адсорбента; 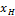 - начальная относительная концентрация извлекаемого компонента в адсорбенте, кг компонента/кг адсорбента. - начальная относительная концентрация извлекаемого компонента в адсорбенте, кг компонента/кг адсорбента.
В химической промышленности наибольшее распространение получили адсорберы с неподвижным слоем адсорбента. В качестве примера, рассмотрим односекционный адсорберс псевдоожиженным слоем высокодисперсного сорбента (рис. 2.15). Поток исходного газа I, содержащего адсорбтив, является ожижающим агентом: пройдя газораспределительное устройство 7, он приводит в псевдоожиженное состояние мелкозернистый сорбент II и покидает слой через сепарационное устройство 3 и систему циклонов 4. Расширенное сепарационное пространство уменьшает пылеунос благодаря понижению рабочей скорости газа. Сорбент, отделённый в циклонах от газового потока, возвращается в псевдоожиженный слой по стоякам 2. Поток свежего сорбента IIс постоянно подаётся в аппарат питателем. Поток насыщенного адсорбатом сорбента IIн непрерывно отводится из аппарата. При высоких тепловых эффектах адсорбции, если газ необеспечивает необходимого отвода теплоты, в псевдоожиженном слое размещают холодильные устройства 5, позволяющие поддерживать температуру процесса на должном уровне.
Ионный обмен Ионообменный процесс–избирательное поглощение одного илинескольких компонентов из растворов с помощью катионов и анионов ионита, используемое в химической технологии для глубокой очистки растворов; удаления из сточных вод вредных примесей и организации оборотного водоснабжения; для разделения металлов с близкими свойствами. Катион–положительно заряженная частица. Анион–отрицательно заряженная частица. Иониты–природные или синтетические адсорбенты,нерастворимые вводе и в обычных растворителях, обладающие подвижными ионами , которые способны обмениваться на эквивалентное количество ионов раствора. Катионит–ионит,обменивающийся с раствором подвижнымикатионами – ионами водорода Н+ или другими положительно заряженными частицами. Анионит–ионит,обменивающийся с раствором подвижными анионами – ионами гидроксила ОН- или другими отрицательно заряженными частицами. По степени ионизации (способности к обмену подвижными ионами) катиониты и аниониты делятся: I. Катиониты. 1. Высокоионизированные катиониты – КУ (универсальные), обладают способностью к обмену ионов Н+ с широким диапазоном изменения рН раствора. 2. Слабоионизированные катиониты – КБ (буферные), способны к обмену ионов Н+ на ион металла только в щелочных и отчасти нейтральных растворах. II. Аниониты. 1. Высокоионизированные АВ, обладают универсальным действием. 2. Низкоионизированные АН, способны обмениваться анионами лишь в кислых и отчасти нейтральных растворах. Амфотерные иониты–иониты,способные к катионному и анионному обмену одновременно. Типичные реакции ионного обмена: 1. Катионный обмен (2.68):
где R – органическая основа ионита с какой-либо заряженной функциональной группой. 2. Анионный обмен (2.69):
Обменная емкость ионита-количество функциональных групп(катионов или анионов), принимающих участие в обмене, которое выражается в эквивалентных единицах и относится к единице количества ионита, г-экв/м3. Уравнение баланса ионов в растворе(2.70):
уравнение баланса ионов в ионите(2.71):
где С0, a0 – начальная концентрация ионов в растворе и в адсорбенте соответственно; Сi – концентрация ионов, перешедших из ионита в раствор; Сj – концентрация ионов, оставшихся в растворе; аi - концентрация ионов, оставшихся в ионите; аj - концентрация ионов, перешедших из раствора в ионит. Способы проведения ионообменных процессов: − в статических условиях:в аппарат периодического действия загружаютионит и раствор, полученную суспензию перемешивают до насыщения ионита адсорбирующимся веществом; − в динамических условиях:раствор пропускают через неподвижный слойионита до момента проскока, данный способ позволяет осуществить более глубокую очистку раствора по сравнению со статическим методом, вследствие последовательного контакта очищенного раствора со свежими, неотработанными слоями ионита. |
|||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 451. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 (2.62)
(2.62) (2.63)
(2.63) (2.64)
(2.64)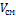 - объемный расход парогазовой смеси или раствора, проходящего через слой адсорбента, м3/с;
- объемный расход парогазовой смеси или раствора, проходящего через слой адсорбента, м3/с;  – фиктивная скорость парогазовой смеси, определяемая с учетом технико-экономических показателей, м/с.
– фиктивная скорость парогазовой смеси, определяемая с учетом технико-экономических показателей, м/с. (2.65)
(2.65) - время защитного действия слоя, с;
- время защитного действия слоя, с;  - потеря времени защитного действия слоя, с.
- потеря времени защитного действия слоя, с.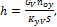 (2.66)
(2.66)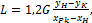 (2.67)
(2.67)
 (2.68)
(2.68) (2.69)
(2.69) (2.70)
(2.70)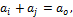 (2.71)
(2.71)