Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Биохимическая функция в организме
Витамин В12 служит предшественником двух коферментов: метилкобаламина в цитоплазме и дезоксиаденозилкобаламина в митохондриях. Метилкобаламин – кофермент, участвующий в образовании метионина из гомоцистеина. Кроме того, он принимает участие в превращениях производных фолиевой кислоты, необходимых для синтеза нуклеотидов – предшественников ДНК и РНК. Дезоксиаденозилкобаламин в качестве кофермента участвует в метаболизме жирных кислот с нечётным числом углеродных атомов и аминокислот с разветвленной углеводородной цепью. Витамин Н (биотин) (антисеборейный)
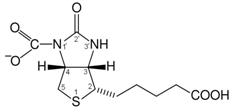
В основе строения биотина лежит тетрагидротиофеновое кольцо, к которому присоединена молекула мочевины, а боковая цепь представлена валериановой кислотой.
N1-имидазольного кольца является местом карбоксилирования. Связываясь с ионом гидрокарбоната (НСО3¯), биотин превращается в карбоксибиотин, приобретая свойства кофермента.
Биотин способен образовывать с авидином – гликопротеином белка куриного яйца – прочный комплекс, который не расщепляется пищеварительными ферментами. Поэтому при частом употреблении сырых яиц прекращается всасывание присутствующего в пище биотина. Способность молекул авидина и биотина специфически связываться друг с другом используется в некоторых методах очистки в биотехнологии.
Биохимическая функция Витамин Н способствует усвоению тканями ионов бикарбоната и активирует реакции карбоксилирования и транскарбоксилирования в составе следующих карбоксибиотинил-содержащих ферментов: - Пируваткарбоксилазы – фермента, катализирующего АТФ-зависимое образование оксалоацетата из пирувата и НСО3¯.  Пируваткарбоксилаза является тетрамерным белком, несущим четыре молекулы биотина, каждая из которых связана с остатком лизина апофермента. Пируваткарбоксилазная реакция является наиболее важной анаплеротической реакцией, особенно в печени и почках (к анаплеротическим относятся возмещающие, дополняющие, реакции). Так, пируваткарбоксилаза восполняет запас оксалоацетата, необходимого для функционирования цикла Кребса. Также пируваткарбоксилаза является важным митохондриальным ферментом глюконеогенеза (новообразования глюкозы). - Ацетил-СоА-карбоксилазы – первого фермента в реакциях биосинтеза жирных кислот. При ферментативном катализе карбоксильная группа бикарбоната передается на ацетил-СоА с образованием малонил-СоА; - Пропионил-СоА-карбоксилазы – фермента, участвующего в окислении жирных кислот с нечетным числом атомов углерода. При этом происходит стереоспецифический перенос активированной карбоксильной группы от карбоксибиотина к пропионил-СоА с образованием метилмалонил-КоА. Следует отметить, что ион бикарбоната может утилизироваться клеткой без участия биотина, как, например, это имеет место в карбомоилфосфатсинтетазной реакции, зависящей от карбомоилфосфатсинтетазы II при синтезе пиримидинов; - b-метилкротоноил-СоА-карбоксилазы – фермента, принимающего участие в реакциях окислительного распада лейцина. - Метилмалонил-оксалацетат-транскарбоксилазы – фермента, ката-лизирующего реакцию транскарбоксилирования, а именно, обратимое превращение пирувата и оксалацетата (другие транскарбоксилазные реакции также протекают с участием биотина).
Витамин Р (биофлавоноиды) (капилляроукрепляющий)
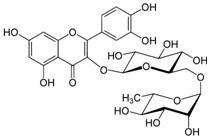
В основе строения соединений Р-витаминного действия – биофлавоноидов, представляющих собой разнообразную группу растительных полифенольных соединений – лежит ядро фенилхромана – флавана.
|
||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 428. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |