Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Принципы классификации инфекционных заболеваний и их отличительные черты.Инфекционное заболевание-крайняя степень проявления инфекционного процесса, когда образуется патологический очаг и появляется специфическая клиническая симптоматика. Т.е. инфекционная болезнь и инфекция-это разные вещи.  41. Природная и приобретенная устойчивость к антибактериальным препаратам. 2)Приобретенная устойчивость-способность отдельных штаммов микроорганизмов выживать при концентрациях антибиотиках, способных ингибировать основную часть микробной популяции данного вида. То есть здесь основной механизм-не отсутствие, а изменение мишени в результате мутаций, модификаций, рекомбинаций. Обусловлена эта устойчивость изменением генома микробной клетки в результате мутаций или связана с получением новой генетической информации в результате конъюгации (передача генетического материала в результате полового процесса у микроорганизмов), трансдукции (передача генетического материала с помощью фагов) или трансформации (непосредственная передача фрагмента ДНК донора реципиентной клетке) с последующей селекцией устойчивых штаммов возбудителей. Этот термин применяют в том случае, когда в чувствительной к определенному химиопрепарату популяции микроорганизмов обнаруживают устойчивые штаммы. 42. Противогрибковые препараты. Противогрибковые препараты — это лекарственные средства, которые обладают фунгицидным (уничтожение грибкового возбудителя) и фунгистатическим (подавление размножения грибкового возбудителя) действием и применяются для профилактики и лечения грибковых заболеваний (микозов). Противогрибковые средства различаются по следующим параметрам: — По происхождению противогрибковых препаратов: природные или синтетические — По спектру и механизму действия — По противогрибковому эффекту: фунгицидные и фунгистатические — По показаниям к применению: для лечения местных или системных грибковых заболеваний — По способу приема: для приема внутрь, для парентерального введения, для наружного применения По химической структуре противогрибковые препараты подразделяются: Классификация противогрибковых препаратов по показаниям к применению Полный перечень противогрибковых препаратов по международным и торговым наименованиям: — АСД фракция 3 — Аморалфин (Лоцерил) — Бифоназол (Бифосин, Микоспор) — Бутоконазол (Гинофорт) — Вориконазол (Вифенд) — Гризеофульвин (Фульцин) — Изоконазол (Гино-Травоген, Травоген) — Итраконазол (Ирунин, Итразол, Итраконазол, Итрамикол, Кандитрал, Миконихол, Орунгал, Орунгамин, Орунит, Текназол) — Клотримазол (Амиклон, Антифунгол, Гине-Лотримин, Имидил, Йенамазол, Кандибене, Кандид, Кандид-В6, Кандизол, Канестен, Канизон, Кломегель, Лотримин, Фактодин) — Каспофунгин (Кансидас) — Кетоконазол (Кето-Плюс, Кетоконазол-Альтфарм, Ливарол, Микозорал, Микокет, Низорал, Ороназол, Перхотал, Румикоз, Себозол, Фунгинок, Фунгистаб) — Леворин (Леворидон) — Микозидин — Миконазол (Гинезол 7, Гино-Дактанол, Гино-Дактарин, Дактанол, Дактарин, Клион-Д 100, Микозон, Нео-Пенотран) — Микафунгин (Микамин) — Натамицин (Пимафуцин) — Нафтифин (Экзодерил) — Нистатин — Оксиконазол (Мифунгар) — Омоконазол (Микогал) — Позаконазол (Ноксафил) — Сертаканазол (Залаин) — Сангвинарина гидросульфат + Хемритрина гидросульфат (Сангвиритрин) — Сафоцид — Тербинафин (Атифин, Бинафин, Ламизил, Ламикан, Ламитель, Миконорм, Микотербин, Онихон, Тербизед, Тербизил, Тербикс, Тербинокс, Тербифин, Термикон, Фунготербин, Цидокан, Экзитер, Экзифин) — Тиоконазол (Гино-Трозид, Трозид) — Ундециленовая кислота (Микосептин) — Фентиконазол (Ломексин) — Флуконазол (Дифлазон, Дифлюзол, Дифлюкан, Медофлюкон, Микомакс, Микосист, Микофлюкан, Нофунг, Проканазол, Флукозан, Флукозид, Флукомабол, Флукомицид, Флуконорм, Флукорал, Флюкостат, Форкан, Фунголон, Цискан) — Флуцитозин (Анкотил, Анмарин) — Фукорцин — Хлорнитрофенол (Нитрофунгин) — Циклопирокс (Батрафен, Дафнеджин) — Эконазол (Ифенек, Гино-Поварил, Экалин, Экодакс) 43. Различия в строении микроорганизмов прокариот и эукариот. Прокариоты не имеют окруженного мембраной ядра. ДНК в виде замкнутой в кольцо молекулы свободно располагается в цитоплазме. Эта «бактериальная хромосома» содержит всю необходимую для размножения клетки информацию. Кроме того, в прокариотической клетке могут содержаться очень небольшие кольцевые молекулы ДНК-плазмиды; без них, однако, клетка может обойтись. Прокариотическая клетка органелл не содержит; подразделение клетки на компартменты менее выражено, чем у эукариот. Рибосомы меньше (70S). У прокариот рибосомы, ферменты белкового синтеза и состав клеточной стенки имеют ряд особенностей, благодаря которым на клетку могут специфически воздействовать многие антибиотики. Прокариоты морфологически относительно слабо дифференцированы, поэтому среди них можно различить лишь ограниченное число форм. В основном это либо сферические формы, либо прямые и изогнутые палочки. С таким внешним «единообразием» удивительно контрастирует чрезвычайное многообразие и пластичность метаболических процессов. В то время как эукариоты нуждаются в молекулярном кислороде, многие группы прокариот способны жить без доступа воздуха (в анаэробных условиях), получая необходимую для роста энергию в результате брожения или анаэробного дыхания. Другие группы прокариот обладают способностью использовать энергию света и строят нужные им вещества либо из органических соединений, либо из углекислоты (двуокиси углерода). Некоторые бактерии могут получать энергию путем окисления различных неорганических соединений или элементов. Среди бактерий широко распространена также способность к фиксации молекулярного азота. 44. Реакция агглютинации. Компоненты, механизм, способы постановки. Применение. РА используют для: определения возбудителя, выделенного от больного животного; Определения антител в сыворотке крови больного животного а)Агглютинация с О-диагностикумом (бактерии, убитые нагреванием, сохранившие O- антиген) происходит в виде мелкозернистой агглютинации.
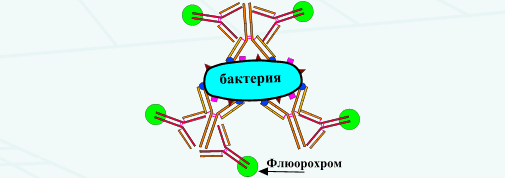
45. Реакция иммунофлюоресценции. Механизм, типы, компоненты, применение для индикации антигенов и серодиагностики. В РИФ люминесценция проявляется в виде флуоресценции — это свечение, возникающее в момент облучения возбуждающим светом и прекращающееся сразу после его окончания. Многие вещества и живые микроорганизмы обладают собственной флуоресценцией (так называемой первичной), однако интенсивность ее очень мала. Вещества, обладающие интенсивной первичной флуоресценцией и используемые для придания флуоресцирующих свойств нефлуоресцирующим веществам, получили название флуорохромы. Такая наведенная флуоресценция называется вторичной. Для возбуждения флуоресценции при люминесцентной микроскопии чаще всего используют ультрафиолетовую или сине-фиолетовую часть спектра (длина волны 300—460 нм). Для этих целей в лабораториях имеются люминесцентные микроскопы различных моделей — МЛ-1—МЛ-4, «Люмам». В вирусологической практике применяют два основных метода люминесцентной микроскопии: флуорохромирования и флуоресцирующих антител (или РИФ). Флуорохромирование — это обработка препаратов флуорохромом с целью увеличения силы и контрастности свечения их. Наибольший интерес представляет флуорохром акридиновый оранжевый, который вызывает полихроматическую флуоресценцию нуклеиновых кислот. Так, при обработке препаратов этим флуорохромом дезоксирибонуклеиновая кислота ярко флуоресцирует зеленым цветом, а рибонуклеиновая — рубиново-красным. Метод РИФ заключается в том, что антитела, соединенные с флуорохромом, сохраняют способность вступать в специфическую связь с гомологичным антигеном. Образующийся комплекс антиген + антитело в связи с присутствием в нем флуорохрома обнаруживают под люминесцентным микроскопом по характерному свечению. Для получения антител используют высокоактивные гипериммунные сыворотки, из которых выделяют антитела и метят их флуорохромом. В качестве флуорохрома наиболее часто используют ФИТЦ-флуоресцеин изотиоционат (зеленое свечение) и РСХ-родамин сульфохлорид (красное свечение). Антитела, меченные флуорохромом, называют конъюгатом. Методика приготовления и окрашивания препаратов заключается в следующем:
Параллельно готовят и окрашивают препараты от здорового животного — контроль. Различают два основных метода применения флуоресцирующих антител: прямой и непрямой. Прямой метод (одноступенчатый). На фиксированный препарат наносят конъюгат (флуоресцирующую сыворотку к предполагаемому вирусу), выдерживают 30 мин при температуре 37 °С во влажной камере. Затем препарат отмывают от несвязанного конъюгата физиологическим раствором (pH 7,2 — 7,5), подсушивают на воздухе, наносят нефлуоресцирующее масло и исследуют под микроскопом. Прямой метод позволяет обнаружить и идентифицировать антиген. Для этого нужно иметь на каждый вирус флуоресцирующую сыворотку. Непрямой метод (двухступенчатый). На фиксированный препарат наносят немеченую сыворотку, содержащую антитела к предполагаемому вирусу, выдерживают 30 мин при 37 °С, отмывают несвязанные антитела. На препарат наносят флуоресцирующую антивидовую сыворотку, соответствующую виду животного — продуцента гомологичных противовирусных антител, выдерживают 30 мин при 37 °С. Затем препарат отмывают от несвязанных меченых антител, подсушивают на воздухе, наносят нефлуоресцирующее масло и исследуют под люминесцентным микроскопом. Антивидовые сыворотки получают, иммунизируя глобулинами животных тех видов, которые служат продуцентами антивирусных антител. Так, если антивирусные антитела получали на кроликах, то используют флуоресцирующую антикроличью сыворотку. Непрямой метод позволяет не только обнаружить и идентифицировать антиген, но и выявить и определить титр антител. Кроме того, этим методом можно обнаруживать одной меченой сывороткой антигены различных вирусов, так как он основан на использовании антивидовых сывороток. Чаще применяют антикроличьи, антибычьи, антилошадиные сыворотки и сыворотки против глобулинов морской свинки. Разработаны несколько модификаций непрямого метода. Наибольшего внимания заслуживает метод с использованием комплемента. Метод заключается в том, что на фиксированный препарат наносят инактивированную нефлуоресцирующую специфическую сыворотку и комплемент морской свинки, выдерживают 30 мин при 37 °С, промывают, и для выявления комплекса антиген + антитело + комплемент наносят флуоресцирующую антикомплементарную сыворотку, выдерживают 30 мин при 37 °С, промывают, подсушивают на воздухе и исследуют под люминесцентным микроскопом. Достоинства РИФ: высокая специфичность и чувствительность; простота техники постановки; требуется минимальное количество компонентов. Это экспресс-метод диагностики, так как в течение нескольких часов можно получить ответ. К недостаткам можно отнести субъективизм в оценке интенсивности свечения и, к сожалению, иногда флуоресцирующие сыворотки бывают плохого качества. В настоящее время РИФ широко применяют в диагностике вирусных болезней животных. 46. Реакция нейтрализации токсина антитоксином. Механизм. Способы постановки, применение. 47. Реакция преципитации. Механизм, компоненты. Способы постановки. Применение.
48. Роль неспецифической резистентности и иммунитета в развитии инфекции. В основе видового иммунитета лежат различные механизмы естественной неспецифической резистентности. Среди них- кожные покровы и слизистые оболочки, нормальная микробиота организма, фагоцитоз, воспаление, лихорадка, система комплемента, барьерные механизмы лимфоузлов, противомикробные вещества, выделительные системы организма, главная система гистосовместимости. Кожа и слизистые- первая линия защиты против возбудителей. Кроме функции механического (анатомического) барьера кожа обладает бактерицидной активностью. Слизь, лизоцим, желудочный сок, слезная жидкость, слюна, деятельность мерцательного эпителия способствует защите слизистых оболочек. Нормальная микрофлора организма препятствует колонизации организма посторонней микрофлорой (конкуренция за субстраты, различные формы антагонизма, в т.ч. выделение антибиотических веществ, изменение рН и др.). Фагоцитоз и система комплемента- вторая линия защиты организма против микроорганизмов, преодолевших поверхностные барьеры. Клеточные факторы системы видовой резистентности- фагоциты, поглощающие и разрушающие патогенные микроорганизмы и другой генетически чужеродный материал. Представлены полиморфоядерными лейкоцитами или гранулоцитами- нейтрофилами, эозинофилами и базофилами (клетками миелопоэтического ряда), а также моноцитами и тканевыми макрофагами (клетками макрофагально- моноцитарной системы). Стадии фагоцитоза. 1.Активация (усиление энергетического метаболизма). Факторами активации и хемотаксиса являются бактериальные продукды (ЛПС, пептиды), компоненты комплемента (С3 и С5), цитокины и антитела. Адгезия связана с наличием ряда рецепторов на поверхности фагоцитов ( к Fc- фрагментам антител, компонентам комплемента, фибронектину), обеспечивающих прочность рецептор- опосредованных взаимодействий опсонинов, обволакивающих микроорганизмы и ограничивающих их подвижность (антитела, С3в, фибронектин). Фагоциты обладают амебоподобными псевдоподиями. При поглощении образуется фагосома с поглощенным объектом (бактерией), к ней присоединяется и сливается содержащая литические ферменты лизосома, образуется фаголизосома. Возможно три исхода фагоцитоза: Завершенный фагоцитоз- полное переваривание микроорганизмов в клетке- фагоците. Незавершенный фагоцитоз- выживание и даже размножение микроорганизмов в фагоците. Это характерно для факультативных и особенно - облигатных внутриклеточных паразитов. Механизмы персистирования в фагоцитах связаны с блокадой фагосомо- лизосомального слияния (вирус гриппа, микобактерии, токсоплазмы), резистентностью к действию лизосомальных ферментов (гонококки, стафилококки), способностью микробов быстро покидать фагосомы после поглощения и длительно пребывать в цитоплазме (риккетсии). В процессе фагоцитоза происходит “окислительный взрыв” с образованием активных форм кислорода, что обеспечивает бактерицидный эффект. К одной из важнейших функций макрофагов (наряду с хемотаксисом, фагоцитозом, секрецией биологически активных веществ) является переработка (процессинг) антигена и представление его иммунокомпетентным клеткам с участием белков главной системы гистосовместимости (МНС) класса 2. Фагоцитоз- не только уничтожение чужеродного, но и представление антигена для запуска иммунных реакций и секреции медиаторов иммунных и воспалительных реакций. Система макрофагов- центральное звено не только естественной резистентности (видового иммунитета), но и играет важную роль в приобретенном иммунитете, кооперации клеток в иммунном ответе. Воспаление. Многие бактериальные продукты активируют клетки макрофагально- моноцитарной системы и лимфоциты, отвечающие на них выделением биологически активных продуктов- цитокинов, в частности интерлейкинов. Их можно характеризовать как медиаторы клеточных иммунных реакций. В воспалительных реакциях основную роль имеет интерлейкин-1 (ИЛ-1), стимулирующий лихорадку, повышающий проницаемость сосудов и адгезивные свойства эндотелия, активирующий фагоциты. Лихорадка. Повышение температуры тела- защитная реакция организма, ухудшающая условия для размножения многих микроорганизмов, активирует макрофаги, ускоряет кровоток и усиливает обменные процессы в организме. Барьерные функции лимфоузлов. По выражению П.Ф.Здродовского (1969) лимфоузлы- своеобразный биологический фильтр для возбудителей, переносимых с лимфой. Здесь проникшие через кожу или слизистые и занесенные током лимфы микроорганизмы задерживаются и подвергаются действию макрофагов и активированных лимфоцитов. Система комплемента- комплекс белков и гликопротеидов сыворотки крови человека и позвоночных животных (их более 20). Отдельные компоненты опосредуют процессы воспаления, опсонизацию чужеродных фрагментов для последующего фагоцитоза, участвуют наряду с макрофагами в непосредственном уничтожении микроорганизмов и других чужеродных клеток (лизис бактерий и вирусов). В условиях физиологической нормы компоненты системы комплемента находятся в неактивной форме. Известны три пути активации системы комплемента- классический, альтернативный и с использованием С1- шунта. Классический путь- каскад протеазных реакций с компонента С1q до С9, реализуется при наличии антител к соответствующему антигену. С комплексом “антиген- антитела” взаимодействует компонент С1q, затем С4, следом- С2. Образуется комплекс “антиген- антитела-С1С4С2”, с ним соединяется С3 (центральный компонент системы) и запускается цепь активации с эффекторными функциями (опсонизация и лизис бактерий, активация системы макрофагов, воспаление). Альтернативный путь реализуется при первичном контакте с возбудителем (когда еще нет антител). Он индуцируется ЛПС и другими микробными антигенами. С1, С4, С2 не участвуют, альтернативный и классический пути смыкаются на уровне С3. Система интерферонов. Интерфероны- синтезируемые различными клетками организма гликопротеиды широкого спектра биологической активности (прежде всего антивирусной), быстрый ответ организма на получение клетками неспецифического сигнала чужеродности. Существует целая система интерферонов, которые разделены на альфа, бета и гамма подтипы с выраженной гетерогенностью свойств. Противовирусное действие проявляется в способности подавлять внутриклеточное размножение ДНК- и РНК- вирусов (прежде всего в результате блокировки синтеза вирусных макромолекул). Индукцию синтеза интерферонов вызывают вирусы, бактерии, риккетсии, простейшие, синтетические соединения. Киллерные клетки. В обеспечении видового иммунитета существенную роль принадлежит Т- цитотоксическим лимфоцитам (Т- киллерам), а также главной системе гистосовместимости (подробнее- в следующих лекциях). Т- киллеры по представлению антигенов главной системы гистосовместимости класса 1 распознают любые чужеродные антигены (включая мутантные, например- раковые клетки), атакуют и уничтожают их. Клетки NK (naturalkiller- натуральные киллеры) имеют важное значение в поддержании генетического гомеостаза и противоопухолевой защите, их функции распознавания не зависят от представления антигенов МНС (majorhistocompatibilitycomplex) класса 1. Системы неспецифической резистентности и видового иммунитета способствуют поддержанию структурной и функциональной целостности организма и являются основой для формирования приобретенного (специфического) иммунитета. Стыкуясь на этом, более высоком уровне, системы видового и приобретенного иммунитета образуют единую и наиболее эффективную систему самозащиты организма от всего чужеродного. 49. Рост и размножение бактерий в искусственных условиях. Фазы размножения. - экспоненциальная (геометрического роста) фаза с резким ростом численности популяции микроорганизмов (2 в степеии n); - стационарная фаза (фаза равновесия размножения и гибели микробных клеток); - стадия гибели - уменьшение численности популяции в связи с уменьшением и отсутствием условий для размножения микроорганизмов (дефицит питательных веществ, изменение рH, rH2, концентрации ионов и других условий культивирования). Данная динамика характерна для периодических культур с постепенным истощением запаса питательных веществ и накоплением метаболитов. Если в питательной среде создают условия для поддержания микробной популяции в экспоненциальной фазе- это хемостатные (непрерывные) культуры. Характер роста бактерий на плотных и жидких питательных средах: сплошной рост, образование колоний, осадок, пленка, помутнение. Основные принципы получения чистых культур (популяций одного вида микроорганизмов): механическое разобщение, рассев, серийные разведения, использование элективных сред, особых условий культивирования (с учетом устойчивости некоторых микробов к определенным температурам, кислотам, щелочам, парциальному давлению кислорода, рН и мн.др). 50. Серодиагностика инфекционных заболеваний. Принципы и диагностические критерии. В клинической практике чаще всего используется реакция агглютинации (РА) Видаля, ее разновидности, РНГА, РСК и более информативные современные методы (ИФА, РИА, ЛИФА и др.). РА — определение неизвестных антител с помощью известных антигенов и установление вида возбудителя с помощью известных антител. РИГА и РНГА — более специфичны, используются меченные эритроциты. РТГА — основан на способности некоторых вирусов агглютинировать эритроциты. РИ — реакция иммунодиффузии, различная способность антигенов и антител диффундировать в геле. РСК-титрование антигенов или антител по степени фиксации комплемента с комплексом антиген-антитело. PH - способность антител нейтрализовать токсины и антигены вирусов. ИФА — используются антитела, конъюгированные с ферментом. РИА — используется радиоактивная метка антигенов или антител. ЛИФА — лантанидный иммунофлюоресцентный анализ — используются в качестве метки элементы редкоземельных металлов.
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 1116. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |