Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Расчеты к подразделу 1.4.5.Р.14. Рассчитать минимальный расход греющего газа (воздуха) для десорбции воды из цеолита. Адсорбент стабилен при температурах до 650 °С. Прочие условия таковы: h = 1,3 кДж/м3 .К, Н = 5,04.102 кДж/м3 .К, Х*n =1,3.102 кг/м3 , ∆H = 4200 кДж/кг, W = 0,2 м/с. Из-за высокой стабильности цеолитов температуру газа, вводимого на регенерацию, определяют по термостабильности материалов и элементов конструкции. Обычно она не превышает 300-350 °С. Примем, что температура газа равна 320 °С. Тогда ∆Т = 320 – 20 = 300 К. Для определения скорости движения фронта подставим параметры в уравнение (1.32):
Utd = Wh/[H +h + (∆H.X*n/∆T)] = 0,2.1,3/[5,04.102 + 1,3 + (4200.1,3.102/300)] =
= 1,1..10-4м/с.
Определим также минимальное количество газа, которое следует подать при регенерации:
ПВtd= W/Utd = 0,2/1,1.10-4 = 1,8.103 м3 /м3 .
Эта цифра в четыре с половиной раза превышает расход газа на нагрев слоя, не содержащего адсорбат.
Р.15. (Самостоятельная работа) Аналогичные расчеты выполнить для силикагеля, предел термостабильности которого составляет 250 С. Теплоту десорбции воды из силикагеля принять равной 2800 кДж/кг. Сравнить скорости движения фронтов десорбции и минимальные удельные расходы газа на регенерацию силикагеля и цеолита.
1.4.6. Динамика адсорбции смесей
Если коэффициенты распределения компонентов смеси, вычисленные по изотермам индивидуальной адсорбции, различаются на порядок и больше, то вместо динамики адсорбции смеси рассматривают динамику индивидуальной адсорбции целевого компонента. Ошибка, связанная с пренебрежением адсорбцией других компонентов не превышает 10%, что допустимо в технических расчетах. Если компоненты смеси имеют близкие значения коэффициентов распределения (коэффициент разделения близок к единице), то введение поправок на множественность адсорбатов становится необходимым.  Равновесная адсорбция компонентов смеси. Приводим без обоснования упрощенную схему расчета совместной адсорбции нескольких веществ для случая, когда индивидуальная равновесная адсорбция каждого из них описывается выпуклой изотермой адсорбции. Основным уравнением в этой схеме является уравнение Люиса, которое ниже записано для адсорбции бинарной смеси:
(Х12 /Х01) + (Х21 /Х02 ) = 1, (1.34)
где Х12 – величина адсорбции первого компонента смеси при содержании его в объемной фазе С1 в присутствии второго компонента, Х21 – величина адсорбции второго компонента смеси при содержании его в объемной фазе С2 в присутствии первого компонента, Х01 – величина индивидуальной адсорбции первого компонента при содержании его в объемной фазе С = С1 + С2, Х02 – величина индивидуальной адсорбции второго компонента при содержании его в объемной фазе С = С1 + С2. В уравнении (1.34) величины индивидуальной адсорбции предполагаются известными; они определяются из изотерм индивидуальной адсорбции, а определению подлежат величины адсорбции компонентов смеси. (При расчете адсорбции смесей концентрации и емкости выражают не в весовых, а в мольных единицах). Уравнение (1.33) решают совместно с выражением для коэффициента разделения (Кр):
Кр = (Х12/С1)(С2/Х21) (1.35)
Коэффициент разделения слабо зависит от состава, давления и температуры и предполагается известной величиной. Его находят либо из экспериментальных данных, либо вычисляют по эмпирическому уравнению: lgKp = -0,23 + 4,76(1 – φ), где φ – отношение коэффициента аффинности в уравнении ТОЗМ хуже сорбирующегося вещества к коэффициенту аффинности вещества, адсорбирующегося лучше. Для смесей, число компонентов (N) в которых более двух, в уравнение Льюиса включают дополнительные слагаемые, а коэффициенты разделения определяют для всех возможных пар присутствующих компонентов. Если изотермы индивидуальной адсорбции компонентов смеси описываются уравнениями Генри, то адсорбцию каждого из них считают независимой от адсорбции других присутствующих веществ. Это разумное допущение, так как в области Генри степень заполненности адсорбционного пространства невелика (≈ 1% и менее) и адсорбирующиеся вещества не вытесняют друг друга. Динамика адсорбции. При линейных изотермах сорбции, в соответствии с приведенным выше допущением, компоненты смеси сорбируются независимо и фронт каждого из них передвигается по слою со своей характерной скоростью, определяемой уравнением (1.21). Расчет ведут по скорости движения целевого компонента, присутствие которого в очищенном газе не допускается. Для выпуклых изотерм адсорбции модели и решения представлены только для изотермической динамики адсорбции. Математическая модель по форме не отличается от модели (М3), но, конечно, намного сложнее, так как для каждого компонента смеси должны быть записаны все уравнения модели. Отмечается, что прямой расчет невозможен и вычисления проводят путем последовательных приближений. Феноменологию процесса, следуя Дубинину и Явичу, принято рассматривать в квазистационарном приближении. На рис.1.24 приведены кривые распределения концентраций адсорбатов в потоке для двухкомпонентной смеси. На этом рисунке сплошная линия отвечает распределению концентраций лучше сорбирующегося компонента, а пунктирная – компонента, сорбирующегося хуже. Отметим, что фронт хуже сорбирующегося компонента всегда опережает фронт компонента, который адсорбируется лучше. В зоне ОА слой равновесно насыщен обоими компонентами при концентрациях в потоке С01 и С02 , отвечающих их
Рис.1.24.Кривые распределения концентраций в объемной фазе адсорбента для адсорбции бинарной смеси.
содержанию в газе, поступающему на очистку. В зоне АВ происходит падение концентрации компонента 2 из-за его адсорбции. В этой же зоне концентрация хуже сорбирующегося компонента 1 возрастает до значения С’01 > C01. Рост концентрации связан с вытеснением компонента 1 компонентом 2 в зоне АВ. Зона ВС насыщена первым компонентом, а его адсорбция происходит в зоне СД.
Рис.1.25. Кривые распределения концентраций в фазе адсорбента при адсорбции бинарной смеси компонентов.
На рис.1.25 изображены кривые распределения концентраций в фазе адсорбента. Из сопоставления рис.1.24 и рис.1.25 видно, что адсорбция первого, хуже сорбирующегося компонента, определяется его свойствами, вытекающими из индивидуальной изотермы адсорбции этого вещества. Единственное, хотя и очень существенное отличие от индивидуальной адсорбции, состоит в том, что эти свойства соответствуют не концентрации С01, в которой этот компонент присутствует в потоке, а концентрации С’01, превышающей исходную на величину ∆С = С’01 – С01 из-за вытеснения первого компонента вторым в зоне 0А. Адсорбция второго компонента определяется свойствами, которые определяются совместной адсорбцией второго и первого компонентов. Обычно концентрация вещества в объемной фазе значительно меньше величины адсорбции. Поэтому для квазистационарного перемещения фронтов можно записать: U1= WC’01/X’1(C’01 ) (1.36)
U2 = WC2 /X21 (1.37)
В этих уравнениях U1 и U2 – скорости движения первого и второго фронтов адсорбции. Скорость движения фронта вытеснения первого компонента из зоны сорбции второго, очевидно, равна скорости движения фронта сорбции второго компонента. Поэтому можно записать:
U2 = WС 2/Х21 = W(С’1 – С01 )/(Х′01 (С’01 ) – Х12) (1.38)
Совместное решение уравнения (1.38) и уравнения изотермы индивидуальной адсорбции первого компонента позволяет определить концентрацию этого компонента в объемной фазе и равновесную ей величину его адсорбции. После этого находятся скорость движения фронта первого компонента. Предельная возможность слоя определяется тем, какой из компонентов смеси является целевым. Если это первый компонент смеси, то ее вычисляют из уравнений (1.23) и (1.36). Если второй – из уравнений (1.23) и (1.37).
Расчеты к подразделу 1.4.6
Р.16. Рассчитать равновесную адсорбцию пропана и бутана на цеолите NаХ в следующих условиях: содержание пропана 0,28, бутана 0,065 об.%, метан (условно неадсорбирующийся компонент) – остальное. Общее давление смеси 1,7 ата. 1.Определим парциальные давления адсорбирующихся компонентов смеси. Для пропана имеем: Р1 = 0,28.10-2 .1,7.760 = 3,62 мм рт.ст.. То же для бутана: Р2 = 0,065.10-2. 1,7.760 = 0,84 мм рт.ст. Суммарное давление адсорбирующихся компонентов: 3,62 + 0.84 = 4,46 мм рт.ст. 2.Определим величины индивидуальной адсорбции пропана и бутана на цеолите при Р = 4,46 мм рт. ст. Обширная информация об адсорбции на цеолитах содержится в монографии Д.Брек, Цеолитовые молекулярные сита, 1976, М., «Мир». Она приведена для кристаллических цеолитов. Для гранулированных цеолитов с учетом потери активности при грануляции и старения следует принимать значения примерно в два раза более низкие, чем указано в монографии. После введения поправок имеем: Х01 = 0,024 г/г = 0,024.1000/44 = 0,54 ммоль/г Х02 = 0,064 г/г = 0.064.1000/56 = 1,14 ммоль/г. Из этих цифр следует, что в смеси пропана и бутана лучше адсорбирующимся компонентом является бутан. 3.Запишем уравнение Люиса: (Х12 /Х01) + (Х21/Х02) = (Х12/0,54) + (Х21/1,14) = 1. 4.Определим коэффициент разделения по уравнению (1.35). Входящие в него коэффициенты аффинности вычисляются по отношению парахоров, но известны также их экспериментальные значения (см.Н.В.Кельцев. Основы адсорбционной техники. М., 1984). Для пропана и бутана они равны 2,27 и 2,90.
lg Кр = -0,23 +4,76 (1 – β пропан / β бутан ) = -0,23 + 4,76 (1 – 2,27/2,90); Кр = 6,3.
5.Запишем уравнение (1.34) в явном виде.
Кр = 6,3 = (Х21/С2)(С1/Х12) = (Х21/0,84) (3,62/Х12)
Х21 /Х12 = 6,3.0,84/3,62 = 1,46.
6.Решим совместно два уравнения и определим величины адсорбции пропана и бутана из их бинарной смеси:
(Х12/0,54) + (Х21/1,14) = 1
Х21/Х12 = 1,46.
Х12=0,32 ммоль/г, Х21 0,47 ммоль/г.
Р.17. В условиях примера Р.16 рассчитать скорости движения фронтов сорбции пропана и бутана при скорости потока 0,2 м/с. При расчете принять, что адсорбция пропана происходит на участке изотермы, который отвечает полной насыщенности адсорбента по этому веществу. Это допущение означает, что изменение концентрации пропана в газовой фазе не изменяет его величину адсорбции. 1.Концентрация бутана, равная 0,065 %, отвечает следующему его содержанию в газовой фазе:
С2 = 0,065.10-2.106 /22,4 = 29 ммоль/м3
Величина адсорбции бутана из смеси, равная 0,47 ммоль/г, в другой размерности составляет:
Х21 = 0,47.500.103 = 2,35.105 ммоль/м3.
В этом уравнении 500 г/л – насыпная плотность адсорбента. 2.По уравнению (1.37) найдем скорость движения фронта сорбции бутана:
U2 =WC2/X21 = 0,2.29/2,35.105 = 2,47.10-5 м/с.
3.Концентрация пропана в газовой фазе, равная 0,28 %, отвечает следующему его содержанию в газовой фазе:
С1 =0,28.10-2.106/22,4 = 125 ммоль/м3.
Согласно допущению, сделанному в условиях задачи, величина адсорбции пропана не зависит от его содержания в потоке и равна Х1 = Х01(С’01) = 0,46 моль/г, или
Х1 = 0,46.500.103 = 2,3. 105 моль/м3.
Пересчет величины сорбции пропана из смеси с бутаном в нужную размерность дает:
Х12= 0, 32 ммоль/г = 1,6.105 моль/м3.
4.По уравнению (1.38) определим исправленную концентрацию пропана С’01. В преобразованном виде уравнение (1.38) записывается так:
C’01 = C1 + U2(X01(C’01) – X12)/W = 125 + 2,47.10-5(2,3 – 1,6).105/0,2 = 133,6 ммоль/м3.
5.По уравнению (1.36) найдем скорость движения фронта сорбции пропана:
U1 = WC’01/X’01 (C’01) = 0,2.133,6/2,3.105 =1,16.10-4 м/с.
Фронт адсорбции пропана опережает фронт адсорбции бутана.
Р.18 На очистку от сероводорода поступает природный газ следующего состава: пропан 0,20; диоксид углерода 0,08; бутан 0,06; сероводород 0,005 % (остальное метан). Прочие условия см. в примерах Р.16 и Р.17.Рассчитать максимальное количество газа, которое может быть очищено 1 м3 цеолита. 1.Упростим состав смеси. Согласно литературным данным, коэффициент разделения в системе бутан-сероводород-цеолит очень близок к единице. Это означает, что эти вещества адсорбируются практически одинаково. Коэффициент разделения в системе пропан-диоксид углерода-цеолит невелик (~3,5) и эти вещества адсорбируются почти одинаково. Таким образом, вместо пятикомпонентной смеси можно условно рассматривать адсорбцию трехкомпонентной смеси состава: «пропан» 0.28, «бутан» 0,065 %, остальное метан. 2.Определим максимальную возможность слоя цеолита по «бутану». Все составляющие приведены в примере Р.17 для бутана (без кавычек).
ПВс = W/U2 =0,2/2,47.10-5 = 8,1.103 м3/м3.
Эта же возможность характерна для удаления сероводорода.
2.Технология адсорбционных процессов 2.1.Краткая историческая справка
Свойство твердых тел, в первую очередь древесных углей и природных глин, очищать, осветлять, обезвреживать жидкости известна с глубокой древности. Это факты история применения адсорбентов. История же адсорбции – технологического процесса значительно короче. Началом ее следует считать 1806 г., когда наполеоновская Франция приняла Эдикт о континентальной блокаде, согласно которому на территорию Европы было прекращено поступление товаров из Великобритании и британских колоний. В число запрещенных к ввозу продуктов попал тростниковый сахар. Во Франции приступили к выращиванию сахарной свеклы и производству свекловичного сахара. По внешнему виду и вкусу он сильно уступал сахару, изготовленному из тростника. Тогда и вспомнили об открытии русского фармацевта (впоследствии академика) Товия Ловица, сделанном им за 9 лет до этого. Ловиц установил, что измельченный и предварительно прокаленный уголь из древисины является эффективным средством облагораживания вина. Такое же благоприятное действие подготовленный уголь оказывал на сахарные сиропы. Сахароварение – достаточно тонкий процесс и предназначенный для него адсорбент должен обладать определенной совокупностью свойств. В то же время, сахароварение было и продолжает оставаться крупнотоннажным производством. Не удивительно, что именно для сахарного производства был разработан специальный адсорбент – костяной уголь. Он был получен в ходе обжига костей животных и рыб. Костяной уголь дороже древесного и его стремились использовать многократно. Так в практику адсорбционных процессов вошли операции по восстановлению поглотительных свойств адсорбента, утраченных в ходе предшествующего применения. Вслед за рафинированием сахарных сиропов в промышленности стали применяться другие процессы очистки жидких сред: пищевых масел и жиров, растворов химических реактивов и лекарственных препаратов, спирта и спиртовых напитков, вина, соков, питьевой воды и др. Эти процессы широко представлены в современной промышленности. Они основываются на применении современных адсорбентов, в первую очередь, активных углей, основы получения которых в самом начале ХХ века разработал германский углехимик Острейко. Все перечисленные выше процессы относятся к очистке жидких сред и осуществляются в аппаратах емкостного типа. Процессы очистки газов возникли в 1915 г. Их появление связано с именем крупного русского ученого Зелинского. Адсорбция и адсорбенты не были предметом его предшествующей деятельности и обратиться к ним Зелинского заставили события первой мировой войны. Вначале на реке Ипр против французских и английских войск, а затем на реке Равка против русских армий германские войска применили отравляющие вещества. Возникла срочная потребность в создании средств защиты. Оно было предложено Зелинским и включало два определяющих элемента: активный уголь в качестве средства очистки воздуха и фильтрующий (неподвижный) слой как способ конструктивного оформления процесса очистки. За прошедшие годы многое изменилось в конструкции противогазов, но эти два элемента так и остались неизменными. В том же 1915 г появился первый технологический адсорбционный процесс. Испытывая острую нужду в моторном топливе, немцы построили установку для извлечения углеводородов из газов прикарпатского газоконденсатного месторождения. Она явилась родоначальником огромного множества рекуперационных установок, используемых в современной промышленности. В начале 20-х годов американец Люис синтезировал адсорбент нового класса – первый синтетический минеральный адсорбент - силикагель. (До открытия Люиса в технике очистки жидких сред применялись природные минеральные адсорбенты – глины). А не позднее начала 30-х годов в промышленную практику вошли процессы осушки газов на его основе. Это было третье после очистки жидких сред и рекуперации углеводородов крупное приложение адсорбционных процессов. Переломными для промышленной адсорбции явились 50-ые годы 20-го века. В самом начале их американская фирма «Линде» (подразделение «Юнион Карбайт»), воплотив разработки англичанина Баррера и американца Брека, осуществила промышленный синтез цеолитов. С ними в практику адсорбции вошло разделение веществ, отличающихся по распределению зарядов и размерам молекул. В середине 50-х г.г. группа американских инженеров под руководством Берга разработала и реализовала непрерывный процесс разделения углеводородов в движущемся слое адсорбента, получивший название «Гиперсорбции». А в конце рассматриваемого периода Скарстром (США) предложил безнагревную технику адсорбционной очистки газов. Свое полное развитие она получила в 70 - 80 г.г., когда на ее основе, в дополнение к методам очистки газов, были созданы процессы их разделения. С начала 60-х г.г. углеродные адсорбенты стали широко применяться в процессах водоподготовки – для очистки воды питьевого назначения. Это направление использования активных углей по масштабам применения угля в настоящее время является главенствующим. С середины 90-х г.г., благодаря работам Мухина (Россия), начались исследования по адсорбционной детоксикации почв – удалению из них внесенных в ходе сельскохозяйственной деятельности токсичных веществ. Сегодня адсорбенты и адсорбционные процессы применяются во всех отраслях промышленности. Они вышли из сферы индустрии и используются в сельском хозяйстве, в медицине, в военном деле, в быту – везде, где есть потребность в очистке или разделении сред.
2.2..Конструктивные схемы адсорберов и типы адсорбционных процессов
2.2.1.Конструкции адсорберов
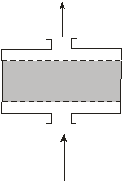
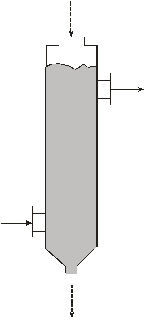
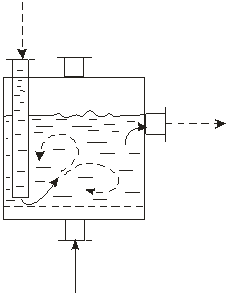
Подавляющее большинство адсорбционных процессов осуществляют в адсорберах двух типов. Первый из них – цилиндрический аппарат, загруженный гранулами адсорбента. Через слой гранул пропускают очищаемый (разделяемый) поток. Через этот же слой в направлении, как правило, противоположном направлению движения потока при очистке, пропускают поток тепло(хладо) агента, с помощью которого осуществляют восстановление утраченных при очистке поглотительных свойств сорбента. В ориентации на этот тип адсорбера в разделе 1.4. были рассмотрены основные особенности тепломассообмена. Аппарат такого типа называют адсорбером с неподвижным слоем зернистого адсорбента. Различают два вида аппаратов с неподвижным зернистым слоем: аксиальный и радиальный. В первом из них потоки двигаются параллельно оси аппарата, во втором – перпендикулярно ей. Аксиальный адсорбер с неподвижным слоем адсорбента называют вертикальным, если отношение L/D, где L – высота слоя адсорбента, D – диаметр аппарата, больше единицы. Если это отношение равно или меньше единицы, аппарат называют горизонтальным. На рис.2.1 а и б приведены конструктивные схемы аксиальных адсорберов. Вертикальный аппарат из-за более равномерного распределения потока по сечению обеспечивает более высокую степень очистки, но он обладает сравнительно высоким гидравлическим сопротивлением. В горизонтальном адсорбере сопротивление невелико, но распределение потока по сечению часто неудовлетворительное и степень очистки сравнительно невелика. Радиальный адсорбер (см. рис. 2.1. в) можно рассматривать как вариант горизонтального аппарата с улучшенным распределением потока. Если подвод (отвод) тепла осуществляют через «стенку», то возникает следующая разновидность адсорбера с неподвижным зернистым слоем – адсорбер-теплообменник. Его конструктивная схема приведена на рис.2.1 г. Наконец, зернистый слой может быть приведен в медленное движение в направлении сверху-вниз – навстречу очищаемому потоку. Такой аппарат носит название адсорбера с движущимся слоем зернистого адсорбента. Аппараты такой конструкции применяют тогда, когда необходима частая выгрузка адсорбента, например, из-за его дезактивации. Конструктивная схема адсорбера этого типа приведена на рис.2.1 д. Все аппараты с неподвижными и движущимися слоями адсорбента работают в режиме, близком к режиму идеального вытеснению потока. Этой своей особенностью они обязаны небольшим размерам гранул адсорбента, создающим глубокое секционирование слоя. Второй распространенный тип адсорбера – это емкость с мешалкой, в которую загружен гранулированный, дробленный или порошкообразный адсорбент. Аппараты этого типа будем называть емкостными адсорберами (см. рис 2.1 е.). В них реализуется режим, близкий к режиму идеального смешения. В адсорбере с псевдоожиженным слоем адсорбента (см.рис.2.1 ж) реализуется режим идеального смешения по газу и идеального вытеснения по твердой фазе. Аппараты этого типа применяют при очень больших (105 – 106 м3/ч) расходах очищаемого газового потока.
а б в г д е ж
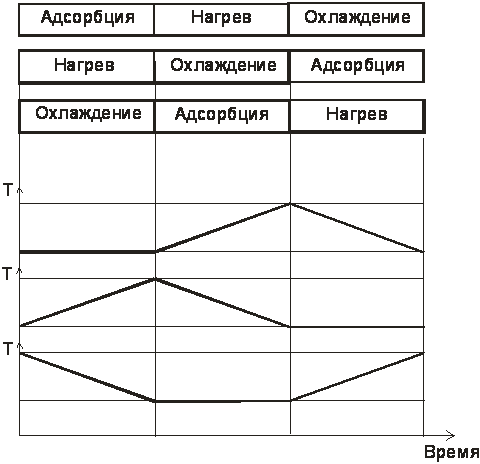
Рис.2.1..Конструктивные схемы адсорберов: а – вертикальный адсорбер с неподвижным слоем адсорбента, б – горизонтальный адсорбер, в – радиальный адсорбер, г – адсорбер-теплообменник, д – адсорбер с движущимся слоем адсорбента, е – адсорбер емкостного типа, ж – адсорбер с псевдоожиженным слоем адсорбента; сплошные линии – направление движения потока, пунктирные – направление движения адсорбента (если оно имеет место). Сопоставим возможности двух основных адсорберов: аппарата с неподвижным зернистым слоем и емкостного адсорбера. Для первого из них будем использовать выражение для предельной возможности ПВс, которое было записано в первой части в виде уравнения (1.23): ПВc= W/Uc = (X*0 + Co )/Co (1.23) Материальный баланс адсорбата в непроточном емкостном адсорбере идеального смешения записывается так: Va ∂C/∂t + G∂X/∂t = 0 (2.1) где Vа- объем жидкой фазы в адсорбере, G – объем адсорбента. Уравнение решается при начальном условии: t = 0, С = Со, Х = 0 и преобразуется к виду: Va (Co – C) = GX*(C) Va/G = X*(C)/(Co –C) (2.2) Для проточного адсорбера идеального смешения в уравнение (2.2) следует подставлять расходы жидкости и адсорбента. Уравнения (1.23) и (2.2) в сущности говорят об одном и том же: они определяют объем жидкости, очищаемый единичным объемом адсорбента. Следовательно, на основе этих уравнений можно сопоставлять адсорберы, которым они отвечают. Количество адсорбента, расходуемого для очистки единицы потока обратно пропорционально предельной возможности (уравнение 1.23) или норме расхода жидкой фазы (левая часть уравнения (2.2)). Следовательно, отношение расхода сорбента в адсорбере неподвижного слоя к расходу его в емкостном аппарате равно: M = Va/(G.ПВc ) = X*(C).Co/[(Co – C).(X*o +Co)] = X*(C)/X*o (2.3) где M – отношение расходов адсорбента в адсорберах рассматриваемых типов. Конечная форма уравнения получена в предположении, что Сo >> C, X*o >> Cо. Эти допущения обычно выполняются. Очевидно, что Х*(С)< X*o и относительный расход адсорбента в неподвижном слое меньше, чем в емкостном адсорбере. Адсорбер с неподвижным слоем является более интенсивным типом аппарата в сравнении с адсорбером емкостным. В уравнение (1.23) конечная величина адсорбции и конечная концентрация адсорбата в объемной фазе не входят. Это означает, что глубина очистки в неподвижном слое в идеальной ситуации, которой отвечает уравнение (1.23), неограниченно высока (С→0). В аппарате емкостного типа С≠0, что отвечает меньшей эффективности аппарата. Таким образом, адсорбер с неподвижным слоем адсорбента по всем показателям является более совершенным аппаратом, чем емкостной адсорбер. Возникает вопрос, почему же емкостные аппараты продолжают применяться в промышленности? Ответ на этот вопрос лежит в том факте, что в емкостных аппаратах легче организовать непрерывный процесс. Оба компонента могут постоянно поступать в емкость и постоянно выводиться из нее. В неподвижном слое операции ввода-вывода адсорбента решаются более сложно. Наше сопоставление можно резюмировать так: емкостные аппараты применяют для грубой очистки жидких сред, аппараты с неподвижным слоем – для тонкой очистки и жидкостей, и газов. Расчет к подразделу 2.2.1 Р.19. В некоторой системе жидкость – адсорбат - адсорбент адсорбционное равновесие описывается степенным уравнением Х = АСВ, где А и В = 0,3 – коэффициенты. Определить отношение расходов адсорбента в адсорбере с неподвижным слоем и адсорбере-емкости. Остаточное содержание адсорбата в жидкости для второго аппарата принять равным С = 0,05Со. Используем уравнение (2.3): М = Х*(С)/Х*о = С0,3/Со0,3= 0.050,3= 0,37. Расход адсорбента в первом из аппаратов примерно в 3 раза ниже, чем во втором. 2.2.2. Типы процессов Емкость адсорбента – величина конечная и после переработки некоторого количества потока адсорбент надо заменить или восстановить его поглотительные свойства. Процессы, в которых адсорбент заменяют, называют процессами с однократно используемым адсорбентом. Процессы, в которых поглотительные свойства адсорбента восстанавливают, - это процессы с адсорбентом, используемым многократно. Восстановление утраченных поглотительных свойств часто можно осуществить в том же аппарате, в котором происходила переработка потока. В этом случае операции восстановления носят название регенерации адсорбента. Если же для восстановления свойств адсорбент выгружают из адсорбера и обрабатывают в некотором другом аппарате, то такие операции называют реактивацией адсорбента. Оба метода восстановления свойств, как правило, (хотя и не исключительно) основаны на нагреве адсорбента. При нагреве парциальное давление адсорбата над адсорбентом возрастает, адсорбат переходит в газовую фазу и потоком отдувочного газа может быть вынесен за пределы аппарата. Выбор метода восстановления определяется, таким образом, температурой, которая обеспечит достаточно полную десорбцию поглощенных веществ. Она, в свою очередь, зависит от их физических свойств. Есть некоторый эмпирический критерий, который говорит о возможности или, наоборот, о невозможности регенерации. Это нормальная температура кипения. Если для некоторого адсорбата она ниже 180 – 190 оС, то регенерация возможна. Если выше, то следует прибегнуть к реактивации. В значении этого критерия учтена ограниченная термическая стабильность конструктивных материалов, из которых изготовлен корпус адсорбера, и арматуры, используемой для управления адсорбционным процессом. Для адсорберов, изготовленных из углеродистой стали, арматуры обычного качества предел термостабильности не превышает 350 – 400 оС. Итак, в ходе регенерации адсорбент был нагрет. Его непосредственное применение для очистки потока невозможно и регенерацию продолжают, охлаждая адсорбент до температуры адсорбции. Регенерация в рассматриваемом примере состоит из двух стадий: нагрева (десорбции) и охлаждения, а сам процесс из трех непрерывно сменяющихся и воспроизводящихся стадий: адсорбция (очистка, разделение) – нагрев – охлаждение и снова адсорбция – и т.д. Из-за повторяемости стадий процессы с регенерируемым адсорбентом часто называют циклическими. Существуют очень сложные адсорбционные циклы, с большим числом стадий и их сложным чередованием во времени. Чтобы дать наглядное представление об адсорбционном цикле, используют так называемые циклограммы процессов.Так называют графическую запись чередования стадий в каждом адсорбере адсорбционной установки во времени. Используют две системы представления циклограммы. В одной из них над осью абсцисс – осью времени надписывают названия чередующихся стадий. В другой системе показывают символические изменения некоторого характерного параметра процесса во времени. Оба вида циклограмм приведены на рис.2.2 для трехстадийного процесса: адсорбция – нагрев – охлаждение, осуществляемого в трехадсорберной установке.
Рис.2.2. Циклограммы (характерный параметр – температура) Различают два вида циклических процессов: с циклически изменяющимся температурой и с циклически изменяющимся давлением. Первый из них часто обозначат аббревиатурой TSA – Thermal Swing Adsorption, второй - PSA – Pressure Swing Adsorption. Число адсорберов в циклических процессах всех типов определяют по уравнению: N = ∑τi / τа (2.4) Здесь: N – количество адсорберов, τi – продолжительность i – ой стадии (например, адсорбции, нагрева или охлаждения), τа - продолжительность стадии адсорбции. Уравнение (2.4) – это требование, согласно которому процесс очистки должен осуществляться непрерывно. Для циклограммы, пример которой был приведен выше, число адсорберов, очевидно равно трем. В зависимости от типа теплоносителя и способа ввод тепла процессы ТSA классифицируют как процессы с прямым вводом тепла с теплоносителем – газом, то же с теплоносителем – паром и процессы с косвенным вводом тепла (вводом через стенку). В последнем случае вид теплоносителя не существенен. Процессы PSA не принято подразделять на более мелкие группы. Реактивацию, которую, как уже указывалось, проводят вне адсорбера, классифицируют по способу выгрузки адсорбента. Эту операцию можно проводить периодически, когда весь находящийся в аппарате адсорбент утратит свою поглотительную способность, или непрерывно. Процессы, отвечающие этим способам, соответственно называют периодическим и непрерывным Классификационная таблица процессов приведена на рис 2.3. Тип процесса обусловлен его назначением (очистка потока, его разделение, извлечение или концентрирование адсорбата) и свойствами системы. Между типом процесса и типом аппарата имеется определенное соответствие. В вертикальных адсорберах с неподвижным слоем осуществляют процессы с прямым вводом тепла газом и безнагревные процессы, в горизонтальных и радиальных адсорберах – процессы, в которых ввод тепла осуществляют с помощью пара. Для процессов с косвенным нагревом, очевидно, пригоден только адсорбер-теплообменник. Непрерывные процессы проводят в адсорберах с движущимся или псевдоожиженным слоями адсорбента и в емкостных адсорберах. Периодические процессы – и в аппаратах с неподвижным слоем, и в емкостных адсорберах. 2.3.Процессы с однократно используемым адсорбентом Это самый старый тип процессов; именно так осуществляли очистку сахарных сиропов в емкостных адсорберах дешевым адсорбентом – древесным углем. С переходом на более качественные и, следовательно, более дорогие адсорбенты – активные угли очистка сиропов стала процессом с многократно используемым адсорбентом. Но имеется огромное множество современных процессов, в которых адсорбент используется однократно. Обычно это такие процессы, в которых требования к чистоте адсорбента чрезвычайно высоки, и процессы, затраты на адсорбент в которых для потребителя адсорбента, не имеют существенного значения. К первому типу относятся, например, процессы и аппараты для защиты органов дыхания, в том числе, противогазы. Использованный противогаз (боевой или промышленный) изымается, заменяется новым и уничтожается. В качестве основного (но не единственного) адсорбента в противогазах, как правило, применяют активный уголь. Адсорбер – противогаз имеет круглое или фасолеобразное сечение и относится к аппаратам горизонтального типа. Сравнительно большое сечение аппарата при небольшой высоте слоя адсорбента обеспечивает низкое гидравлическое сопротивление, что важно для аппаратов, в которых движение потока очищаемого воздуха происходит за счет дыхания.
Рис.2.3. Адсорбционные процессы
Так же однократно используют активные угли при гемосорбционном лечении больных. Этот операционный метод предназначен для удаления из крови человека токсинов, попавших в организм извне или образовавшихся в нем в ходе болезни. Во время операции из вены больного на ноге отбирают кровь, пропускают ее через колонку с активным углем и возвращают в вену руки. Вариантами гемосорбции являются лимфосорбция и плазмосорбция. К углям, применяемым в медицине, предъявляют повышенные требования. Используют высокопрочные и мало пылящие их модификации. Угли отмывают от смол, стерилизуют и часто предварительно обрабатывают плазмой крови больного. Эту операцию проводят для того, что подавить реакции отторжения, проявляющиеся при контактировании крови больного с поверхностью необработанного угля. При ликвидации запасов химического оружия, к которой Россия должна приступить в ближайшее время, также применяют активные угли. Их используют как средство для обеспечения промышленной безопасности при проведении процесса дезактивации. Особенности функционирования одного из изделий этого назначения будут рассмотрены в примере. В приведенных выше ситуациях однократное применение адсорбента было обусловлено высокой токсичностью накопленных им веществ и медицинскими противопоказаниями для повторного применения отработанного адсорбента, даже если его свойства в целом могут быть восстановлены. В промышленности, соображения из-за которых адсорбент после использования выбрасывают вместо того, чтобы, восстановив его поглотительную способность, использовать повторно, носят экономический характер. Считают, что при расходе адсорбента менее 100 кг/год и его средней стоимости 50 – 100 руб./кг потребителю выгоднее заменить адсорбент, чем усложнять производство операциями по восстановлению свойств. Конечно, указанная граница во многом условна и конкретное значение ограничения обусловлено целым рядом сопутствующих условий. Но общий смысл понятен: если, с точки зрения потребителя, расход адсорбента невелик, то проще его заменить, чем восстановить. Отработанный адсорбент выбрасывают, и он в конечном счете оказывается на свалках твердых промышленных отходов. Типичный пример однократно используемого адсорбционного фильтра дает техника умеренного холода. В каждом бытовом или промышленном холодильнике имеется патрон, содержащий адсорбент. Он расположен после воздушного холодильника и непосредственно перед дросселем сжатого хладагента. Адсорбент осушает масло-хладоновую смесь, циркулирующую в холодильнике, очищает ее от кислых компонентов и, тем самым, защищает дроссель от забивки твердыми отложениями льда. Именно адсорбент обеспечивает долгую безаварийную работу холодильной машины. В качестве него используют цеолит, в состав гранул которого введен оксид алюминия. Цеолит выполняет функцию осушителя, оксид алюминия химически связывает кислоты, которые из-за окисления веществ и материалов постепенно накапливаются в масло-хладоновой композиции. Фильтр, содержащий адсорбент, после исчерпывания емкости по воде выбрасывают и заменяют новым. Преобладают две модификации адсорберов: фильтр с неподвижным слоем зернистого (сферического) адсорбента и фильтр с блочным адсорбентом, конструкция которого показана на рис.2.4. Предпочтение отдается блочной конструкции, адсорбент в которой меньше подвержен эрозии. Как видно из рисунка, очищаемая смесь поступает в фильтр сверху, попадает в центральный канал блока, фильтруется через его стенки и через нижний штуцер возвращается в систему. Тупиковый конец канала выполняет функции сборника грязи. Пространство высоковольтных трансформаторов заполнено специальным маслом, наличие которого предотвращает пробой между токопроводящими элементами. По мере работы трансформатора в масле накапливаются вода и кислоты, появление которых ухудшает диэлектрические свойства масла и понижает величину пробойного напряжения. Для удаления примесей трансформаторы оборудуют фильтрами с адсорбентами. С помощью насоса осуществляют циркуляцию масла из трансформатора в фильтр и обратно. В качестве адсорбентов применяют цеолит, алюмогель и даже природные глины. В трансформаторах малой мощности адсорбент используют однократно. В более мощных и, следовательно, более крупных агрегатах его подвергают реактивации, которую проводят периодически. В последние годы появилась тенденция к непрерывной реактивации адсорбента, выгружаемого из трансформаторов большой мощности.
Рис.2..4. Фильтр – осушитель для малых холодильных машин
Многие приборы, изделия радиоэлектроники, машиностроения поступают к потребителям в полиэтиленовой упаковке. Она обладает ограниченной герметичностью и с течением времени внутри ее влажность возрастает. При высокой относительной влажности (более 30 %) суточные колебания температуры окружающей среды могут привести к выпадению росы, что, естественно, нежелательно. Неконтролируемое повышение влажности предотвращают, размещая внутри упаковки мешочки с адсорбентом-осушителем – силикагелем. После растаривания изделия мешочки выбрасываются – адсорбент используется однократно. Вода является одним из немногих веществ, способных к инфракрасному излучению даже в холодном состоянии, и наличие паров ее в пространстве между оконными рамами увеличивает потери тепла. За рубежом, а в последние годы и в России, в пространство между рамами стали помещать сферический цеолит NaA, который обладает превосходными осушающими свойствами. Считают, что применение стеклопакетов с цеолитом на 30 % понижает потери тепла в течение отопительного сезона. Адсорбент, загруженный в рамы, используется однократно, затраты на его обновление для единичного потребителя, следовательно, невелики. Оно, однако, огромно в абсолютных цифрах и масштабы производства шариковых цеолитов этого назначения превышают масштабы получения всех остальных гранулированных цеолитов– адсорбентов.
Расчет к разделу 2.3
Р.20. Речь пойдет о промышленном предприятии, осуществляющем ликвидацию отравляющего вещества (ОВ). Это очень опасное производство, аппараты в котором тщательно герметизированы, а само помещение оборудовано приточно-вытяжной вентиляцией. Совокупность мер защиты в нормальном режиме работы цеха обеспечивает в помещении концентрацию ОВ 1,39.10-6мг/л, что несколько ниже ПДК. Таким образом, формально нужда в дополнительной очистке вентиляционных выбросов отсутствует. Рассматривается, однако, нештатная ситуация: в силу некоторых непредсказуемых причин (например, из-за аварийной разгерметизации одного из аппаратов) концентрация ОВ в помещении и в выбросах резко увеличивается. Нужно сохранить чистоту воздуха, поступающего в атмосферу. Для этого вентиляционные коммуникации цеха оборудуют адсорбционным фильтром. Адсорбент (активный уголь) в нем, конечно, будет работать однократно: после ликвидации аварии он будет выгружен из адсорбера, направлен на дезактивацию и захоронение. Исходя из некоторых предположений, в основе которых лежат представления о максимальном количестве ОВ, способном попасть в атмосферу цеха, проектировщик установил, что в адсорбционном фильтре должно находится 0,26 м3 активного угля, и предложил конструкцию фильтра. Пусть он представляет собой вертикальный короб сечением 1,7 м2 и шириною 0,15 м. Воздух проходит через сечение короба и выбрасывается в атмосферу. Уголь, если возникнет потребность в его замене, будет выгружен в герметичную тару под действием собственного веса через патрубок, расположенный внизу короба. Однако, срок наступления аварии неизвестен, а воздух непрерывно проходит через фильтр. Уголь, естественно, постепенно теряет свои поглотительные свойства, так как в проходящем через него воздухе всегда содержится небольшое количество ОВ. Возникает вопрос: не будет ли уголь к моменту наступления аварии полностью дезактивирован? Требуется определить, как часто уголь требуется менять. Через фильтр, заполненный активным углем, при 20 0 С и атмосферном давлении проходит 2500 м3 /ч воздуха, который содержит ОВ в концентрации 1,39.10-6 мг/л. Определим срок службы фильтра (0,26 м3 угля) до появления за слоем его относительной концентрации С/Со = 0,5. 1.Физические свойства ОВ: давление насыщенного пара при указанной температуре 0,29 мм рт.ст., плотность в жидкой фазе 1,88 г/см3, парахор 285. 2. Структурные параметры угля по ТОЗМ: W =0,3 см3 /г, В = 1,097.10-6 К-2. 3.Определим концентрацию ОВ в паровоздушном потоке, отвечающую условиям насыщения:
СS = РSМ/RТ = 0,29.207,3.103/62,36.293 =3,3 мг/л
В этом уравнении: СS – искомая концентрация, РS = 0,29 мм рт.ст. – давление насыщенного пара ОВ, М = 207,3 –молекулярная масса ОВ, R = 62,36 мм рт.ст.л/(К.моль)- газовая постоянная, Т = 293 К – температура. Относительная концентрация ОВ в поступающем воздухе равна: Со/СS = 1,39.10-6/3,3 = 4,2.10-7 . 4.Определим коэффициент аффинности: β = ПОВ/ПБЕНЗОЛ = 285/207 = 1,38, где ПОВ , ПБЕНЗОЛ – парахоры ОВ и бензола. 5.Найдем равновесную величину адсорбции ОВ по уравнению ТОЗМ:
Х(Со) = Wρ.exp[-B(T.lg(CS/C)/β)2] =
= 0,3.1,88 exp[ - 1,097.10-6(293.lg(1/4,2.10-7)/1,36)2] = 0,063 г/г угля,
или 0,063.450 =28 г/л, или 28.103мг/л (450 г/л – насыпная масса угля).
6.Найдем предельную возможность слоя угля:
ПВc = Х(Cо)/Cо = 28.103/1,39.10-6 = 2.1010 л/л
7.Относительная проскоковая концентрация С/Со =0,5 примерно соответствует «центру тяжести» выходной кривой. Следовательно, в данном случае предельная возможность соответствует реальной возможности. Определим, какое количество воздуха может быть очищено слоем угля объемом 0,26 м3: 0,26. 2.1010 = 5,2.109 м3.
8.Найдем срок службу угля; он равен: 5,2.109/2500 = 2.106. В году около 9000 ч и срок службы угля превысит 200 лет (!). Очевидно, что цех по уничтожению химического оружия так долго существовать не будет. Следовательно, если не произойдет аварии, уголь заменять не потребуется.
2.4.Циклические процессы с регенерацией адсорбента прямым вводом тепла теплоносителем – газом
2.4.1.Назначение и условия осуществимости
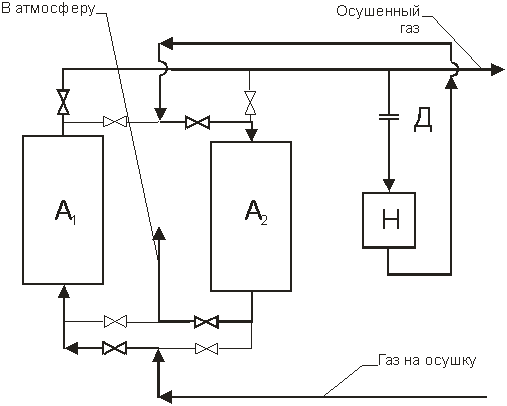
Этот тип циклических процессов (разновидность TSA) применяют для глубокой очистки промышленных (технологических) потоков любой мощности от микропримесей хорошо адсорбирующихся веществ. Организация процесса предусматривает использование части очищенного потока для регенерации слоя – его нагрева и охлаждения. Эта особенность вытекает из предназначенности метода: глубокая очистка требует, чтобы на стадиях регенерации адсорбента он был подготовлен с предельно возможной чистотой. Между тем, в условиях производства, как правило, отсутствует поток более чистый, чем газ, полученный в самой адсорбционной установке. Из этих соображений вытекает схема организации процесса, приведенная на рис.2.5. Итак, пусть в установку под давлением поступает некоторый газ, предназначенный для очистки. При контакте с адсорбентом в одном из адсорберов он очищается и выводится из адсорбера. Основная часть потока идет на потребление, а часть очищенного потока с помощью дросселя Д, понижающего давление газа, отбирают для того, чтобы с его помощью осуществить регенерацию адсорбента во втором адсорбере. Этот поток пропускают через нагреватель Н, газ нагревают и вводят во второй адсорбер в направлении, как правило, противоположном направлению газа при адсорбции. Адсорбент нагревается, примесь десорбируется и переходит в регенерирующий поток. Поток выводят из установки. После того, как нагрев и десорбция будут завершены, нагреватель выключат и в адсорбер начинает поступать холодный чистый поток: слой адсорбента охлаждается. После охлаждения слоя осуществляют переключение адсорберов: первый из них, который к этому моменту времени насыщен примесью, ставят на регенерацию, а во втором начинают процесс адсорбции. Затем последует еще одно переключение адсорберов, еще одно и т.д. Установка в целом работает непрерывно и непрерывно выдает потребителю поток очищенного газа. Циклограмма работы этой двухадсорберной установки приведена на рис.2.6, а на рис.2.5 жирными линиями обозначены коммуникации, «задействованные» в первом полуцикле. Итак, условие, обеспечивающее глубокую очистку потока, - это использование очищенного потока для регенерации адсорбента. Но для того, чтобы оно было выполнено, необходимо, чтобы количество газа, отбираемого на регенерацию, было меньше (желательно, во много раз меньше), чем количество очищенного потока. В противном случае установка будет работать сама на себя или с малым выходом очищенного газа.
Рис.2.5. Схема типичного процесса с прямой регенерацией адсорбента теплоносителем – газом: А1 и А2 – адсорберы, заполненные некоторым адсорбентом, Н – нагреватель, Д – дроссель, цифрами обозначены клапаны, с помощью которых осуществляют управление процессом очистки.
Рис.2.6.Циклограмма работы двухадсорберной установки, схема которой приведена на рис.2.5: А – адсорбция, Н – нагрев, О – охлаждение.
Выше мы привели уравнения для расчета предельных возможностей слоя. Они таковы - максимальная возможность при очистке ПВс - см. уравнение (1.23), - минимальная возможность (потребность) при нагреве или охлаждении ПВt – см. уравнение (1.25), - минимальная возможность (потребность) при нагреве, который сопровождается десорбцией ранее поглощенного вещества, ПВtd – см. уравнение (1.32). Очевидно, что для того, чтобы в процессе рассматриваемого типа выход очищенного газа превышал его расход на собственные нужды установки, необходимо соблюдение следующего условия:
ПВc > ПВt + ПВtd (2.5)
Подставим в уравнение (2.5) значения предельных возможностей:
(X*o + Co)/Co > 2[(H + h)/h] +[ ∆H..X*o/(h.∆T)]
Смысл неравенства не изменится, если из правой части исключить последнее слагаемое:
(Х*о + Со)/Со >> 2(H +h)/h (2.6)
Уравнение (2.6) удобно тем, что в левой части его присутствуют только физико-химические свойства (концентрации) системы, а в правой – только свойства теплотехнические (теплоемкости). В примере Р.5 мы определили отношение теплоемкостей для типичного адсорбента и двухатомного газа, находящегося при атмосферном давлении; оно примерно равно 5.102. Таким образом, очистка этого газа от некоторой примеси в процессе с прямым вводом тепла теплоносителем-газом возможна, если отношение величины адсорбции примеси к ее исходному содержанию в потоке превышает 2.5.102 = 1.103. Эта цифра и есть левое ограничение на область применения метода. Иными словами, очистка потока, в котором коэффициент распределения меньше 103 невозможна, так как расход потоков на регенерацию превысит производительность установки по очищенному газу. Правым ограничением является та область, которая соответствует переходу от процессов с регенерируемым адсорбентом к процессам с адсорбентом реактивируемым. Выше мы определили ее в терминах, связанных с термостабильностью конструктивных материалов. Ее значение, оцененное по коэффициенту распределения ( или предельной возможности при адсорбции) таково: К < 105. В этих двух порядках (103 < K < 105 ) и лежат реальные возможности рассматриваемого метода.
Расчеты к подразделу 2.4.1
Р.21.Возможна ли адсорбционная осушка воздуха, насыщенного водой, при атмосферном давлении и температуре 30 о С? Концентрация воды в газе при 30 0 С в условиях насыщения составляет примерно 32 г/м3. Равновесная величина адсорбции воды свежим цеолитом или силикагелем примерно равна 20 г/100 г. В ходе эксплуатации активность из-за старения и дезактивации адсорбента (см. далее) понизится в 2-3 раза и составит примерно 7 г/100 г. Приведем размерность величины адсорбции к форме, сопоставимой с размерностью концентрации: 7.10-2.600.103 =4,2.104 г/м3 где 600 г/л – насыпная масса адсорбента. Коэффициент распределения равен:
К = (Х*о + Со) / Со = (4,2.104 + 32)/32 = 1,3.103 ,
что практически равно левому ограничению на область применимости метода. Адсорбционная осушка в этих условиях не осуществима, так как почти весь произведенный ею сухой газ потребуется направить на регенерацию. Р.22. Рассмотрим ту же задачу, что в примере Р.21, но при давлении 0,5 МПа. ( В технологических расчетах адсорбции давление выражают в абсолютной шкале, и атмосферному давлению соответствует 0,1 МПа). Концентрация паров воды в сжатом воздухе составляет примерно 32 г в расчете на 1 м3 сжатого воздуха. Величина адсорбции практически не изменится и составит 4,2.104 г/м3. Отсюда коэффициент распределения воды равен К = 1,3 .103 м3 сжатого воздуха в расчете на 1 м3 адсорбента. Но на операции регенерации поступает воздух при атмосферном давлении. В расчете на атмосферное давление коэффициент распределения составит: К = 1,3.103. 0,5/0,1 = 6,5.103 . Это значение заметно превышает левое ограничение и процесс осушки при давлении 0,5 МПа оказывается возможным. Отметим, что с физической точки зрения, потенция к осушке появилась, благодаря тому, что в ходе сжатия газа из него было удалено (переведено в форму конденсата) примерно 4/5 первоначально содержавшейся воды. Р.23. Можно ли очисть от диоксида углерода сухой воздух, в котором содержится 0,03 об.% этого вещества? Для определенности будем считать, что процесс очистки осуществляют при атмосферном давлении и 20 0 С. Концентрацию диоксида углерода в газе выразим в более удобных размерностях: Со = 0,03.10-2.760 = 0,23 мм рт.ст = 0,03.10-2.1,98.103 = 0,6 г/м3, где 1,98 кг/м3 – плотность диоксида углерода при нормальных условиях. Для поглощения диоксида углерода при низких парциальных давлениях в газе пригодны только цеолиты. Их активность, согласно экспериментальным данным, составит примерно 1,5.10-2 г/г, или 1,5.10-2.600.103 = 9.103 г/м3. Отсюда коэффициент распределения К = 9.103 /0,6 = 1,5.104. Процесс очистки возможен. Р.24. Можно ли очистить от диоксида углерода топочный газ, содержащий 12 % этой примеси (будем считать, что прочие загрязняющие компоненты в газе отсутствуют и единственным массовым компонентом топочного газа является не адсорбирующийся азот)? Давление очистки атмосферное, температура 20 0 С. Концентрация диоксида углерода в газе: Со = 11.82.10-2 .760 = 91 мм рт.ст = 12.10-2.1,98.103 = 240 г/м3. Адсорбент – цеолит. Его активность по диоксиду углерода – 0,1 г/г, или 0,1.600.103 = 6.104 г/м3. Коэффициент распределения: К = 6.104/240 = 2,5.102, что много меньше, чем пороговое значение 1.103. Очистить топочный газ рассматриваемым методом невозможно.
2.4.2.Осушка газов
Характеристика влажных газовых сред.В современной технике глубокая осушка газов с помощью адсорбентов вытеснила практически все другие возможные методы. В промышленности используют разные, в том числе специфические, способы выражения абсолютной концентрации паров воды в газах. Назовем их: массовая концентрация (г/м3), парциальное давление ( мм рт. ст.), точка росы (0 С), частей на 1 миллион, или пропромилле (эту концентрацию выражают в объемных и массовых единицах). Из четырех способов два тривиальны. Объясним смысл двух других. Точка росы – это температура, которая соответствует переходу газа, ненасыщенного парами воды, при охлаждении в состояние насыщенности. Очевидно, что понижение температуры ниже точки росы вызовет конденсацию паров – появление «росы». Пропромилле говорит о том, сколько единиц объема (массы) находится в 1 миллионе единиц объема (массы) сухой среды. Эту концентрацию записывают латинскими буквами ppm. Очевидно, что 1ppm = 10 –4 %. Все способы выражения концентраций взаимосвязаны и могут быть рассчитаны по уравнениям состояния газов. Результаты одного из таких расчетов приведены в таблице. Таблица 2.1 Влагосодержание воздуха при атмосферном давлении
Абсолютное влагосодержание многих газов выше, чем воздуха. К числу таких газов относятся сероводород, диоксид углерода, углеводородные газы. Данные о нем приведены в специальной литературе и в справочниках. Абсолютное влагосодержание зависит от давления, при котором находится газ. До давлений порядка 6 – 10 МПа массовая концентрация понижается обратно пропорционально росту давления. Так как процессы осушки газов проводят при повышенных давлениях, а измерения влагосодержания обычно осуществляют при давлении атмосферном, то в значения показателей, характеризующих влагосодержание газа, необходимо вносить определенные поправки. Покажем, как это делается. Пусть в трубопроводе находится воздух при давлении 1 МПа. В пробе этого воздуха, отобранной при атмосферном давлении (0,1 МПа), определено массовое содержание паров воды. Оно, предположим, составляет 50 мг/м3. Влагосодержание в других размерностях берется из таблицы: точка росы –50 0 С, парциальное давление 0,03 мм рт.ст., ppm (объемные) 40, ppm (весовые ) 25 (все цифры округленные). В трубопроводе газ имеет следующие показатели влагосодержания. Массовая концентрация составляет 50.1/0,1 = 500 мг/м3 , парциальное давление -0,03.1/0,1 = 0,3 мм рт.ст., точка росы, определенная по строчке в табл.1.3, которая отвечает парциальному давлению 0,3 мм рт.ст., равна – 30 0 С. Пропромилле – это относительные концентрации, и их значения в сжатом газе такие же, как в расширенном: 40 и 25 ppm. Адсорбенты.Для осушки газов применяют микро- (мелко-) пористые адсорбенты с гидрофильной поверхностью. К ним относятся цеолиты, силикагель, алюмогель. Обычно применяют следующие марки адсорбентов-осушителей: цеолит NaA, силикагель КСМ, технический алюмогель-осушитель. Физико-химическими характеристиками системы вода-адсорбент являются изотермы адсорбции, которые несут информацию о равновесной (предельной) влагоемкости адсорбентов (величине адсорбции паров воды) при разных температурах и разных концентрациях водяного пара в объемной фазе. Практическая влагоемкость, реализующаяся в процессе осушки, которую часто называют динамической активностью, значительно ниже влагоемкости равновесной. Ее значения примерно составляют 6 – 8 г/100 г для силикагеля и алюмогеля и 8 –12 г/100 г для цеолита. О причинах сильных отличий динамической влагоемкости от влагоемкости равновесной (20 г/100 г и более) будет сказано ниже. Средняя теплота адсорбции паров воды составляет 2500 кДж/кг воды для силикагеля и алюмогеля и 4200 кДж/кг для цеолита. В табл.2.2 приведено качественное сопоставление ряда свойств промышленных адсорбентов-осушителей. Данные таблицы содержат информацию, полезную для выбора конкретного адсорбента. Если технологические предпочтения отсутствуют, то используют самый дешевый адсорбент – силикагель. В перечне свойств отсутствуют сведения об остаточном содержании воды в газе, выходящем из адсорбционной установки, или степени осушки. Эти показатели связаны друг с другом: степень осушки = (Со – Сост)/Со. К вопросу об их возможных значениях мы вернемся ниже. Здесь же покажем, что, вопреки распространенному мнению, равновесное давление паров воды над адсорбентом, достигающееся в ходе регенерации, в циклическом процессе не зависит от типа адсорбента. На рис. 2.7 в полулогарифмических координатах представлены две изотермы адсорбции, соответствующие температурам Та и Тр (Тр > Та). Первую из температур будем рассматривать как температуру, при которой происходит адсорбция (осушка), вторую температуру – как температуру, соответствующую регенерации (нагреву).
Таблица 2.2 Технологические свойства промышленных адсорбентов |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 453. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |