Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Внутри-диффузионная кинетика адсорбции
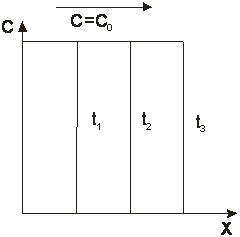
Экспериментальное изучение кинетики адсорбции обладает внешней простотой. Известны две схемы выполнения этого исследования. Они иллюстрированы рис 1.9. Согласно первой из них (рис.1.9 а) гранулу «чистого» адсорбента помещают в трубочку-«перекладину» Н-образного прибора. В «стоячках» прибора двигаются потоки газа. Левый, например, поток – это смесь газа-носителя и газа-метки, диффузию которого изучают. Правый поток – чистый газ-носитель. Метка диффундирует через гранулу и ее концентрацию измеряют на входе в левый «стоячек» (С0) и на выходе из правого (С1). Скорость миграции метки (Р) описывают первым законом Фика:
Р = - DS (dС/dl), или (1.6)
Р = De S (dХ/dl), (1.6а)
где D - коэффициент диффузии, выраженный в концентрационных единицах подвижной фазы, De - эффективный коэффициент диффузии, выраженный в концентрационных единицах неподвижной фазы, S – площадь гранулы, нормальная к направлению диффузии, l – координата по длине гранулы. Предполагается, что значения С и Х равновесны. Заменяя производные конечными разностями, например, dС/dl = (С0 – С1)/L, где L – длина гранулы, вычисляют D и De. Соотношение между ними, очевидно, такое: De = D/(dХ/dС), или для линейной изотермы:
De = D/Г (1.7),
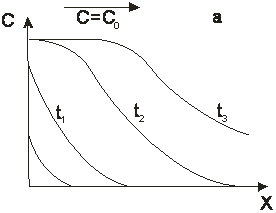
где Г – коэффициент Генри. Размерность коэффициентов диффузии – м2/с. Недостаток схемы, приведенной на рис.1а, заключается в том, что в опытах, выполненных по этой схеме, в сущности, измеряется коэффициент проницаемости сквозных транспортных пор в грануле. Тупиковые поры, в том числе микропоры, в которых происходит адсорбция, этой методикой не учитывается.  Можно поступить по-другому: прикрепить, например, к коромыслу весов гранулу и поместить ее в поток несорбирующегося газа, содержащего адсорбтив в концентрации Со (см. рис.1.9б) Начнется процесс адсорбции – весы будут фиксировать постепенное увеличение веса гранулы. Оно будет продолжаться до тех пор, пока величина адсорбции не достигнет значения, равновесного концентрации адсорбтива в потоке. Обозначим текущую величину адсорбции через Х, равновесную - через Хо. Тогда отношение γ = Х/Хо есть степень отработки емкости сорбента, а ее зависимость от времени [γ = γ(t), где t - время], называемая кинетической кривой, - кинетическая характеристика процесса. Математический аппарат для обработки кинетической кривой и вычисления ее параметра – коэффициента диффузии заимствован из теории теплопроводности. Процесс диффузии в однородное сферическое зерно адсорбента, подобный процессу нагрева (охлаждения) однородной сферической гранулы, при тех начальных условиях, которые были названы в тексте, записывается дифференциальным уравнением, которое носит название второго закона Фика:
∂С/∂t = D[∂2C/∂r2 + (2/r)(∂C/∂r)] (1.8.)
В этом уравнении: С – концентрация адсорбата в газовой фазе гранулы адсорбента, r – текущий радиус гранулы. Решение (1.8.) при линейной изотерме адсорбции дает следующее интегральное выражение:
γ = Х/Хо = 1 – (6/π2) Σ(exp( – n2Fo)/n2 ), (1.9.)
где n = 1, 2, 3,… - ряд целых натуральных чисел, Fo - критерий Фурье: Fo = π2De.t/R2, R,- радиус гранулы. Имеются изящные приемы вычисления De из уравнения (1.9) по известным парным значениям γ и t, т.е. из кинетических кривых. Для гранул иных форм, чем сферическая, получены аналогичные соотношения. Определенные в ходе опытов значения D и De не вполне корректны. Они получены в предположении, что изотермы адсорбции линейны. Между тем, они, как правило, выпуклы. Адсорбция всегда идет с выделением тепла. Расчет же коэффициентов осуществляется в предположении, что процесс адсорбции изотермичен. Но самое главное - это непригодность экспериментально измеренных коэффициентов для прямого прогнозирования переноса в других системах и условиях, чем те, которые были использованы в опытах. Чтобы такое прогнозирование оказалось возможным, необходимы модели структуры адсорбентов и модели переноса вещества в них. Рассмотрим этот вопрос более подробно.
Рис.1.9. Две установки для экспериментального изучения кинетики адсорбции
Промышленный адсорбент содержит поры разного размера. В простейшем случае в рассмотрение следует включить адсорбирующие (микро-) и транспортные поры. Можно принять, что перенос вещества в микропорах характеризуется размером зоны микропористости (для цеолита – радиусом кристаллита), равным r, и эффективным коэффициентом диффузии в микропористости (первичной пористости) - De1 Перенос в транспортных порах (во вторичной пористости) характеризуется радиусом гранулы R и коэффициентом диффузии D2. Будем считать, что перенос в первичной пористости - простое явление и не носит составного характера. В этом случае De1 – единственная диффузионная характеристика этого вида переноса. Для транспортных пор известны, по меньшей мере, две составляющие: перенос по поверхности этих пор и перенос в их объеме. Это параллельные виды переноса и суммарный коэффициент диффузии записывается следующим образом:
D2 = Dv + Г. Des, (1.10)
Dv – коэффициент диффузии в объеме вторичных пор, Des – эффективный коэффициент диффузии по поверхности вторичных пор. Перенос в объеме вторичных пор, видимо, происходит по механизму нормальной диффузии, коэффициенты (Dн) которой широко представлены в литературе. В значения коэффициентов надо внести поправку на порозность гранулы (ε) и извилистость каналов. Доказывается, что
Dv=(ε/K2)Dн (1.11)
Перенос в транспортных порах и в микропорах - последовательные виды переноса и они должны суммироваться через сложение сопротивлений. Строгое определение диффузионного сопротивления отсутствует, но, по здравому смыслу, оно должно быть пропорционально времени пребывания молекул в рассматриваемой среде: t1 – в адсорбирующих порах и t2 – в транспортных порах Для адсорбирующей пористости время пребывания (t1) пропорционально r2/ De1, а для транспортной t2 ~ R2/ D2. Сложение времен дает оценку общего времени пребывания в двух видах пористости (Т):
Т = t2 + t2 ~ R2/ D + r2 /De1.Г (1.12).
Будем рассматривать общее время пребывания в качестве меры диффузионного сопротивления гранул. Иногда величину, обратно пропорциональную общему времени пребывания, называют кинетическим коэффициентом: КК = 1/Т. Его записывают в форме неразложимого комплекса КК = (D/R2). Обратим внимание, что уравнение (1.12) и кинетический коэффициент не содержат некоторого «общего» коэффициента диффузии и принципиально не могут его содержать. Это связано с тем, что у исследователя отсутствуют данные об эффективном (кажущемся) размере гранулы с разными видами пористости, в которых протекают последовательные переносы вещества.
1.3.2. Внешне-диффузионная кинетика адсорбции
Подвод вещества из ядра потока к поверхности адсорбента описывают теми же соотношениями, какими описывают любой процесс массообмена на границе «поток-стенка». Уравнения кинетики в некотором огрублении имеют вид:
(dX/dt) = β*ex f (C – Cх*) = βex(C –Cх*) (1.13.)
В этих уравнениях: X - величина адсорбции, г/м3 ; t - время, с; C и Cх* - текущая концентрации адсорбата в потоке и концентрация, равновесная величине адсорбции на поверхности раздела фаз, г/м3; f- внешняя удельная поверхность гранул, м2/м3; β*ex - коэффициент внешней массоотдачи, отнесенный к единице поверхности раздела фаз, м/с; βex - коэффициент внешней массоотдачи, отнесенный к единице объема слоя, 1/с. Для вычисления коэффициентов внешней массоотдачи используют критериальные уравнения вида:
Nue = A ReemScn , (1.14.)
где Ree - модифицированный критерий Рейнольдса, вычисленный по эквивалентному диаметру прохода; Sc - критерий Шмидта и Nue– модифицированное число Нуссельдта, вычисленное по эквивалентному диаметру прохода, A, m, n – коэффициенты критериального уравнения, значения которых определяются гидродинамическим режимом в зернистом слое. Граничным значениям гидродинамических режимов в зернистом слое соответствуют следующие значения критерия Рейнольдса: ламинарный режим Ree <2, переходной режим 2 < Ree < 30 и турбулентный режим, который реализуется при значениях критерия Рейнольдса более высоких, чем 30. Информация, относящаяся к уравнениям (1.13.) и (1.14.), широко представлена в литературе по химической инженерии.
1.3.3. Смешанно-диффузионная кинетика адсорбции
Уравнение кинетики смешанно-диффузионного процесса часто записывают так:
(dX/dt) = βo(C – C*), (1.15)
где βо – общий коэффициент массопередачи, С* - концентрация адсорбата в потоке, равновесная средней концентрации его в адсорбенте. Смысл прочих параметров уравнения (1.15.) и их размерности см. в уравнении (1.13.). Считают, что общий коэффициент массопередачи есть величина, обратная общему сопротивлению в системе, которое складывается из сопротивления внешней массоотдачи и сопротивления внутренней массоотдачи. Для адсорбции правило аддитивности сопротивлений не доказано, но на практике оно часто используется. Иногда в число сопротивлений включают сопротивление, эквивалентное продольным квазидиффузионным эффектам. Так называют факторы, понижающие эффективность массообмена из-за неидеальной структуры потока в зернистом слое адсорбента. Запишем уравнение аддитивности сопротивлений:
(1/βо) = (1/βех) + (1/βin) + (1/βd), (1.16.)
где βin – кажущийся коэффициент внутренней массоотдачи, βd - коэффициент массоотдачи, эквивалентный продольно-диффузионным эффектам. Размерности всех коэффициентов уравнения (1.16.) – 1/с. Очень часто адсорбционный процесс длится долго. Доказывается, что при больших временах (Fo = 1 и более), когда всеми слагаемыми уравнения (1.9), кроме первого, можно пренебречь, общее время пребывания адсорбата в грануле и коэффициент внутренней массоотдачи связаны примерным соотношением, которое носит название уравнения Глюкауфа. В нашей записи, ориентированной на использование уравнения (1.12.), оно имеет вид:
β in = 15 /Т = 15(D/R2) (1.17.).
Это соотношение позволяет оценить второе слагаемое уравнения (1.16). При «ленгмюровской» изотерме адсорбции, как показали Тодес и Биксон, для сопротивления, обусловленного продольно диффузионными эффектами, справедливо следующее уравнение:
(1/βd) = D*/W2 , (1.18.)
где W – скорость потока, D*- коэффициент продольной диффузии, вычисляемый по справочным данным и значениям критериев Рейнольдса и Шмидта (см. в примере Р.4). Приведенный выше материал позволяет рассчитать параметры, характеризующие кинетику адсорбции. Но качество этого расчета трудно признать удовлетворительным. Кинетика адсорбции – слабо разработанная область теории адсорбции. Поэтому расчетные значения коэффициентов диффузии, массоотдачи и массопередачи в ней часто рассматривают в качестве оценочных параметров и, если необходимо, уточняют их в специальных технологических экспериментах.
Расчеты к разделу 1.3.
Р.4.. Определить общий коэффициент массопередачи при адсорбции воды гранулированным цеолитом NaA из потока метана. Адсорбция происходит при 25 С и давлении 6 МПа, скорость потока в слое цеолита составляет 0,2 м/с. Гранулы адсорбента имеют шарообразную форму; их диаметр составляет 3 мм. Содержание воды в метане 3,3.10-2 кг/м3 . 1.В справочниках приведены значения физических свойств метана при 25 °С и 6 МПа: - плотность ρ = 43,4 кг/м3 ; - вязкость μ = 1,3.10-5 кг/(с.м); - коэффициент нормальной диффузии Dn= 4,9.10-7 м2/с. 2.По уравнению ТОЗМ, приведенному в разделе 1.2., рассчитаем величину адсорбции воды при 25 С и С = 3,3.10-2 кг/м3. Ради экономии, расчет не приводится. Результат его таков: Хо = 1,3.102 кг/м3 3.Определим эквивалентный диаметр сферических гранул цеолита: de = (2εd)/[3(1 –ε)] = (2.0,4.3)/[3(1-0,4)] = 0,67 мм. 4.Критерий Рейнольдса и гидродинамический режим в зернистом слое адсорбента. Критерий Рейнольдса равен: Ree = (Wdeρ)/μ = 0,2.0,67.10-3.43,4/1,3.10-5 = 470. Согласно данным монографии М.Э.Аэрова и О.М.Тодеса (Гидравлические и тепловые основы работы аппаратов со стационарным м кипящим зернистым слоем , Л., «Химия». 1968), граничное значеиие критерия Рейнольдса для турбулентной области в зернистом слое равно 30. Процесс протекает в турбулентном режиме, для которого коэффициенты уравнения (1.14) таковы: A = 0,395, m = 0,64, n =0,333. 5.Критерии Шмидта и Нуссельдта. Sc = μ/(ρDn) = 1,3.10-5/(43,4.4,9.10-7 = 0,64. Nu = ARemScn = 0,395.8700,640,640,33 =37,4. 6.Определим коэффициент внешней массоотдачи: β*ex = Nu.Dn/de = 37,4.4,9.10-7/1,3.10-3 = 1,41.10-2 м/с. Удельная внешняя поверхность гранул составляет: f=6/d =6/3.10-3 = 2.103 м2/м3. Отсюда коэффициент внешней массоотдачи, отнесенный к единице объема слоя,равен: βех = β*ехf = 1,41.10-2. 2.103 = 28,2 1/с. 7.Определим по уравнению (1.12) коэффициент диффузии в объеме транспортных пор гранулы адсорбента: Dv2 = (ε/Ki2)Dn = (0,5/1,52)4,9.10-7 = 1,1.10-7 м2/с. 8. Информация о диффузии по поверхности транспортных пор отсутствует. Можно считать, что приведенное выше значение есть минимальная оценка коэффициента диффузии в транспортных порах: D2 > Dv2.. Отсюда время пребывания молекул воды в транспортной пористости не превышает t2 = R2 /D2 = ((1,5.10-3)2/(1,1.10-7) =20 с. 9.В монографии Д.П.Тимофеева Кинетика адсорбции М., 1962 приведено значение эффективного коэффициента диффузии воды в кристаллах цеолита NaA: De1 = 0,6.10-10 м2/с. Отсюда время пребывания в адсорбирующих порах (в первичной пористости) равно: t1 = r2/De1Г =(1,5.10-6)2 / ((0,6.10-10) .3,9.103) = 1.10 –5 с. Здесь: 1,5.10-6 м – радиус частиц кристаллита. Считают, что в случае нелинейных изотерм адсорбции, к которым относится изотерма адсорбции воды на цеолите, возможна приближенная замена Г на К = Х/С0 = 3,9.103 . 10. Общее время пребывания молекул адсорбата в грануле цеолита: Т = t1 + t2 = 1.10-5 + 20 = 20 с. Лимитирующим сопротивлением в рассмотренном примере является сопротивление транспортных пор. 11.Найдем βin по уравнению (1.17.): βin = 15/Т= 15/20 = 0,75 1/с. 12.Найдем диффузионный критерий Пекле (Ре). Для его определения используем диаграмму, приведенную на стр.229 монографии М.Э.Аэрова и О.М.Тодеса. Согласно этой диаграмме, при Re = 470 и Sc = 0,64 критерий Ре = 2. 13.Определим коэффициент продольной диффузии: D*= Wde/Pe = 0,2.1,3.10-3/2 = 1,3.10-4 м2/с. 14.Определим коэффициент массоотдачи, отвечающий продольной диффузии: βd = W2/D* = 0,22/(1,3.10-4) = 308 1/с. 15.Рассчитаем сумму диффузионных сопротивлений и найдем коэффициент массопередачи: (1/βо) = (1/βex) + (1/βin) + (1/βd) = (1/28,2) + (1/0,75) +1/308) = 1,3 с, βо = 0,75 с-1 Процесс адсорбции в рассмотренном нами случае лимитируется внутренней диффузией, которая в свою очередь определяется диффузией в транспортных порах цеолита.
1.4. Конвективный тепло-массообмен в неподвижном зернистом слое
1.4.1.Объекты рассмотрения Как правило, адсорбционные процессы проводят, пропуская поток через слой неподвижного зернистого адсорбента. При контактировании потока с зернами происходит адсорбция примесей и очистка потока. Это конвективный массообмен в неподвижном зернистом слое. Адсорбция сопровождается выделением тепла. Иногда оно невелико и можно считать, что массообмен протекает в изотермических условиях. В большинстве случаев выделение тепла значительно и адсорбцию следует рассматривать как совмещенный тепло-массообмен в зернистом слое. В ходе адсорбции происходит насыщение адсорбента примесями и он постепенно утрачивает свою очистительную способность. Ее восстанавливают, пропуская через слой поток нагретого газа. Это тоже процесс конвективного тепло-массообмена: нагрева адсорбента и десорбции примеси. И наконец, нагретый адсорбент перед повторным использованием охлаждают потоком холодного чистого газа. Это процесс теплообмена. Таким образом, тепло- и массообмен в неподвижном зернистом слое – суть многих технологических адсорбционных процессов. Конвективный тепло- массообмен в зернистом слое часто называют динамикой (динамикой адсорбции, динамикой нагрева, охлаждения и т.п.). Это самый распространенный вариант осуществления адсорбционных процессов. Мы увидим, что содержание тепло-массообмена в зернистом слое составляют перемещения температурных и концентрационных фронтов (волн). Поэтому динамику процессов переноса в зернистом слое часто называют фронтальной динамикой. Объектом рассмотрения будет являться цилиндрический аппарат (адсорбер), в котором находятся гранулы адсорбента. Начало координат х = 0 поместим в плоскости ввода потока. Начальным условиям будет отвечать адсорбент, равномерно насыщенный адсорбатам. (Частным случаем равномерной насыщенности является слой, не содержащий адсорбат). В тепловых задачах начальному условию обычно отвечает слой с постоянной температурой. В некоторый момент времени t = 0 в слой с расходом W начинает поступать поток, который содержит адсорбат в иной концентрации, чем слой, или имеет температуру, отличающуюся от температуры слоя. Начинаются процессы тепло-массообмена. Будем считать, что концентрация адсорбата в поступающем потоке и его температура не изменяются в течение всего периода пропускания. Концентрация и (или) температура в слое и на выходе из него изменяются из-за протекания массообменных и(или) теплообменных процессов. Определение закономерностей их протекания и составляет основную задачу динамики адсорбции. Методом решения задач динамики тепло-массообмена является математическое моделирование. Структура моделей и вид уравнений баланса обосновываются в курсах математической физики. Уравнения равновесия и кинетики задает технолог. Решения моделей редко имеют аналитическую форму. Обычно результаты получают в численном виде. Они могут использоваться непосредственно или в виде «сверток» в некоторые приближенные соотношения.
Рис.1.10. Зернистый слой – объект рассмотрения.
Такая процедура решения задач по тепло-массообмену в зернистом слое связана с большими затратами времени и труда. Поэтому, наряду с нею, существуют некоторые приближенные приемы. Они вытекают из математических моделей, хотя и являются их сильным упрощением. Эти приближенные приемы полезны, когда решается принципиальный вопрос: возможен или нет некоторый процесс очистки или разделения? Он позволяет затем, по мере получения положительных предварительных оценок, переходят к решениям повышенного уровня сложности.
1.4.2. Нагрев (охлаждение) зернистого слоя и динамика изотермической адсорбции при линейной изотерме адсорбции
Эти две задачи можно рассматривать одновременно, так как в математическом отношении они очень схожи. Математическая модель конвективного нагрева (охлаждения) зернистого слоя имеет вид:
Wh(∂Tg/∂x) + H(∂Ta/∂t) + h(∂Tg/∂t) = 0
∂Ta/∂t = α(Tg – Tg*) (M.1)
T*g = Ta
Начальные условия: t = 0, 0 < x < L; Tg =Ta = Tn Граничные условия: t > 0, x = 0; нагрев Tg > Tn = To; охлаждение Tg < Tn = To. В этих уравнениях: W – скорость потока, h – теплоемкость потока, H – теплоемкость гранул твердого тела (адсорбента), α – коэффициент температуропроводности, L – длина слоя, Tg – текущая температура потока, Ta – текущая температура твердого тела, Tg* - температура потока, равновесная текущей температуре твердого тела, Tn – начальная температура в слое, To – температура потока, поступающего в слой, x – координата длины слоя, t – время. Первое уравнение системы (М.1) – уравнение скоростей изменения теплосодержания (тепловой баланс) в фазах системы. Оно записано с некоторыми упрощениями, основные из которых – это пренебрежение продольной теплопроводностью в слое и потерями тепла в окружающую среду. Второе уравнение – уравнение переноса температуры. Установлено, что процессы переноса тепла (температуры) в зернистом слое, как правило, лимитируются внешней теплоотдачей. Последнее уравнение представляет собой условную запись теплового «равновесия» в системе. Очевидно, что при теплообмене «равновесие» между фазами тождественно равенству их температур. Соотношения однозначности формализуют то качественное описание, которое было приведено в подразделе 1.4.1. Запишем также уравнения математической модели динамики изотермической адсорбции при линейной изотерме адсорбции. Будем предполагать, что адсорбируется только один компонент потока, концентрация которого так мала, что переход вещества из потока в адсорбент не сопровождается тепловыми эффектами и не приводит к изменению скорости потока. В этом случае:
W(∂C/∂x) + ∂X/∂t + ∂C/∂t = 0
∂X/∂t = β0(C – C*) (M/2)
X = ΓC*
Начальные условия: t = 0, 0 < x < L; C = Cn (0), X = Xn (0). (Значения в скобках – часто встречающийся случай с так называемыми нулевыми начальными условиями). Граничные условия: t > 0, x = 0; C = Co. В этих уравнениях: Г – коэффициент Генри, βо- общий коэффициент массопередачи, С – текущая концентрация адсорбата в потоке, Х – текущая концентрация адсорбата в адсорбенте, C* - концентрация адсорбата в потоке, равновесная его концентрации в адсорбенте, Cn - концентрация адсорбата в объемной фазе к моменту начала процесса, Co - концентрация адсорбата в потоке, входящем в слой, X n - концентрация адсорбата в адсорбенте к началу процесса. Смысл уравнений системы (М.2) подобен смыслу уравнений, входящих в систему (М.1). Системы (М.1) и (М.2) имеют аналитическое решение. Оно сложно по структуре и его не часто используют в технологических расчетах. Это решение, однако, удобно для изучения особенностей протекания процессов. Их иллюстрируют рис.1.11.а и 1.11.б. В момент времени, отличный от нулевого в слой начинает поступать поток. Направление движения потока обозначено на рис.1.11 стрелкою. Так как температура (или концентрация адсорбата) в потоке выше, чем температура (или начальная концентрация) в слое, в нем начинают протекать процессы тепло- или массообмена. Из-за конечной скорости переноса тепла (массы) процессы не мгновенны и в слое образуются некоторые кривые распределения температур (концентраций). На рис.1.11а они приведены для возрастающих моментов времени. Как видно из рисунка, кривые распределения (синонимы: фронты, волны) перемещаются
Рис.1.11. Нагрев зернистого слоя или адсорбция при линейной изотерме адсорбции: а – распределения температур или концентраций в моменты времени t1 < t2 < t3; б – выходная кривая для слоя длиною L.
Рис.1.12. Охлаждение зернистого слоя или десорбция при линейной изотерме адсорбции: а – кривые распределения, б – выходная кривая. по слою в направлении, совпадающем с направлением движения потока. При этом их протяженность непрерывно изменяется; она возрастает прямо пропорционально t1/2
В некоторый момент времени (его называют моментом проскока, временем защитного действия) повышенная температура (концентрация) появляются на выходе из слоя и анализатор, установленный в его выходном сечении, начнет фиксировать непрерывное изменение потенциала. Зависимость изменений температуры (концентрации) от времени приведена на рис 1.11.б. Она носит название выходной кривой. На рис.1.12. аналогичные данные приведены для процессов охлаждения слоя (десорбции адсорбата). С точки зрения технолога, основной интерес представляют выходные кривые, так как именно они говорят о том, как скоро слой будет нагрет (охлажден) или насыщен адсорбатом (освобожден от него). На основании тех точных решений, которые были упомянуты выше, для модели (М2) были получены приближенные соотношения. Ниже представлено одно из приближенных соотношений - уравнение Жуховицкого, Забежинского, Тихонова для изотермической адсорбции вещества при линейной изотерме адсорбции:
t0,5 = (LΓ/W)0,5 – Ф(y). (Г/βo)0,5 (1.19.)
В этом уравнении: Ф(у) – вероятностная функция относительной концентрации адсорбата в потоке (у), которая носит название обратной функции Крампа, у = (С - Сn)/(Сo - Сn). Эта функция табулирована и ее значения приведены в математических справочниках и некоторых пособиях по адсорбции. Отметим, что при у = 0,5 имеем Ф(у) = 0; При у < 0,5 Ф(у) положительна, а при у > 0,5 она отрицательна. Функциональное содержание формулы (1.19.) заключается в определении времени (t) появления за слоем длиною (L) некоторой относительной проскоковой концентрации адсорбата (у). Эта концентрация рассматривается в качестве предельно допустимого остаточного содержания примеси в потоке. Возможна и обратная постановка задачи: определение длины слоя, который обеспечивает некоторое предельное содержание примеси в потоке в течение заданного времени. Уравнение (1.19.) получено для прямой задачи массообмена – для адсорбции. Но подобие процессов адсорбции и десорбции при линейной изотерме адсорбции позволяют распространить его на обратную задачу, т.е. на десорбцию. В этом случае между слагаемыми уравнения будет стоять знак «+». Его можно применять также для решения задач, связанных с конвективным нагревом или охлаждением слоя. В этих задачах параметр Г уравнения заменяется отношением теплоемкостей [(H + h)/h)], а общий коэффициент массопередачи будет заменен общим коэффициентом температуропроводности (α). На рис.1.13 в координатах «у-х» повторно изображена одна из кривых распределения концентраций (а) и выходная кривая (б). Нанесем на кривую распределения точку уц (Сц) и проведем через нее вертикальную линию. Площади, образованные кривой распределения и линиями построения, обозначим F1, F2, F3. Пусть относительная концентрация уц в данный момент времени t находится на расстоянии L от места ввода потока в слой. Очевидно, что количество адсорбата, накопленного в слое длиною L, пропорционально площади F3. Площадь F2 пропорциональна количеству адсорбата, которое не уловлено в слое рассматриваемой длины и ушло за его пределы, а площадь F1 – количеству адсорбата, которое в этом слое не поглотилось к моменту времени t, но поглотится, если время будет более значительным. Аналогичные построения можно выполнить для выходной кривой, и соответствующие площади на ней означены через F*.
Рис.1.13. К определению скорости движения центра тяжести: а – кривая распределения концентраций, б – выходная кривая.
Сумма F3 + F 2 пропорциональна количеству вещества, введенному в слой адсорбента. Сумма F 3 + F 1 – количеству адсорбата, которое может быть поглощено в слое рассматриваемой длины. Таким образом:
F3 + F2 ~ WSC0t, F3 + F1 ~ (LSX*0 +LSC0), где S – площадь поперечного сечения слоя, X*0 – величина адсорбции, равновесная концентрации адсорбата в поступающем потоке. Выберем такое положение точки уц (Сц), для которого F1 = F2 . Ее можно назвать центром тяжести кривой распределения (выходной кривой). Для нее из приведенных выше соотношений имеем:
WC0t = L(X*0 + C0) (1.20)
Отношение L/t = Uс следует рассматривать как скорость движения центра тяжести кривой распределения по слою:
Uс = WC0/(X*0+ C0) (1.21)
Так как все величины, входящие в правую часть уравнения (1.21) – постоянные, то скорость движения этой и только этой точки постоянна. Для других концентрационных точек она будет меняться со временем, что приводит, как было показано на рис.1.11., к постепенному увеличению протяженности кривой распределения. Вернемся к уравнению (1.19.). Условие постоянства отношения L/t (скорости движения) для него выполняется, если Ф(у = 0,5) = 0. Значит, координата центра тяжести в рассматриваемых случаях есть у = 0,5. Относительные концентрации, не равные 0,5, передвигаются по слою быстрее (у < 0,5) или медленнее (y > 0,5), чем центр тяжести, что и приводит к постепенному увеличению протяженности кривой распределения. Вывод о постоянстве скорости движения центров тяжести кривых распределения справедлив для фронтов разных форм и разной природы. Он соблюдается при теплообмене и массообмене, для процессов прямых и обратных, для линейной и любых других изотерм адсорбции. Это универсальное свойство движущихся волн. Его использование облегчает грубый расчет (оценку) конвективных процессов в зернистом слое. Преобразуем уравнение (1.21) в следующую форму:
Uс /W = C0/(X*0+ C0) (1.22.)
Умножив числитель и знаменатель левой части уравнения на S – площадь сечения слоя и t - время, мы получаем отношение объема слоя (V = LS) к количеству газа (Q = WSt), которое через слой следует пропустить, чтобы на выходе из него появился центр тяжести кривой распределения. Обратную величину этого отношения можно назвать предельной возможностью слоя при массообмене. Обозначим ее как ПВс:
ПВс = W/Uс = (X*0 + C0)/C0 = К (1.23.)
Она, как видно из уравнения (1.23), равна коэффициенту распределения. Аналогичным образом могут быть получены выражения для скорости движения центра тяжести тепловой волны и предельной возможности слоя при теплообмене (ПВt): Ut =Wh/(H + h) (1.24.)
ПВ t= W/Ut = (H + h)/h, (1.25.)
Ut – скорость движения центра тяжести тепловой волны. Адсорбция – процесс очистки и технолога, как правило, интересуют возможности слоя, отвечающие концентрациям более низким, чем концентрация в центре тяжести волны. По отношению к ним предельная возможность, даваемая уравнением (1.23.), является максимальной возможностью. Она говорит о том, какое максимальное количество потока можно очистить единицей объема адсорбента. Практическая возможность, конечно, будет ниже ее. При нагреве или охлаждении слоя точка глубокого нагрева (охлаждения) всего слоя лежит ближе к входному сечению слоя, чем центр тяжести, и предельная возможность в задачах теплообмена является минимальной возможностью. Она говорит о том, какое минимальное количество потока надо ввести в единицу объема слоя, чтобы его нагреть или охладить. Практическое количество потока будет превышать минимальное. Таким образом, предельные возможности – это приближенные оценки технологических характеристик, или оценки по порядку величин. Их ценность состоит в очень простом определении даже в крайне непростых для точного расчета случаях.
Расчеты к подразделу 1.4.2
Р.5. Теплоемкость двухатомных газов при атмосферном давлении составляет h = 1,25 кДж/м3.К; теплоемкость адсорбента равна H = 0,96 кДж/кг.К. Определить минимальное количество воздуха с температурой 20 °С, которое необходимо пропустить через слой объемом 15 м3 , имеющим начальную температуру 200 °С, чтобы охладить слой, и самую высокую температуру слоя после такого охлаждения. 1.Изменим размерность H: Н = 0,96.ρа = 0,96.600 = 580 кДж/м3.К, где ρа = 600 кг/м3 – насыпная плотность адсорбента. 2.Определим предельную возможность, которая является минимальной; она равна: ПВt = (Н + h)/h = (580 +1,25)/1,25 = 460 м3/м3 3.Для охлаждения 15 м3 слоя потребуется воздуха не менее 15.460 = 6900 м3 . 4.Самая высокая температура слоя будет находиться в сечении, противоположном сечению ввода охлаждающего воздуха. При пропускании того количества, которое было определено выше, в этом сечении будет находиться центр тяжести тепловой волны, для которого у = 0,5. По определению имеем: у = (Т – Т0)/(Тn – Т0 ) = 0,5 0,5 = (Т – 20)/(200 – 20); Т = 110 °С.
Р.6. В слой некоторого сорбента, объем которого составляет 15 м3, ввели поток. В нем находится нежелательный компонент, адсорбция которого на данном адсорбенте характеризуется коэффициентом Генри Г = (Х*о + С0)/С0 = 1000 м3/м3 . Определить предельную возможность слоя в удалении нежелательной примеси и максимальное количество очищенного потока. 1.Для 1 м3 имеем: ПВс = Г = 1000 м3/м3 . 2.Для 15 м3 имеем: 15.1000 = 15000 м3 – таково максимально возможное количество очищенного потока.
Р.7. В условиях примера Р.6 определить практическое количество очищенного потока, если остаточное содержание нежелательного компонента в очищенном потоке не должно превышать 0,05 С0. Коэффициент массопередачи принять равным β0 = 1,09 1/с, скорость потока 0,2 м/с, сечение 4 м2. Начальным содержанием адсорбата в адсорбенте пренебречь. Подстановкой в правую и левую части уравнения (1.19) произведения (SW)1/2 придадим ему следующую форму: Q1/2 = (VΓ)1/2 – Ф(y).(WSГ/β)1/2 1.По условию задачи у = 0,05. Найдем Ф(у) по таблице, приведенной в пособии Е.Н.Серпионова. Промышленная адсорбция газов и паров. М., «Высшая школа», 1969, стр.87. При указанном значении у имеем: Ф(у) = 1,19. 2.Подставим условия задачи в модифицированное уравнение: Q1/2 = (15.1000)1/2 – 1,19. (0,2.4.1000/1.09)1/2 = 95,38 м3/2, или Q = 9100 м3. Практическое количество очищенного потока примерно на 40 % ниже максимально возможного, определенного в предыдущем расчете. Обратим внимание на то, что расчет практического количества очищенного потока потребовал задания ряда конструктивных параметров, тогда как расчет максимального базировался только на свойствах системы. Таким образом, эти два расчета относятся к разным этапам проектирования: расчет максимального к более раннему этапу, а расчет практического к более позднему.
Р.8. Слой нагретого адсорбента охлаждают потоком, скорость которого составляет 0,2 м/с. Поток содержит нежелательную примесь, которая не адсорбируется нагретым адсорбентом, но поглощается в слое после охлаждения. Теплоемкости потока и адсорбента приведены в примере Р.5. Будет ли одновременно с охлаждением идти процесс адсорбции, если Г = 1000? Если Г= 100? 1.Найдем скорость движения концентрационного фронта при Г =1000. Uс = W/Г =0,2/1000 = 0,0002 м/с 2.Найдем скорость движения теплового фронта: Uе = Wh/(Н + h) = 0,2.1,25/(580 + 1,25) = 0,00043 м/с. Скорость движения теплового фронта примерно в два раза больше, чем концентрационного. Поэтому в слое образуется некоторая зона, в которой адсорбент уже охлажден, но еще не насыщен примесью. Охлаждение будет сопровождаться очисткой, хотя, возможно, и неэффективной. 3.При Г = 100 скорость движения концентрационного фронта составит: Uс = 0,002 м/с. Скорость движения теплового фронта приведена в п.2. Она примерно в 5 раз выше скорости движения концентрационного фронта. В слое отсутствуют условия для образования холодной зоны ненасыщенного адсорбента. В этих условиях охлаждение не сопровождается очисткой.
1.4.3. Динамика изотермической адсорбции при произвольной изотерме адсорбции Общий подход.Динамика изотермической адсорбции при произвольной изотерме адсорбции рассматривается при тех же допущениях, что и динамика при линейной изотерме. Запись математической модели (система уравнений (М3)) во всех отношениях, кроме уравнения равновесия, приведенного в третьей строчке системы, подобна записи системы (М2). Уравнение равновесия в систему (М3) включено в общем виде.
W(∂C/∂x) + ∂X/∂t + ∂C/∂t = 0
∂X/∂t = β0(C – C*) (М3)
X = X(C*)
Будем считать, что начальные и граничные условия в системах (М2) и (М3) одинаковы. Система (М3) аналитического решения не имеет. Ее решают численными методами. Систему уравнений (М3) приводят к разностной форме. Для этого слой длиною L разбивают на m-интервалов, ожидаемую общую продолжительность адсорбции t - на n-интервалов. Для i-го интервала по длине и j-го по времени при использовании простейшей разностной схемы уравнения системы (М3) будут записываться так:
W(Cij – Ci-1-1,,j )/hi + (Xij – Xi,j-1)/hj + (Cij – Ci,j-1 )/hj = 0
(Хij - Х i – 1, j)/hi = β0(Cij – C*ij)
Xij = X(Cij)
В этих уравнениях hi, hj - шаги по времени и длине. Система в конечных разностях состоит из трех уравнений и содержит три подлежащие определению переменные: Сij, С*ij и Хij, Она, следовательно, решается. После определения значений переменных в точке ij проводится переиндексация. Индексы i и j присваивают следующей точке, отстоящей на один шаг дальше по координатам t или L, а прежняя точка, ранее имевшая индексы іј получает индексы i-1,j, если сдвиг производится по координате t, или i,j-1, если сдвиг произведен по координате L. В новой точке рассчитываются новые значения переменных. Далее делается следующая переиндексация, еще одна и т.п. до тех пор, пока значения переменных ни будут рассчитаны во всем поле значений L – t. В качественном отношении решения модели (М3) хорошо согласуются с экспериментальными данными. Количественное соответствие улучшают путем подгонки значений параметра β 0. Причина, из-за которой именно этот параметр принимают в качестве подгоночного, указана в разделе 1.3. В левой части рис.1.14 приведены кривые распределения концентраций по слою адсорбента для так называемых выпуклых изотерм адсорбции. К этому типу относятся, в частности, изотермы, описываемые уравнениями Ленгмюра и ТОЗМ. Для них характерен более быстрый рост величин адсорбции в области малых давлений, чем в области больших. Пример выпуклой изотермы приведен в правой части рисунка.
Рис.1.14. Кривые распределения (t 1 < t 2 < t3 ) и выпуклая изотерма адсорбции.
На рис.1.15. приведены аналогичные кривые для изотерм вогнутых. Для них, как видно из правого рисунка, характерен сравнительно медленный рост величин адсорбции в области малых концентраций и быстрый – в области больших. Сопоставление кривых распределения на рис.1.14 и рис.1.15 говорит о том, что общие закономерности протекания
Рис.1.15. Кривые распределения (t1 < t2 < t3) и вогнутая изотерма адсорбции.
адсорбционного процесса для этих изотерм различны. При выпуклой изотерме кривые распределений с течением преобразуются в некоторое компактное распределение. При вогнутой наблюдается тенденция к неограниченному росту протяженности распределения. Выкладками, подобными тем, которые были выше приведены для линейной изотермы, можно показать, что скорости движения концентрационных точек, отвечающих центрам тяжести, в случае и выпуклых, и вогнутых изотерм описываются уравнением:
Uc = WC0 /(X*0 + C0) = W/K, (1.21)
где К – коэффициент распределения. Аналогичным образом предельные (максимальные) возможности равны: ПВс = К. Хотя для выпуклой и вогнутой изотерм скорости движения центра тяжести и максимальные возможности в принципе могут быть одинаковы, практические возможности, относящиеся к головным участкам кривых распределения, для выпуклых изотерм, как правило, выше, чем для вогнутых. Иными словами, при прочих равных условиях выпуклая изотерма обеспечивает сравнительно более высокий съем очищенного потока и по этой причине является предпочтительной. Путем «свертки» очень большого объема расчетной информации Жуховицкий, Забежинский и Тихонов получили следующие интерполяционные уравнения для выпуклых изотерм при нулевых начальных условиях (t = 0, 0 ≤ x ≤ L, C = X = 0): Ленгмюровская изотерма:
t = (X*0/WC0){L – (W/β0) [ln((C0/C) – 1)/p + ln(C0/C) –1]}, (1.26)
где р = С0/Сˆ, Сˆ – концентрация адсорбата в потоке, равновесная величине Х = 0,5 Хm; Прямоугольная изотерма (так называют идеализированную изотерму адсорбции, для которой можно записать: С > 0, Х = Хm =const):
t = (X*0/WC0)[L – (W/β0)(ln(C0/C – 1)] (1.27).
Равновесное приближение.Общий подход не содержит явных указаний на причины, в силу которых в системах с разными типами изотерм адсорбции кривые распределения ведут себя по-разному. Ответ на этот вопрос представляет познавательный интерес, полезен в расчетах и часто необходим в выборе адсорбентов. Он решается в рамках равновесного приближения. Исключим из системы (М3) уравнение кинетики, предположив, что β0 → ∞. В этом случае С – С* → 0 и С ≈ С*. При таких допущениях модель приобретает вид:
W(∂C/∂x) + ∂X/∂t + ∂C/∂t) = 0
X =Х (C) (M.4).
Решения системы (М4) при тех же условиях однозначности, которые были записаны выше, получены Викке в форме уравнений для скоростей движения фронтов. Они таковы:
- для С = const, Uf = WC0/(X*0 + C0) (1.28)
- для C ≠ const, Uc = W/(1 + Х′(C)) (1.29)
Уравнение (1.28) по другим, но схожим поводам, неоднократно представлялось выше. Оно носит название уравнения Вильсона и описывает движение «обрывного» (С = const) концентрационного фронта. Он движется по слою с постоянной скоростью Uf . «Обрывный» фронт и его перемещения показаны на рис. 1.16.
Рис.1.16. Движение по слою «обрывного» концентрационного фронта.
Уравнение (1.29) носит название уравнения Викке. Оно говорит о том, что при отсутствии «обрывного» фронта каждая концентрационная точка кривой распределения концентраций передвигается по слою со своей характерной скоростью Uс, значение которой зависит от производной изотермы адсорбции (Х′ (С)) в этой концентрационной точке. При нелинейной изотерме адсорбции значения производной непостоянны: они уменьшаются с ростом концентрации, если изотерма выпуклая, и возрастают в случае изотермы вогнутой. Соответственно в «необрывном» фронте и выпуклой изотерме концентрационная точка, отвечающая высокой концентрации, будет двигаться быстрее, чем точка низкой концентрации. При вогнутой изотерме и прочих одинаковых условиях по слою быстрее передвигается слою точка, отвечающая низкой концентрации. Кривые, приведенные на рис. 1.17, отражают эти особенности процесса для выпуклой (а) и вогнутой (б) изотерм. Итак, при вогнутой изотерме адсорбции и том направлении движения потока, которое обозначено на рис. 1.17 стрелкой, первоначальное размытое распределение концентраций в слое становится еще более размытым: в ходе движения фронта градиент концентраций уменьшается. В тех же условиях при выпуклой изотерме концентрационные точки, отвечающие высоким концентрациям, постепенно догоняют точки низких концентраций. Градиент концентраций возрастает до тех пор, пока в слое ни образуется «обрывный» фронт. С момента его образования все концентрационные точки, т.е. фронт в целом, передвигаются по слою с одной и той же скоростью, значение которой дается уравнением Вильсона. Для вогнутой изотермы, таким образом, наблюдается полное качественное соответствие между предсказаниями моделей (М3) и (М4). Для выпуклой изотермы полное соответствие отсутствует: из модели (М3) следует, что в своем предельном состоянии фронт компактен, но размыт, из (М4), что он предельно компактен – «обрывный».
Рис.1.17. Кривые распределения концентраций в равновесной динамике адсорбции при вогнутой (а) и выпуклой (б) изотермах.
Отметим, что при изменении направления движения потока на противоположное направление фронт сжимается при вогнутой изотерме адсорбции и расширяется при выпуклой. Эти ситуации отвечают обратному процессу – десорбции. Квазистационарное приближение. Неполное соответствие кривых распределения, полученных из моделей (М3) и (М4), при выпуклых изотермах адсорбции было объяснено Зельдовичем. Суть объяснения сводится к следующему. Из-за конечной скорости массообменных процессов размывание кривых распределения идет всегда. При вогнутой изотерме оно усугубляется размывающим эффектом, который обусловлен видом изотермы адсорбции. При выпуклой изотерме размывающий эффект конечной скорости массообмена, наоборот, компенсируется сжимающим эффектом, обусловленным видом изотермы. В слое достаточно большой протяженности и выпуклой изотерме эффекты размывания и сжатия компенсируют друг друга и по слою, начиная с некоторого момента времени, с постоянной скоростью передвигается фронт постоянной протяженности и постоянного профиля. Скорость его движения описывается уравнением Вильсона, что естественно, так как в состав этого фронта входит центр тяжести. Такой режим переноса фронта носит название квазистаионарного. Существование квазистационарного режима переноса фронта сорбции было зафиксировано уже в ранних работах (Шилов с сотр.) по динамике адсорбции. Причины и условия его возникновения были непонятны, но сам факт его реализации позволил разработать сравнительно простые приемы расчета процесса. К числу их относятся уравнение Шилова, концепция зоны массопередачи (высоты работающего слоя) и некоторые другие подходы. Некоторые из них обсуждаются в общеинженерных курсах.
Расчеты к подразделу 1.4.3 Р.9.Рассчитать продолжительность осушки метана цеолитом NаА, длина слоя которого составляет L = 3 м. Остаточную концентрацию воды в газе принять равной С = 10 мг/м3. Прочие условия процесса осушки приведены в примере Р.4: начальная концентрация воды в метане С0 =3,3.10-2 кг/м3; равновесная величина адсорбции Х*0= 1,3.102кг/м3; скорость потока W = 0,2 м/с; общий коэффициент массопередачи β0 =1,09 1/с. Изотерма адсорбция воды на цеолитах имеет почти прямоугольную конфигурацию. Поэтому продолжительность процесса может быть рассчитана по уравнению (1.26):
t = (X*0/WC0) [L – (W/β0) (ln(C0/C) –1)] =
(1,3.102/0,2.3,3.10-2) [ 3 – (0,2/1,09)(ln(3,3.10-2/10-6) – 1)] = 3.104 c ≈ 8 ч.
Р.10. На приведенном ниже рисунке, который повторяет рис.1.6, приведены изотермы адсорбции воды на среднепористом (1) и микропористом (2) силикагелях. Руководствуясь данными этого рисунка определить, какой из этих силикагелей следует выбрать для организации адсорбционного процесса осушки газа. Принять, что относительная влажность φ =100 % соответствует концентрации воды в газе, поступающем на осушку, равной 20 г/м3 1.Если ориентироваться на максимальную возможность адсорбентов:
ПВc= K = (X*0 + C0)/C0 ,
то предпочтение будто бы должно быть отдано среднепористому силикагелю. Действительно, при φ = 100 % (С0 =20 г/м3) его равновесная активность более чем в 1,5 раза превышает равновесную активность мелкопористого силикагеля, Соответственно, возможность этого адсорбента, рассчитанная по концентрации воды в газе, поступающем на осушку, будет больше в сравнении с силикагелем мелкопористым. Увы, этот вывод неверен.
Изотермы адсорбции воды средне- (1) и микропористым (2) силикагелями
2.Изотермы адсорбции воды на силикагелях имеют сложную конфигурацию: начальный участок изотерм выпуклый, средний вогнутый, а замыкающий снова выпуклый. В соответствии с концепциями, изложенными в подразделе «Равновесное приближение», кривые распределения адсорбата по слою также будут иметь сложную конфигурацию. В головной части распределения будет расположен почти обрывный участок, отвечающий первому выпуклому участку изотермы адсорбции. За ним будет следовать размытый участок кривой распределения (средний интервал концентраций) и снова – почти обрывный участок. Гипотетическое распределение концентраций для выпукло-вогнутой-выпуклой изотермы адсорбции, которая характерна для системы вода-силикагель, изображено на рисунке.
Гипотетическое распределение концентраций воды в слое силикагеля
3.В соответствии с п 2, расчет максимальных возможностей должен выполняться по точке перегиба на изотерме адсорбции, разделяющей первый выпуклый и вогнутый участки. Эта точка лежит при φ =35 % для обоих силикагелей (С =7 г/м3). При этой концентрации величина адсорбции воды на мелкопористом силикагеле в 2 раза превышает величину адсорбции на силикагеле среднепористом. Предельные возможности силикагелей, рассчитанные по концентрации и величине сорбции в точке перегиба, будут различаться в такое же количество раз. Для адсорбции воды следует выбрать мелкопористый силикагель.
1.4.4. Динамика адиабатической адсорбции Общий подход.Если концентрация примеси в потоке значительна, то ее адсорбция сопровождается выделением тепла, что приводит к увеличению температуры потока и адсорбента. Адсорбция приобретает характер неизотермического процесса. В пренебрежении потерями тепла в окружающую среду и теплообменом со стенкою адсорбера можно говорить о адиабатическом процессе, или динамике адиабатической адсорбции. Очевидно, что изотермический процесс – это предельный случай процесса адиабатического, при котором тепловыделения в слое пренебрежимо малы. Поэтому все допущения модели изотермической, кроме особенностей тепловыделения и теплообмена, распространяются на модель адиабатической сорбции. Общая запись ее такова:
W(∂C/∂x) + ∂X/∂t + ∂C/∂t = 0
Wh(∂Tg/∂x) + H(∂Ta/∂t) + h(∂Tg/∂t) + ∆H(∂X/∂t) = 0
X = X(C*, Ta) (М.5)
∂X/∂t = β0(C –C*)
∂Ta/∂t=α0(Tg-T*g)
Первое уравнение этой модели – уравнение материального баланса адсорбата. По записи оно не отличается от аналогичных уравнений предшествующих моделей. Второе уравнение – тепловой баланс; в отличие от аналогичного уравнения модели (М1), оно содержит слагаемое, которое отвечает приходу тепла в результате адсорбции. Характеристикой этого источника является теплота адсорбции - ∆Н (кДж/г). Третье уравнение – политерма равновесной адсорбции. Она представляет собой семейство изотерм адсорбции, отвечающих разным температурам. Вид изотерм в этой задаче обычно не рассматривается. Но скрыто предполагается, что все они являются выпуклыми. Четвертое и пятое уравнения – это соответственно уравнения кинетики сорбции и теплообмена. Все параметры и переменные, которые входят в систему (М5), кроме ∆Н, были определены в ранее рассмотренных моделях. Начальные условия: t = 0, 0 ≤ x ≤ L, C = X =0, Tg= Ta = Tn . Граничные условия: t > 0, x = 0, C = C0, X = X(C0 , t), Tg = Tg0 , Ta = Ta(t). Многие параметры, входящие в систему (М5), зависят от температуры. К ним относятся скорость потока, теплоемкости, коэффициенты изотерм адсорбции, коэффициенты уравнений массо- и теплопередачи. Поэтому базовая система (М5) обычно дополняется соотношениями, учитывающими зависимости параметров от температуры. Полная система, описывающая адиабатическую адсорбцию, приобретает громоздкую форму. Ее аналитическое решение невозможно. В литературе представлены немногочисленные лримеры численных решений модели (М5). Феноменология процесса. Качественные особенности протекания адиабатических процессов рассмотрены в работах двух групп исследователей: Тодеса-Лезина и Пана-Басмаджиана. Эти работы и положены в основу приведенного ниже обсуждения. Авторы выделяют два предельных (идеализированных) режима переноса температурного и концентрационного фронтов в слое: режим одиночной тепловой волны и режим комбинированных волн .Выходные кривые для них приведены на рис.1.18 и 1.19.
Рис.1.18. Выходные кривые адиабатической адсорбции для режима одиночной тепловой волны: 1 – температурная кривая, 2 – концентрационная кривая.
Рис.1.19. Выходные кривые адиабатической адсорбции для режима комбинированных волн: 1 – температурная кривая, 2 – концентрационная кривая.
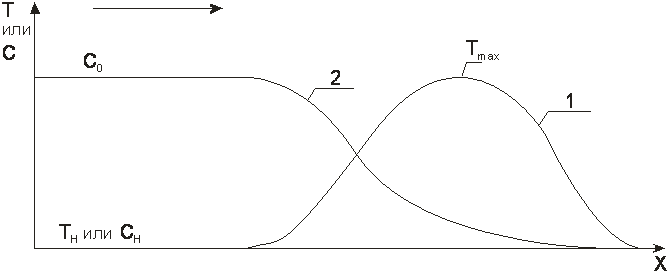
Кривые на рисунках разбиты на интервалы для того, чтобы облегчить их обсуждение. Итак, на участке ОА рис.1.18 температура потока и концентрация примеси в нем за слоем длиною L равны начальным значениям этих переменных. Изменения температуры и концентрации, обусловленные адсорбцией, происходят внутри слоя и пока не проявляются на выходе из него. В точке А из слоя начинает выходить поток с повышенной температурой; концентрация продолжает оставаться неизменной и равной начальной. В точке В, когда температура достигает максимального значения (Тmax ), на выходе из слоя появляется концентрационная точка отвечающая более высокому, чем начальное, содержанию адсорбата в потоке. Таким образом, в течение времени, пропорционального протяженности участка АВ, из слоя выходит «горячий» и чистый поток. Тепловой фронт обогнал фронт концентрационный, что и дало основания назвать такой режим режимом одиночной тепловой волны. Концентрация примеси за слоем продолжает нарастать, Но скорость адсорбции уменьшилась, приход тепла от адсорбции не компенсирует его вынос с потоком и подъем температуры сменяется ее падением. Начало падения, которое происходит из-за поступления в слой сравнительно холодного очищаемого газа, обозначено на рисунке точкой С. После того, как адсорбция примеси в слое завершилась, на выходе из него появилась концентрационная точка, отвечающая содержанию примеси в исходном потоке (Со). Температура потока к этому моменту времени достигла значения, характерного для газа, поступающего на очистку. Завершению процессов тепло- и массообмена отвечает точка Д. Кривые распределения температур и концентраций в слое есть некоторое «обращение» выходных кривых внутрь слоя. Для режима одиночной тепловой волны и некоторого времени t кривые распределения приведены на рис.1.20.
Рис.1.20. Кривые распределения температур (1) и концентраций (2) в слое адсорбента (t < tA ) для режима одиночной тепловой волны
Рассмотрим выходные кривые на рис.1.19. На участке ОА изменения температуры и концентрации отсутствуют: они происходят внутри слоя адсорбента. В точке А на выходе из слоя почти одновременно появляются температура и концентрация, отличные от начальных значений этих параметров. В точке В температура достигает максимального значения (Тmax ) а концентрация приближается к значению (С’), промежуточному между содержанием адсорбата в исходном потоке и его начальным содержанием в адсорбенте. Далее, вплоть до точки С значения концентрации и температуры почти постоянны. Концентрация и температура достигают исходного уровня в точке Д. Из-за одновременного появления за слоем температурной и концентрационной волн режим называют комбинированным. На рис 1.21 приведены кривые распределения температур и концентраций в слое. Подчеркнем особенности режимов. В режиме одиночной тепловой волны, начиная с некоторого момента времени, когда адсорбция в слое еще не завершена, тепло адсорбции начинает выноситься из слоя. В режиме комбинированных волн тепло адсорбции не выносится из слоя, а аккумулируется в нем вплоть до почти полного завершения адсорбции.
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 725. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |