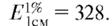Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
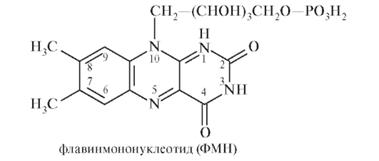
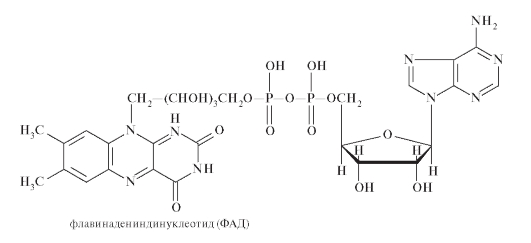
Механизмы действия и биотрансформация⇐ ПредыдущаяСтр 43 из 43 Всасываясь из кишечника, рибофлавин при участии АТФ фосфорилируется и превращается в коферментные формы: флавинмононуклеотид (ФМН) и флавинадениннуклеотид (ФАД).
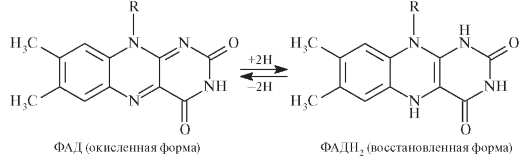
Оба кофермента принимают участие в окислительновосстановительных процессах с присоединением двух атомов водорода и образованием восстановленной формы ФАД2:
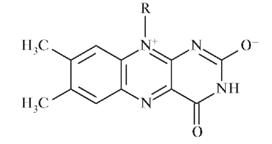
При недостатке рибофлавина развивается ангулярный стоматит (нейлоз): трещины в углах рта и на губах. Наблюдается гноссит (сосочки языка сглажены, цвет языка пурпурный с синеватым оттенком), поражение кожи у носа, ушных раковин. Обнаруживается васкулярный кератит: расширение сосудов конъюнктивы вокруг роговицы. Возникают светобоязнь, слезотечение. Иногда происходит нарушение зрения в темноте - гемералопия. Нередко возникает анемия. Контроль качества В молекуле рибофлавина атом азота в положении N10 проявляют основные свойства; основность атомов азота N1, N5 ослаблена из-за участия в сопряжении π-связей азодиеновой группы и свободных электронов атомов азота. Основными свойствами обусловлены аналитические эффекты при взаимодействии рибофлавина с общеалкалоидными осадительными реактивами (раствор йода в йодиде калия K[I3], реактив Драгендорфа K[BiI4] (см. приложение 5), фосфорно-молибденовая кислота H3PO4 • 12MoO3 • 2H2O кремнефольфрамовая кислота SiO2 • 12WO3 • 2H2O, пикриновая кис лота - 2,4,6-тринитрофенол, раствор танина). Рибофлавин растворим в уксусной кислоте и сильных минеральных кислотах. При растворении в кислотах образуется таутамерная (аллоксазиновая) форма рибофлавина:
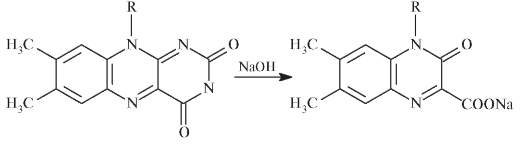
В 0,1 моль/л растворе NaOH происходят разрыв пиримидинового кольца рибофлавина и окисление по положению С2 пиразинового цикла: 
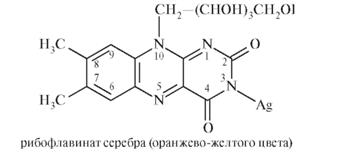
В положении N3 находится -NH-центр кислотности, обусловленный электроноакцепторным влиянием карбонильного атома кислорода в положениях С2 и С4. Это свойство лежит в основе реакций образования комплексов рибофлавина с ионами металлов Cu2+, Co2+, Ag+:
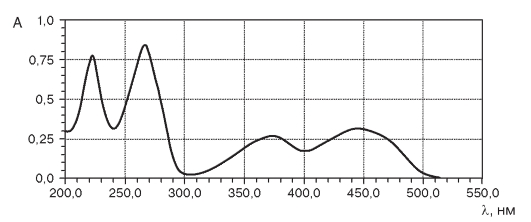
Для молекулы рибофлавина характерна пространственная изомерия, связанная с присутствием хиральных центров - асимметрических атомов углерода в положениях С2, С3, С4 рибитильной цепи. Это свойство рибофлавина можно использовать при его идентификации или определении содержания действующего вещества методом поляриметрии. Определение подлинности.Способность водного раствора рибофлавина (1:100 000) желто-зеленого цвета флуоресцировать и менять интенсивность флуоресценции используют при его идентификации. При добавлении 0,02 г натрия водородсульфита (гидросульфита) к 5 мл раствора рибофлавина окраска исчезает и появляется вновь при встряхивании смеси на воздухе. Флуоресценция исчезает также при добавлении раствора HCl разведенной или раствора щелочи. Раствор рибофлавина в фосфатном буфере (1:100 000), рН 7,0, поглощает в ближней, дальней УФ- и видимой областях с максимумами при 223, 268, 373 и 445 нм (рис. 10.9). Для поляриметрического определения подлинности навеску высушенного рибофлавина (0,1 г) растворяют в 4 мл 0,4 моль/л раствора NaOH, добавляют 10 мл свежепрокипяченой и охлажденной воды, 4 мл спирта и доводят объем до 20 мл. Определяют угол вращения в 100 мм кювете через 30 мин после приготовления испытуемого раствора. Удельное оптическое вращение раствора рибофлавина Испытания на чистоту.В субстанции рибофлавина нормируют содержание люмифлавина колориметрическим способом, используя свойство люмифлавина растворяться в хлороформе. Для этого 0,025 г рибофлавина встряхивают с 10 мл хлороформа, не содержащего спирт, и фильтруют. Фильтрат не должен иметь более интенсивную окраску, чем раствор сравнения (2 мл 0,016 моль/л K2Cr2O7 разводят водой до 100 мл).
Рис. 10.9. Электронный спектр раствора рибофлавина (фосфатный буфер) в УФ- и видимой области спектра
Потеря в массе при высушивании не должна превышать 1,5%. Остаток после сжигания не должен превышать 0,20%. Количественное определение.Количественное определение рибофлавина проводят методами: - спектрофотометрии; - поляриметрии: - титриметрии. Методика количественного определения рибофлавина основана на снятии электронного спектра поглощения его раствора в видимой области: в колбе из темного стекла на 500 мл суспендируют 65 мг рибофлавина в 5 мл воды и разводят 5 мл раствора натрия гидроксида. После полного растворения добавляют 100 мл воды и 2,5 мл ледяной уксусной кислоты, разводят до 500 мл водой. 20 мл полученного раствора переносят в колбу из темного стекла на 200 мл, добавляют 3,5 мл 14 г/л раствора натрия ацетата и разводят 200 мл водой. Измеряют абсорбцию полученного раствора при длине волны 445 нм. Рассчитывают содержание действующего вещества, используя значение коэффициента удельного погашения
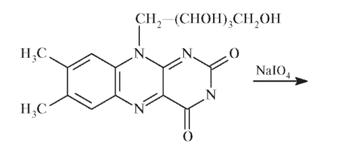
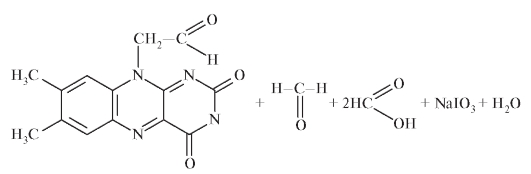
Перйодатное окисление (реакция Малапрада) основано на окислении D-рибитила в положении N10 рибофлавина 0,02 моль/л раствором перйодата натрия (калия) в нейтральной среде при комнатной температуре с образованием муравьиной кислоты. Количество выделяющейся муравьиной кислоты эквивалентно исходному количеству рибофлавина:
В результате реакции происходит восстановление йода(VII) до йода(V). Затем для завершения количественного определения проводят: - нейтрализацию муравьиной кислоты щелочью:
Контрольные вопросы и задания • Напишите структурную формулу рибофлавина. Охарактеризуйте физические и физико-химические свойства (внешний вид, растворимость, оптическая активность, поглощение в УФ- и видимой областях спектра). Укажите значение этих свойств при оценке качества ЛВ. • Обоснуйте способность рибофлавина участвовать в окислительно-восстановительных процессах. Укажите возможности использования окислительно-восстановительных реакций для определения подлинности препаратов. • Охарактеризуйте кислотно-основные свойства рибофлавина. Опишите испытания, характеризующие эти свойства. • Объясните неустойчивость рибофлавина к действию кислот и щелочей. Напишите реакции гидролитического разложения препарата. • Охарактеризуйте светочувствительность рибофлавина. Напишите продукты его превращения под действием света. Укажите значение этого свойства для выбора условий хранения рибофлавина. ■ Выделите в рибофлавине асимметрические атомы углерода. ■ Какими особенностями химической структуры искомого ЛВ объясняются его окраска и флуоресценция? ■ Что происходит с ЛВ при действии химических веществ с восстановительными свойствами?
ПОНЯТИЕ ОБ АНТИБИОТИКАХ Антибиотики- синтезируемые микроорганизмами вещества, а также продукты их химической модификации (полусинтетические антибиотики), которые способны подавлять рост микроорганизмов, а также вирусов и клеток (проявлять цитостатическое или цитоцидное действие). Некоторые антибиотики получают из неприродных полупродуктов. Это синтетические антибиотики, например хлорамфеникол. Иногда к антибиотикам относят антибактериальные вещества, выделенные из растительных и животных тканей. Большинство антибиотиков получают в промышленности микробиологическим синтезом. Антибиотики обладают высокой биологической активностью. Например, бензилпенициллин в концентрации 1 мкг/мл оказывает выраженное бактерицидное действие по отношению к чувствительным к нему бактериям. По мере использования антибиотиков в качестве ЛС относительно быстро появляются резистентные штаммы микроорганизмов, устойчивые к их действию. Появление устойчивости связано с выработкой микроорганизмами специфических ферментов, которые разрушают молекулы антибиотиков. Это приводит к потере их активности. По этой причине применяют комбинации нескольких антибиотиков, обладающих различными механизмами действия. В некоторых случаях одновременно применяют антибиотик и сульфаниламидные ЛС. В настоящее время известно более 10 тыс. природных и синтетических антибиотиков. Более 100 из них применяют в медицине и ветеринарии. Мировое производство антибиотиков составляет около 50 тыс. тонн в год. История применения антибиотиков начинается с 1929 г., когда впервые была обнаружена гибель стафилококковых бактерий (Staphylococcus) при контакте с зеленой плесенью (плесневого гриба)Penicillium notatum. Было установлено (1940), что биологической активностью обладало химическое соединение, впервые выделенное из плесени, - пенициллин. Пенициллин применяли во время Второй мировой войны. Оказалось, что антибиотическое действие пенициллинов проявляется за счет р-лактамного цикла. Классификация антибиотиков Первоначально антибиотики делили на группы, исходя из источников их выделения (пенициллины, стрептомицины, цефалоспорины и др.). В настоящее время в медицине применяется классификация антибиотиков по спектру действия. • Антибиотики, действующие только на грамположительные микробы (стафилококки, стрептококки, пневмококки и др.). Спектр их действия сравнительно узкий. К ним относятся бензилпенициллин, эритромицин, альбомицин, грамицидин С, бацитрацин и др. • Антибиотики, действующие как на грамположительные, так и на грамотрицательные организмы (кишечная палочка, палочка дифтерии или брюшного тифа и др.). Это антибиотики широкого спектра действия. К ним относятся стрептомицин, хлоромицин, тетрациклины, неомицин, канамицин и др. Грамположительные и грамотрицательные микроорганизмы различаются окраской их протоплазмы при действии красителей - генцианового фиолетового или метилового фиолетового либо йода. Грамположительные микроорганизмы образуют окрашенный комплекс, не обесцвечивающийся под действием спирта (окраска по Граму); грамотрицательные микроорганизмы не окрашиваются. • Антибиотики, действующие на грибки. К ним относятся группа полиеновых антибиотиков (нистатин, кандицидин, трихомицин и др.), антимицин и др. • Антибиотики, действующие как на микроорганизмы, так и на опухолевые (раковые) клетки, - актиномицины, митомицин, саркомицин, азасерин, пуромицин и др. Химическая классификацияпозволяет изучать зависимость между химической структурой, физико-химическими свойствами и механизмами действия антибиотиков. При этом природные и полусинтетические антибиотики могут быть разделены на следующие группы: - антибиотики алициклического строения (тетрациклины); - антибиотики ароматического ряда (группа левомицетина); - антибиотики гетероциклической структуры (пенициллины, цефалоспорины); - антибиотики-аминогликозиды (стрептомицин, канамицин, гентамицин, амикацин); - антибиотики-макролиды (эритромицин, азитромицин). Получение антибиотиков Антибиотики тетрациклинового и пенициллинового ряда, антибиотики-гликозиды получают микробиологическим синтезом на основе плесневых или лучистых грибов. Это неустойчивые соединения, которые выпускаются в виде стерильных порошков для инъекций или в ампулах. Полусинтетические антибиотики (полусинтетические пенициллины, цефалоспорины, тетрациклины) получают сочетанием микробиологического и химического синтеза (химической модификацией природных антибиотиков). Как правило, эти вещества более стабильны по сравнению с природными и их выпускают в виде таблеток, капсул, суспензий. Для получения синтетических антибиотиков, имеющих несложную химическую структуру (левомицетин и его производные), применяют химический синтез из органических соединений. Промышленный микробиологический синтез включает несколько стадий: - выбор высокопроизводительных штаммов продуцента (до 45 тыс. ЕД/мл) и питательных сред для него; - процесс биосинтеза; - выделение антибиотика из культуральной жидкости и его очистка. Природные штаммы в большинстве своем малоактивны и не могут использоваться для промышленных целей. Поэтому после отбора наиболее активного природного штамма для повышения его продуктивности применяют различные мутагены, вызывающие стойкие наследственные изменения. Эффективными мутагенами являются мутагены физической природы - ультрафиолетовое и рентгеновское излучение, быстрые нейтроны или химические вещества. Использование мутагенов позволяет не только повысить продуктивность природного штамма, но и получать штаммы с новыми неизвестными для природного микроорганизма свойствами. Большое значение для биосинтеза антибиотика имеет подбор рационального состава питательных сред. Выбор метода выделения антибиотика из культуральной жидкости зависит от его химической природы. Это может быть адсорбция на различных адсорбентах, ионный обмен на различных катионои анионообменниках, экстракция различными органическими растворителями из раствора с тем или иным значением рН, осаждение. Очистка антибиотика производится хроматографическими методами (хроматография на оксиде алюминия, целлюлозе, ионитах) или противоточной экстракцией. Очищенные антибиотики подвергают лиофильной сушке. После получения кристаллического антибиотика проводят испытания его чистоты. Для этого определяют его элементный состав и физико-химические константы (температуру плавления, молекулярную массу, светопоглощения в видимой, УФ- и ИК-областях спектра, удельное вращение раствора). Исследуют также антибактериальную активность, стерильность и токсичность антибиотика. Токсичность антибиотиков определяют на экспериментальных животных, которым в течение определенного периода времени внутривенно, внутрибрюшинно, внутримышечно или иным путем вводят различные дозы изучаемого антибиотика (см. главу 1). При отсутствии внешних изменений в поведении животных в течение 12-15 сут считают, что испытуемый антибиотик не обладает заметными токсическими свойствами. При более глубоком исследовании выясняют, обладает ли данный антибиотик скрытой токсичностью и влияет ли на отдельные ткани и органы животных. Одновременно для характеристики механизма антибактериальных свойств исследуют, является ли антибиотик бактериостатическим или бактерицидным. Затем изучают терапевтические свойства антибиотика. Экспериментальных животных заражают определенным видом патогенного микроба. Минимальное количество антибиотика, способствующее предохранению животного от смертельной дозы инфекции, является минимальной терапевтической дозой.Чем больше отношение токсичной дозы антибиотика к терапевтической, тем выше терапевтический индекс. Если терапевтическая доза равна токсической или приближается к ней (низкий терапевтический индекс), применение антибиотика в лечебной практике не разрешается. Стандартизация антибиотиков.За единицу антибиотической активностипринимают минимальное количество антибиотика, способное подавить развитие или задержать рост стандартного штамма тест-микроба в определенном объеме питательной среды. Величину биологической активности антибиотиков выражают обычно в условных единицах дозы(ЕД), содержащихся в 1 мл раствора (ЕД/мл) или в 1 мг препарата (ЕД/мг). Например, за единицу антибиотической активности пенициллина принимают его минимальное количество, способное задерживать рост золотистого стафилоккока стандартного штамма 209 в 50 мл питательного бульона. Для стрептомицина за единицу активности принимают минимальное количество антибиотика, задерживающее рост E. coli в 1 мл питательного бульона. Для антибиотиков, полученных химическим синтезом, биологическую активность выражают в массовых единицах (мкг/мг). Например, установлено, что 1 мг чистого основания стрептомицина эквивалентен 1000 единицам биологической активности (ЕД). Следовательно, 1 ЕД активности стрептомицина эквивалентна 1 микрограмму (мкг) чистого основания этого антибиотика. Единица биологической активности антибиотика не всегда совпадает с 1 мкг. Например, для бензилпенициллина 1 ЕД эквивалентна примерно 0,6 мкг, так как 1 мг антибиотика соответствует 1667 ЕД. Методы анализа антибиотиков.Для идентификации антибиотиков могут быть использованы различные хромогенные (цветные) реакции на соответствующие функциональные группы; спектральные характеристики в видимой, УФ-, ИК-областях спектра; хроматографические методы. Для количественного определения антибиотиков используют биологические, химические и физико-химические методы. Биологические методы основаны на действии антибиотика на тест-организм, чувствительный к данному антибиотику. При этом используют способность молекул антибиотика диффундировать в агаровых средах. Оценивается размер зоны, в которой используемые тест-организмы не развиваются. Этот размер зависит от химической природы антибиотика, его концентрации, рН и состава агаровой среды, температуры. Для биотестирования используют также турбидиметрию - метод количественного анализа по интенсивности света, поглощенного взвешенными частицами - клетками микроорганизмов. При добавлении определенных количеств антибиотиков наблюдается задержка роста клеток микроорганизмов (бактериостатический эффект), а затем их гибель (бактерицидный эффект). При этом снижается светопоглощение пробы. В качестве альтернативного турбидиметрии метода может быть использован нефелометрический метод, в котором оценивают интенсивность рассеянного света при добавлении антибиотика. Для количественного определения антибиотиков применяют спектрофотометрические методы. ФАРМАКОПЕЙНАЯ СТАТЬЯ ВОДА ОЧИЩЕННАЯ (ФС 42-0324-09) (ИЗВЛЕЧЕНИЯ) Настоящая фармакопейная статья распространяется на воду очищенную, получаемую из воды питьевой методами дистилляции, ионного обмена, обратного осмоса, комбинацией этих методов или другим способом и применяемую для приготовления нестерильных лекарственных средств, воды для инъекций, а также для проведения испытаний лекарственных средств. Вода очищенная не должна содержать антимикробных консервантов или других добавок. Описание.Бесцветная прозрачная жидкость без запаха. pH.От 5,0 до 7,0. К 100 мл воды прибавляют 0,3 мл насыщенного раствора калия хлорида и определяют pH раствора потенциометрически. Кислотность и щелочность.К 20 мл воды очищенной прибавляют 0,05 мл 0,1% раствора фенолового красного. Если появилась желтая окраска, то она должна измениться на красную от прибавления не более 0,10 мл 0,01 моль/л раствора натрия гидроксида. Если появилась красная окраска, то она должна измениться на желтую от прибавления не более 0,15 мл 0,01 М раствора хлористоводородной кислоты. Сухой остаток.100 мл воды очищенной выпаривают досуха и сушат при температуре от 100 до 105 °С до постоянной массы. Остаток не должен превышать 0,001%. Восстанавливающие вещества.100 мл воды очищенной доводят до кипения, прибавляют 1 мл 0,02 моль/л раствора калия перманганата и 2 мл кислоты серной разведенной 16%, кипятят 10 мин; розовая окраска должна сохраниться. Диоксид углерода.При взбалтывании воды очищенной с равным объемом известковой воды в наполненном доверху и хорошо закрытом сосуде не должно быть помутнения в течение 1 ч. Нитраты и нитриты.К 5 мл воды очищенной осторожно прибавляют 1 мл свежеприготовленного раствора дифениламина; не должно появляться голубого окрашивания Аммоний.10 мл воды очищенной должны выдерживать испытание на аммоний с использованием эталонного раствора, содержащего 1 мл стандартного раствора аммоний-иона (2 мкг/мл) и 9 мл воды, свободной от аммиака (не более 0,00002%). Примечание. Стандартный раствор аммоний-иона (2 мкг/мл) готовят разбавлением стандартного раствора аммоний-иона (200 мкг/мл) водой, свободной от аммиака. Хлориды.К 10 мл воды очищенной прибавляют 0,5 мл азотной кислоты, 0,5 мл 2% раствора серебра нитрата, перемешивают и оставляют на 5 мин. Не должно быть опалесценции. Сульфаты.К 10 мл воды очищенной прибавляют 0,5 мл хлористоводородной кислоты разведенной 8,3% и 1 мл 5% раствора бария хлорида, перемешивают и оставляют на 10 мин. Не должно быть помутнения. Кальций и магний.К 100 мл воды очищенной прибавляют 2 мл буферного раствора аммония хлорида pH 10,0, 50 мг индикаторной смеси протравного черного 11 и 0,5 мл 0,01 моль/л раствора эдената; должна наблюдаться чисто голубая окраска раствора. Тяжелые металлы.120 мл испытуемой воды очищенной упаривают до объема 20 мл. 10 мл оставшейся после упаривания воды должны выдерживать испытание на тяжелые металлы с использованием эталонного раствора, содержащего 1 мл стандартного раствора свинец-иона (5 мкг/мл) и 9 мл испытуемой воды очищенной (не более 0,00001% в испытуемой воде очищенной). Примечание. Стандартный раствор свинец-иона (5 мкг/мл) готовят разбавлением стандартного свинец-иона (100 мкг/мл) испытуемой водой очищенной. Микробиологическая чистота.Не более 100 микроорганизмов в 1 мл при отсутствии бактерий сем.Enterobacteriaceae, Staphylococcus aureus, Pseudomonas aeruginosa. Испытания проводят методом мембранной фильтрации. Объем образца для испытания должен составлять не менее 50 мл. Хранение и распределение.Вода очищенная хранится и распределяется в условиях, предотвращающих рост микроорганизмов и исключающих возможность любой другой контаминации. ВОДА ДЛЯ ИНЪЕКЦИЙ (ФС 42-0325-09) Настоящая фармакопейная статья распространяется на воду для инъекций, получаемую из воды очищенной и применяемую в качестве растворителя для приготовления инъекционных лекарственных средств для парентерального применения. Вода для инъекций должна выдерживать испытания, приведенные в статье «Вода очищенная», должна быть апирогенной, не содержать антимикробных веществ и других добавок. При изготовлении стерильных лекарственных средств, которые изготавливают в асептических условиях и не подвергают последующей стерилизации, вода для инъекций должна быть стерильной. Микробиологическая чистота.Не более 10 микроорганизмов в 100 мл при отсутствии бактерий сем.Enterobacteriaceae, Staphylococcus aureus, Pseudomonas aeruginosa. Испытания проводят методом мембранной фильтрации. Объем образца для испытания составляет 200 мл. Бактериальные эндотоксины.Менее 0,25 ЕЭ/мл. Хранение и распределение.Воду для инъекций используют свежеприготовленной или хранят и используют в условиях, предотврающихся рост микроорганизмов и исключающих возможность любой другой контаминации, но не более 1 сут.
ПРИЛОЖЕНИЕ 2 Журнал регистрации результатов контроля лекарственных средств на подлинность
Журнал регистрации результатов органолептического, физического и химического контроля внутриаптечной заготовки, лекарственных форм, изготовленных по индивидуальным рецептам (требованиям лечебных организаций), концентратов, полуфабрикатов, тритураций, спирта этилового и фасовки
| |||||||||||||||||||||||||||||||||||||||||||||||||||
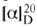 от -128 до -142.
от -128 до -142.