Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Климатические изменения на ЗемлеПогода — это ежедневное состояние атмосферы. Погода является хаотичной не линеарной динамической системой. Климат — это усредненное состояние погоды и он, напротив, стабилен и предсказуем. Климат включает в себя такие показатели как средняя температура, количество осадков, количество солнечных дней и другие переменные, которые могут быть измерены в каком-либо определенном месте. Однако на Земле происходят и такие процессы, которые могут оказывать влияние на климат. Билет 74. 1.Матричныйсинтезкакспецифическоесвойствоживого. Матричный cинтез. 1. Полимеризация и поликонденсация, при которых строение образующегося полимера и (или) кинетика процесса определяются другими макромолекулами (матрицами), находящимися в непосредственном контакте с молекулами одного или неск. мономеров и растущими цепями. Пример матричного синтеза в живой природе - синтез нуклеиновых кислот и белков. в котором роль матрицы играют ДНК и РНК, а состав и порядок чередования звеньев в растущей (дочерней) цепи однозначно определяются составом и структурой матрицы.
Термин "матричный синтез " обычно используют при описании синтеза нуклеиновых кислот и белков. а при рассмотрении способов получения др. полимеров пользуются такими терминами, как матричные полиреакции, полимеризация, поликонденсация. Такой матричный синтез реализуется при условии хим. и стерич. соответствия (комплементарности) мономеров и растущей цепи, с одной стороны, и матрицы - с другой; при этом элементарные акты осуществляются между мономерами и растущими макромолекулами (а также олигомерами - при матричной поликонденсации), связанными с матрицей.  Обычно мономеры и олигомеры обратимо связываются с матрицей достаточно слабыми межмолекулярными взаимодействиями - электростатическими, донорно-акцепторным и т.д. Дочерние цепи практически необратимо ассоциируют с матрицей ("узнают" матрицу) только после того, как достигнут некоторой определенной длины, зависящей от энергии взаимодействия между звеньями матрицы и дочерней цепи. "Узнавание" матрицы растущей цепью - необходимая стадия матричный синтез; дочерние цепи практически всегда содержат фрагмент или фрагменты, образовавшиеся по "обычному" механизму, т. е. без влияния матрицы. Скорость матричный синтез может быть выше, ниже или равна скорости процесса в отсутствие матрицы (кинетический матричный эффект). Структурный матричный эффект проявляется в способности матрицы влиять на длину и химическое строение дочерних цепей (в том числе их стерическую структуру), а если в матричном синтезе участвуют два или более мономера - то также на состав сополимера и способ чередования звеньев. Методом матричного синтеза получают полимер-полимерные комплексы, обладающие более упорядоченной структурой, чем поликомплексы, синтезируемые простым смешением растворов полимеров, а также поликомплексы, которые нельзя получить из готовых полимеров вследствие нерастворимости одного из них. Матричный синтез - перспективный метод получения новых полимерных материалов. Термин "матричный синтез " обычно используют при описании синтеза нуклеиновых кислот и белков. а при рассмотрении способов получения др. полимеров пользуются такими терминами, как матричные полиреакции, полимеризация, поликонденсация.. 2. Химические реакции, в которых строение образующегося мономолекулярного органического соединения и (или) кинетика процесса определяется атомомметалла (так называемый темплатный синтез). Атом металла может входить в состав соли или комплексного соединения и выполнять в матричном синтезе различные функции. Он координирует молекулы и тем самым ориентирует их реагирующие фрагменты (так называемый кинетический эффект в матричном синтезе); в этом случае образование целевого продукта без участия в реакции атома металла вообще не происходит. Атом металла может связывать в комплекс только один из конечных продуктов, которые образуются в равновесной реакции (так называемый термодинамический эффект в матричном синтезе); образование целевого продукта может происходить и в отсутствие металла, однако под влиянием последнего выход реакции существенно возрастает. Часто оба эти механизма проявляются одновременно. Известны случаи, когда равновесная реакция осуществляется на стадии образования промежуточного продукта. Последний фиксируется в виде металлокомплекса, и дальнейшее превращение идет специфическим образом (так называемый равновесный эффект в матричном синтезе). Возможны и другие механизмы матричного синтеза. Матричный синтез обычно используют для синтеза циклических соединений. Типичный пример матричного синтеза - получение коррина (промежуточного вещества в синтезе витамина В12)
2. Классификация тератогенов. В классификации пороков у ребенка выделяют несколько групп пороков. В зависимости от времени воздействия вредных факторов и объекта поражения выделяют следующие формы пороков развития. 1.Гаметопатии – патологические изменения в половых клетках, произошедшие до оплодотворения и приводящие к спонтанному прерыванию беременности, врожденным порокам развития, наследственным заболеваниям. Это наследственно обусловленные врожденные пороки, в основе которых лежат спорадические мутации в половых клетках родителей или унаследованные мутации у более отдаленных предков. 2.Бластопатии – это повреждения зиготы в первые 2 недели после оплодотворения (до момента завершения дифференциации зародышевых листков и начала маточно-плацентарного кровообращения), вызывающие гибель зародыша, внематочную беременность, пороки развития с нарушением формирования оси зародыша (симметричные, асимметричные и неполностью разделившиеся близнецы, циклопия, аплазия почек и др.). 3.Эмбриопатии – согласно классификация пороков у ребенка - это поражения зародыша от момента прикрепления его к стенке матки (15-й день после оплодотворения) до сформирования плаценты (75-й день внутриутробной жизни), проявляющиеся пороками развития отдельных органов и систем, прерыванием беременности. Поскольку в эмбриональный период происходит формирование основных морфологических структур органов, то естественно, что большинство врожденных пороков образуется именно в этот период.Наличие критических периодов, т.е. стадий интенсивной дифференцировки органов, когда они наиболее легко повреждаются, определяет существование временной специфичности для различных органов. Так, воздействие повреждающего фактора на 4-6-й неделе внутриутробного развития часто ведет к формированию у плода порока сердца, на 12-14-й неделе – порока развития половых органов и т.д. Локализация дефекта также зависит от интенсивности повреждающего воздействия. 4.Фетопатии – общее название болезней плода, возникающих под воздействием неблагоприятных факторов с 11-й недели внутриутробной жизни до начала родов. Важнейшая роль в формировании фетопатии принадлежит состоянию плацентарного комплекса. Признаками фетопатии становятся: задержка внутриутробного развития; врожденные пороки в результате обратного развития зародышевых структур (кишечный свищ, открытые артериальный проток или овальное окно) или эмбриональных щелей (расщелины губы, неба, позвоночника, уретры); сохранение первоначального расположения органов (крипторхизм); гипоплазии и дисплазии отдельных органов и тканей (дисплазия почек, микроцефалия, гидроцефалия и др.); избыточное разрастание соединительной и других тканей при инфекциях (катаракта и др.); врожденные болезни (гемолитическая болезнь новорожденных, гепатиты, циррозы, пневмонии, миокардиты, энцефалиты и др.). Фетопатии нередко приводят к преждевременным родам, асфиксии при рождении, метаболическим и другим нарушениям адаптации новорожденных к внеутробной жизни и являются наиболее частыми причинами неонатальных болезней и смертности. К врожденным порокам относятся следующие нарушения развития. 1.Агенезия – полное врожденное отсутствие органа. 2.Аплазия – врожденное отсутствие органа или выраженное его недоразвитие. Отсутствие некоторых частей органа называется термином, включающим в себя греч. слово olygos («малый») и название пораженного органа. Например, олигодактилия – отсутствие одного или нескольких пальцев. 3.Гипоплазия – недоразвитие органа, проявляющееся дефицитом относительной массы или размеров органа. 4.Гипотрофия – уменьшенная масса тела новорожденного или плода. 5.Гиперплазия (гипертрофия) – повышенная относительная масса (или размеры) органа за счет увеличения количества (гиперплазия) или объема (гипертрофия) клеток. 6.Макросомия (гигантизм) – увеличенные длина и масса тела. Термины «макросомия» и «микросомия» нередко применяются для обозначения соответствующих изменений отдельных органов. 7.Гетеротопия – расположение клеток, тканей либо целых участков органа в другом органе или в тех зонах того же органа, где их быть не должно. 8.Гетероплазия – расстройство разграничения некоторых видов ткани. Гетероплазии следует дифференцировать от метаплазий – вторичного изменения разграничения тканей, которое связывают с хроническим воспалением. 9.Эктопия – смещение органа, т.е. локализация его в несвойственном ему месте. Например, наличие почки в тазу, сердца – вне грудной клетки. Удвоение и увеличение в числе того или иного органа или части его. 10.Атрезия – полное отсутствие канала или естественного отверстия. 11.Стеноз – сужение канала или отверстия. 12.Неразделение (слияние) органов двух симметрично или асимметрично развитых однояйцевых близнецов. Название пороков, определяющих неразделение конечностей или их частей, начинается с греч. приставки syn («вместе»)– синдактилия, симподия (соответственно – неразделение пальцев и нижних конечностей). 13.Персистирование – обратное развитие морфологических структур, которые в норме исчезают к определенному периоду развития (артериальный проток или овальное окно у ребенка в возрасте старше 3 месяцев). Одной из форм персистирования является дизрафия (арафия)– незаращение эмбриональной щели (расщелины губы, неба, позвоночника и т.д.). 14.Дисхрония – нарушение темпов (ускорение или замедление) развития. Процесс может касаться клеток, тканей, органов или всего организма. Врожденные пороки могут проявляться и другими изменениями органов. Например, нарушением лобуляции (увеличение или уменьшение долей легкого или печени), образованием врожденных водянок (гидроцефалия, гидронефроз), инверсией – обратным (зеркальным) расположением органов.К неклассифицированным комплексам относят пороки, проявления которых не укладываются ни в один из известных синдромов.1)изменением наследственных структур (мутациями); 2)воздействием тератогенных факторов;3)воздействием и мутаций, и тератогенных факторов (пороки мультифакториального генеза).Среди пороков центральной нервной системы (ЦНС) различают пороки конечного мозга, обонятельного анализатора, стволовых отделов, мозжечка, спинного мозга и позвоночника, вентрикулярной системы и субарахноидального пространства.Наиболее распространенной классификацией пороков у ребенка является классификация, в основу которой положен анатомо-физиологический принцип деления тела человека на системы органов (ВОЗ, 1995г.).А. Врожденные пороки развития органов и систем:пороки ЦНС и органов чувств, ороки лица и шеи, пороки сердечно-сосудистой системы, пороки дыхательной системы, пороки органов пищеварения, пороки костно-мышечной системы, пороки мочевой системы, пороки половых органов, пороки эндокринных желез, пороки кожи и ее придатков ,пороки последа..Б. Множественные врожденные пороки: Хромосомные синдромы. Генные синдромы. Синдромы, обусловленные экзогенными факторами. Синдромы неустановленной этиологии. Множественные неуточненные пороки. 3.- Билет 75 1. РНК виды РНК и их биологическая роль. Рибонуклеи́новые кисло́ты (РНК) — нуклеиновые кислоты, полимерынуклеотидов, в состав которых входят остаток ортофосфорной кислоты, рибоза (в отличие от ДНК, содержащей дезоксирибозу) и азотистые основания — аденин, цитозин, гуанин и урацил (в отличие от ДНК, содержащей вместо урацила тимин). Эти молекулы содержатся в клетках всех живых организмов, а также в некоторых вирусах Клеточные РНК образуются в ходе процесса, называемого транскрипцией, то есть синтеза РНК на матрице ДНК, осуществляемого специальными ферментами — РНК-полимеразами. Затем матричные РНК (мРНК) подвергаются сплайсингу и принимают участие в процессе, называемом трансляцией. Трансляция — это синтез белка на матрице мРНК при участии рибосом. Другие РНК после транскрипции подвергаются химическим модификациям, и после образования вторичной и третичной структур выполняют функции, зависящие от типа РНК. Для одноцепочечных РНК характерны разнообразные пространственные структуры, в которых часть нуклеотидов одной и той же цепи спарены между собой. Некоторые высокоструктурированные РНК принимают участие в синтезе белка клетки, например, транспортные РНК служат для узнавания кодонов и доставки соответствующих аминокислот к месту синтеза белка, а рибосомные РНК служат структурной и каталитической основой рибосом. Однако функции РНК в современных клетках не ограничиваются их ролью в трансляции. Так малые ядерные РНК принимают участие в сплайсингеэукариотическихматричных РНК и других процессах. Помимо того, что молекулы РНК входят в состав некоторых ферментов (например, теломеразы) у отдельных РНК обнаружена собственная энзиматическая активность, способность вносить разрывы в другие молекулы РНК или, наоборот, «склеивать» два РНК-фрагмента. Такие РНК называются рибозимами. Геномы ряда вирусов состоят из РНК, то есть у них она играет роль, которую у высших организмов выполняет ДНК. На основании разнообразия функций РНК в клетке была выдвинута гипотеза, согласно которой РНК — первая молекула, которая была способна к самовоспроизведению в добиологических системах. Матричная (информационная) РНК — РНК, которая служит посредником при передаче информации, закодированной в ДНК к рибосомам, молекулярным машинам, синтезирующим белки живого организма. Кодирующая последовательность мРНК определяет последовательность аминокислот полипептидной цепи белка [29]. Однако подавляющее большинство РНК не кодируют белок. Эти некодирующие РНК могут транскрибироваться с отдельных генов (например, рибосомальные РНК) или быть производными интронов [30]. Классические, хорошо изученные типы некодирующих РНК — это транспортные РНК (тРНК) и рРНК, которые участвуют в процессе трансляции[31]. Существуют также классы РНК, ответственные за регуляцию генов, процессинг мРНК и другие роли. Кроме того, есть и молекулы некодирующих РНК, способные катализировать химические реакции, такие, как разрезание и лигирование молекул РНК[32]. По аналогии с белками, способными катализировать химические реакции — энзимами (ферментами), каталитические молекулы РНК называются рибозимами. Роль разных типов РНК в синтезе белка (по Уотсону) Информация о последовательности аминокислот белка содержится в мРНК. Три последовательных нуклеотида (кодон) соответствуют одной аминокислоте. В эукариотических клетках транскирибированный предшественник мРНК или пре-мРНК процессируется с образованием зрелой мРНК. Процессинг включает удаление некодирующих белок последовательностей (интронов). После этого мРНК экспортируется из ядра в цитоплазму, где к ней присоединяются рибосомы, транслирующие мРНК с помощью соединённых с аминокислотами тРНК. В безъядерных клетках (бактерии и археи) рибосомы могут присоединяться к мРНК сразу после транскрипции участка РНК. И у эукариот, и у прокариот цикл жизни мРНК завершается её контролируемым разрушением ферментами рибонуклеазами[29]. Транспортные (тРНК) — малые, состоящие из приблизительно 80 нуклеотидов, молекулы с консервативной третичной структурой. Они переносят специфические аминокислоты в место синтеза пептидной связи в рибосоме. Каждая тРНК содержит участок для присоединения аминокислоты и антикодон для узнавания и присоединения к кодонам мРНК. Антикодон образует водородные связи с кодоном, что помещает тРНК в положение, способствующее образованию пептидной связи между последней аминокислотой образованного пептида и аминокислотой, присоединённой к тРНК [30]. Рибосомальные РНК (рРНК) — каталитическая составляющая рибосом. Эукариотические рибосомы содержат четыре типа молекул рРНК: 18S, 5.8S, 28S и 5S. Три из четырёх типов рРНК синтезируются в ядрышке. В цитоплазме рибосомальные РНК соединяются с рибосомальными белками и формируют нуклеопротеин, называемый рибосомой[29]. Рибосома присоединяется к мРНК и синтезирует белок. рРНК составляет до 80 % РНК, обнаруживаемой в цитоплазме эукариотической клетки [33]. Необычный тип РНК, который действует в качестве тРНК и мРНК (тмРНК) обнаружен во многих бактериях и пластидах. При остановке рибосомы на дефектных мРНК без стоп-кодонов тмРНК присоединяет небольшой пептид, направляющий белок на деградацию [34] 2. Иерапевтическое клонирование. Понятие о стволовых клетках. Терапевтическом клонировании используется процесс, известный как пересадка ядер соматических клеток, (замена ядра клетки, исследовательское клонирование и клонирование эмбриона), состоящий в изъятии яйцеклетки (ооцита) из которой было удалено ядро, и замена этого ядра ДНК другого организма. После многих митотических делений культуры (митозов культуры), данная клетка образует бластоцисту (раннюю стадию эмбриона состоящую из приблизительно 100 клеток) с ДНК почти идентичным первичному организму. Цель данной процедуры — получение стволовых клеток, генетически совместимых с донорским организмом. Например, из ДНК больного болезнью Паркинсона можно получить эмбриональные стволовые клетки, которые можно использовать для его лечения, при этом они не будут отторгаться иммунной системой больного. В настоящее время такая терапия в России не осуществляется, и развитие технологии клонирования было приостановлено до того момента, когда в правительстве наконец решат разрешить исследования в этой области. Стволовые клетки, полученные путем терапевтического клонирования, применяются для лечения многих заболеваний. Кроме этого, в настоящее время ряд методов с их использованием находятся на стадии разработки (лечение некоторых видов слепоты[1], повреждений спинного мозга[2] и др.). По данным от 2006 года клонирование в терапевтических целях применяют в Великобритании, Бельгии и Швеции. В Японии, Сингапуре, Израиле и Корее разрешены исследования в этой областиhttp://ru.wikipedia.org/wiki/%D0%A2%D0%B5%D1%80%D0%B0%D0%BF%D0%B5%D0%B2%D1%82%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%BE%D0%B5_%D0%BA%D0%BB%D0%BE%D0%BD%D0%B8%D1%80%D0%BE%D0%B2%D0%B0%D0%BD%D0%B8%D0%B5 - cite_note-2. В Великобритании терапевтическое клонирование разрешено в научно-исследовательских целях и включено в Human Fertilization and Embryology Act (Акт об Оплодотворении и клонировании человека) в 2001 году. Во многих других странах, терапевтическое клонирование запрещено, хотя законы постоянно обсуждаются и изменяются. 8.12.2003 страны ООН проголосовали против запрета на репродуктивное и терапевтическое клонирование, предложенного Коста-Рикой. 3.- Билет 76. 1. Роль РНК в реализации наследственной информации. Синтез белка. Белки синтезируются живыми организмами из аминокислот на основе информации, закодированной в генах. Каждый белок состоит из уникальной последовательности аминокислот, которая определяется нуклеотидной последовательностью гена, кодирующего данный белок. Генетический код составляется из трёхбуквенных «слов», называемых кодонами; каждый кодон отвечает за присоединение к белку одной аминокислоты: например, сочетание АУГ соответствует метионину. Поскольку ДНК состоит из четырёх типов нуклеотидов, то общее число возможных кодонов равно 64; а так как в белках используется 20 аминокислот, то многие аминокислоты определяются более, чем одним кодоном. Гены, кодирующие белки сначала транскрибируются в последовательность нуклеотидов матричной РНК (мРНК) белками РНК-полимеразами. У прокариот мРНК может считываться рибосомами в аминокислотную последовательность белков сразу после транскрипции, а у эукариот она транспортируется из ядра в цитоплазму, где находятся рибосомы. Скорость синтеза белков выше у прокариот и может достигать 20 аминокислот в секунду[22]. Процесс синтеза белка на основе молекулы мРНК называется трансляцией. Во время начальной стадии биосинтеза белков, инициации, обычно метиониновый кодон узнаётся малой субъединицей рибосомы, к которой при помощи белковых факторов инициации присоединена метиониновая транспортная РНК (тРНК). После узнавания стартового кодона к малой субъединице присоединяется большая субъединица и начинается вторая стадия трансляции — элонгация. При каждом движении рибосомы от 5' к 3' концу мРНК считывается один кодон путём образования водородных связей между тремя нуклеотидами (кодоном) мРНК и комплементарным ему антикодоном транспортной РНК, к которой присоединена соответствующая аминокислота. Синтез пептидной связи катализируется рибосомальной РНК (рРНК), образующей пептидилтрансферазный центр рибосомы. Рибосомальная РНК катализирует образование пептидной связи между последней аминокислотой растущего пептида и аминокислотой, присоединённой к тРНК, позиционируя атомы азота и углерода в положении, благоприятном для прохождения реакции. Ферменты аминоацил-тРНК-синтетазы присоединяют аминокислоты к их тРНК. Третья, и последняя стадия трансляции, терминация, происходит при достижении рибосомой стоп-кодона, после чего белковые факторы терминациигидролизуют последнюю тРНК от белка, прекращая его синтез. Таким образом, в рибосомах белки всегда синтезируются от N- к C-концу. 2. Клонирование и вопросы трансплантации. Бурный научно-технический прогресс ХХ столетия уже к началу 40-50-х годов создал условия для развития новой области реконструктивной хирургии – трансплантации органов. Пока трансплантологические операции исчислялись единицами и носили экспериментальный характер, они вызывали удивление и даже одобрение. 1967 год — год, когда К. Бернардом была произведена первая в мире пересадка сердца. За ней в течение 1968 года последовали более сотни подобных операций. В нашей стране первая аллотрансплантация – пересадка почки от трупа выполнена Ю.Вороным в 1931. Первая в России успешная пересадка сердца в клинике была проведена В. Шумаковым в 1986г. Эти годы называли в прессе временем «трансплантационной эйфории». Новое направление медицины призывают обеспечивать замену утраченных функций поврежденных органов (или тканей) для сохранения жизнедеятельности организма. Стремительный выход трансплантации на уровень массовой практики повлек за собой создание многочисленных деклараций и документов этичекого характера, инструкций и новых законов для решения возникших вопросов. Пересадка сердца, как никакое другое достижение современной культуры, с особой остротой поставило перед ней блок философско-антропологических проблем: что такое человек? Что определяет личность? В чем заключается человеческая самоидентичность? Расширение практики трансплантологии не снимает антропологическую «остроту» и сопровождается усилением этико-правовой напряженности вокруг этого вида медицинской деятельности. Так, в докладе, открывающем в 2008 году городскую научно-практическую конференцию «Актуальные вопросы трансплантации органов» в г. Москве, было отмечено, что развитие клинической трансплантологии в нашей стране сопряжено со значительными трудностями, значительно большими, чем в других странах. «Казалось бы, необходимость пересадки органов очевидна, однако специалисты констатируют, что наше общество и многие врачи относятся к трансплантации с недоверием. Имеет место непонимание общественностью всей значимости работы трансплантологических служб, что наблюдается даже в среде медицинских работников. Нередко трансплантологам приходится сталкиваться с их прямым противодействием. Это говорит о низком уровне пропаганды гуманистической сути донорства как акта дарения…» Клони́рование (англ. cloning от др.-греч. κλών — «веточка, побег, отпрыск») — в самом общем значении — точное воспроизведение какого-либо объекта N раз. Объекты, полученные в результате клонирования, называются клоном. Причём как каждый по отдельности, так и весь ряд. Клони́рование челове́ка — действие, заключающееся в формировании и выращивании принципиально новых человеческих существ, точно воспроизводящих не только внешне, но и на генетическом уровне того или иного индивида, ныне существующего или ранее существовавшего. Кклон, клонирование первоначально использовались в микробиологии и селекции, после — в генетике, в связи с успехами которой и вошли в общее употребление. Надо добавить, что их популяризации в значительной мере способствовали также литература, киноискусство и компьютерные игры. Технология:ока технология клонирования человека не отработана. И здесь встаёт ряд как теоретических, так и технических вопросов. Однако, уже сегодня есть методы, позволяющие с большой долей уверенности говорить, что в главном вопрос технологии решён. Наиболее успешным из методов клонирования высших животных оказался метод «переноса ядра». Именно он был применён для клонирования овцы Долли в Великобритании, которая, как известно, прожила достаточное число лет (6), чтобы можно было говорить об успехе эксперимента. По мнению учёных, эта техника является лучшей из того, что мы имеем сегодня, чтобы приступить к непосредственной разработке методики клонирования человека. Более ограниченным и проблематичным выглядит метод партеногенеза, в котором индуцируется деление и рост неоплодотворённой яйцеклетки, даже если он будет реализован, то позволит говорить только об успехах в клонировании индивидов женского пола. Так называемая технология «расщепления» эмбриона, хотя и должна давать генетически идентичных между собой индивидов, не может обеспечить их идентичности с «родительским» организмом, и поэтому технологией клонирования в точном смысле слова не является и как возможный вариант не рассматривается. Репродуктивное клони́рование человека — предполагает, что индивид, родившийся в результате клонирования, получает имя, гражданские права, образование, воспитание, словом — ведёт такую же жизнь, как и все «обычные» люди. Репродуктивное клонирование встречается со множеством этических, религиозных, юридических проблем, которые сегодня ещё не имеют очевидного решения. В некоторых государствах работы по репродуктивному клонированию запрещены на законодательном уровне[1][2]. Терапевти́ческое клони́рование челове́ка — предполагает, что развитие эмбриона останавливается в течение 14[источник?] дней, а сам эмбрион используется как продукт для получения стволовых клеток. Законодатели многих стран[уточнить] опасаются, что легализация терапевтического клонирования приведёт к его переходу в репродуктивное. Однако в некоторых странах (США[3], Великобритания) терапевтическое клонирование разрешено. 3. –, вызывающие травматизацию (поражение) слизистой оболочки ротовой полости, кишечника и даже кожи животных (липучка обыкновенная, люцерна малая, щетинник зеленый, ячмень, прицепник липучковый). В лесной и лесостепной зонах чаще встречаются щетинник зеленый, прицепник липучковый. Волчник, или волчье лыков народе называют волчьей ягодой. Это кустарник или мелкие деревца с ярко-красными ягодами, похожими на облепиху. Сок этого ядовитого растения, попавший на кожу, может вызвать боль, красноту, отек, и даже пузыри и язвы (глубокие дефекты кожи, после их заживления остаются рубцы). При попадании ягод или сока в желудок, признаки отравления будут такими: жжение во рту и глотке, затруднение глотания, слюнотечение, боли в желудке, понос, рвота. В моче появится кровь. Другие симптомы отравления будут похожи на симптомы при отравлении ландышем майским. 4. Синдром Клайнфелтера (дисгенезия семенных канальцев) — заболевание, обусловленное аномалией половых хромосом, характерным симптомом которого является нарушение сперматогенеза. Частота заболевания среди лиц с мужским фенотипом составляет 1:1100, среди мужчин, страдающих бесплодием,— 1:9, а среди олигофренов — 1:95. Билет 77. 1. Экспериментальные доказательства генетической роли нуклеиновых кислот. Известно, что бактерия Pneutnococcus pneumoniae имеет несколько форм. Вирулентность бактерии определяется наличием мукополисахаридной капсулы, расположенной па поверхности клетки. Эта капсула защищает бактерию от воздействий со стороны организма-хозяина. В результате, размножившиеся бактерии убивают зараженное животное. Бактерии этого штамма (S-штамм) образуют гладкие колонии. Авирулентные формы бактерий не имеют защитной капсулы и образуют шероховатые колонии (R-штамм). Микробиолог Фредерик Гриффитс в 1928 году инъецировал мышам живого пневмококка R-штамма вместе с S-штаммом, убитым высокой температурой (65°С). Спустя некоторое время ему удалось выделить из заражённых мышей живых пневмококков, обладающих капсулой. Таким образом, оказалось, что свойство убитого пневмококка - способность образовывать капсулу - перешло к живой бактерии, т.е. произошла трансформация. Поскольку признак наличия капсулы является наследственным, то следовало предположить, что какая-то часть наследственного вещества от бактерий штамма S перешла к клеткам штамма R. В 1944 году О.Т. Эвери, К.М. Маклеод и М. Маккарти показали, что такое же превращение типов пневмококков может происходить в пробирке, т.е. in vitro. Эти исследователи установили существование особой субстанции -"трансформирующего принципа", -экстракта из клеток штамма S, обогащенного ДНK. Как далее выяснилось, ДНK, выделенная из клеток S-штамма добавленная в культуру R-штамма, трансформировала часть клеток в S-форму, Клетки стойко передавали это свойство при дальнейшем размножении. Обработка "трансформирующего фактора" ДНК-азой, ферментом разрушающим ДНK, блокирована трансформацию. Эти данные впервые показали, что именно ДНК, а не белок, как полагали до тех пор, является наследственным материалом. 2. 1952г. Эксперимент Альфреда Херши и Марты Чейз.
Результаты этого эксперимента прямо показали, что ДНК родительских фагов проникает в бактерии и затем становиться составляющей развившихся новых фагов частиц.
3. 1957г. Опыты Френкеля - Конрата Френкель-Конрат работал с вирусом табачной мозаики (ВТМ). В этом вирусе содержится РНК, а не ДНК. Было известно, что разные штаммы вируса вызывают разную картину поражения листьев табака. После смены белковой оболочки "переодетые" вирусы вызывали картину поражения, характерную для того штамма, чья РНК была покрыта чужим белком. Следовательно, не только ДНК, но и РНК может служить носителем генетической информации. На сегодняшний день существуют сотни тысяч доказательств генетической роли нуклеиновых кислот. Приведенные три являются классическими. 2. Вопросы трансплантации. Виды трансплантации. Бурный научно-технический прогресс ХХ столетия уже к началу 40-50-х годов создал условия для развития новой области реконструктивной хирургии – трансплантации органов. Пока трансплантологические операции исчислялись единицами и носили экспериментальный характер, они вызывали удивление и даже одобрение. 1967 год — год, когда К. Бернардом была произведена первая в мире пересадка сердца. За ней в течение 1968 года последовали более сотни подобных операций. В нашей стране первая аллотрансплантация – пересадка почки от трупа выполнена Ю.Вороным в 1931. Первая в России успешная пересадка сердца в клинике была проведена В. Шумаковым в 1986г. Эти годы называли в прессе временем «трансплантационной эйфории». Новое направление медицины призывают обеспечивать замену утраченных функций поврежденных органов (или тканей) для сохранения жизнедеятельности организма. Стремительный выход трансплантации на уровень массовой практики повлек за собой создание многочисленных деклараций и документов этичекого характера, инструкций и новых законов для решения возникших вопросов. Пересадка сердца, как никакое другое достижение современной культуры, с особой остротой поставило перед ней блок философско-антропологических проблем: что такое человек? Что определяет личность? В чем заключается человеческая самоидентичность? Расширение практики трансплантологии не снимает антропологическую «остроту» и сопровождается усилением этико-правовой напряженности вокруг этого вида медицинской деятельности. Так, в докладе, открывающем в 2008 году городскую научно-практическую конференцию «Актуальные вопросы трансплантации органов» в г. Москве, было отмечено, что развитие клинической трансплантологии в нашей стране сопряжено со значительными трудностями, значительно большими, чем в других странах. «Казалось бы, необходимость пересадки органов очевидна, однако специалисты констатируют, что наше общество и многие врачи относятся к трансплантации с недоверием. Имеет место непонимание общественностью всей значимости работы трансплантологических служб, что наблюдается даже в среде медицинских работников. Нередко трансплантологам приходится сталкиваться с их прямым противодействием. Это говорит о низком уровне пропаганды гуманистической сути донорства как акта дарения…»
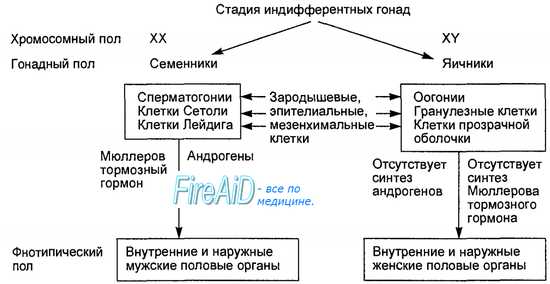
3. – Растения, нарушающие процессы тканевого дыхания (лен посевной, клевер в молодом виде, лядвенец рогатый в период цветения, манник плавающий, бухарник шерстистый и др.). При определенных условиях и в определенное время (чаще в жаркое и сухое) они накапливают значительное количество синильной кислоты, которая и вызывает отравление животных на пастбищах или при скармливании свежескошенной зеленой массы. Бывают случаи отравления и при скармливании животным сорго, суданской травы, вики и других культурных растений. 4, кошачий сосальщик (плоские черви)гельминтология=1-ротовая полость.2-глотка.3- к-к 4.брюшная присоска.5.-матка. 6-желточники 7-семенники. Билет 78 1. Синтез белка в клетке. Генетический код. Функции и-,т-,р-РНК. Одним из важнейших процессов, протекающих в клетке, является синтез белков. Клетка содержит тысячи белков, клетка должна непрерывно синтезировать белки для восстановления своих мембран, органоидов и т. п. Синтез белка требует больших затрат энергии. Источником этой энергии, как и для всех клеточных процессов, является АТФ. В ДНК используется четыре нуклеотида — аденин (А), гуанин (G), цитозин (С), тимин (T), которые в русскоязычной литературе обозначаются буквами А, Г, Ц и Т. Эти буквы составляют алфавит генетического кода. В РНК используются те же нуклеотиды, за исключением тимина, который заменён похожим нуклеотидом — урацилом, который обозначается буквой U (У в русскоязычной литературе). В молекулах ДНК и РНКнуклеотиды выстраиваются в цепочки и, таким образом, получаются последовательности генетических букв. Для построения белков в природе используется 20 различных аминокислот. Каждый белок представляет собой цепочку или несколько цепочек аминокислот в строго определённой последовательности. Эта последовательность определяет строение белка, а следовательно все его биологические свойства. Набор аминокислот также универсален почти для всех живых организмов. Реализация генетической информации в живых клетках (то есть синтез белка, кодируемого геном) осуществляется при помощи двух матричных процессов: транскрипции (то есть синтеза и-РНК на матрице ДНК) и трансляции генетического кода в аминокислотную последовательность (синтез полипептидной цепи на р-РНК). Для кодирования 20 аминокислот, а также сигнала «стоп», означающего конец белковой последовательности, достаточно трёх последовательных нуклеотидов. Набор из трёх нуклеотидов называется триплетом. Принятые сокращения, соответствующие аминокислотам и кодонам. иРНК - информационная - несёт закокодированную информацию о ДНК в рибосомы. в трансляции несет инфо о последовательности аминокислот белка. 2, Дифференциация мужской половой системы. При фертилизации, в зиготе, находящейся в репродуктивном тракте женского организма, на основе генетической программы первоначально формируется хромосомный, или генетический, пол человека. Затем в ходе развития эмбриона формируется гонадный пол, когда недифференцированные гонады развиваются либо в семенники, либо в яичники. В зависимости от гонадного пола у плода происходит дифференциация мужских или женских внутренних и наружных гениталий (формируется фенотипиче-ский пол). В целом указанные превращения называется половой дифференциацией человека (рис. 16.2).
3.-Поллиноз или сезонный аллергический риноконъюнктивит — сезонное заболевание, причиной которого является аллергическая реакция на пыльцу растений. Иногда также называемое сенной лихорадкой, хотя сено не является значимым фактором в генезе заболевания, а лихорадка не характерна для данной патологии. |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 550. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
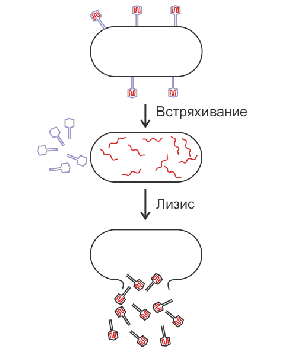 Как известно, фаг Т2 является вирусом, инфицирующим бактерию E. coli. фаговые частицы абсорбируются на наружной поверхности клетки, их материал проникает внутрь и примерно через 20 минут бактерия лизируется, освобождая большое количество фаговых частиц - потомков. В 1952 году Альфред Херши и Марта Чейз инфицировали бактерии фагами Т2, которые были мечены радиоактивными соединениями: ДНК - с помощью 32P. Белковая часть фага - 35S. После инфекции бактерии фагами, с помощью центрифугирования удалось выделить две фракции: пустые белковые оболочки фага и бактерии, инфицированных фаговой ДНК. Оказалось, что 80% метки 35S осталась в пустых фаговых оболочках, а 70% метки 32P - в инфицированных бактериях. Фаги-потомки получили только около 1% исходного белка, меченного 35S, однако они же обнаружили около 30% метки 32P.
Как известно, фаг Т2 является вирусом, инфицирующим бактерию E. coli. фаговые частицы абсорбируются на наружной поверхности клетки, их материал проникает внутрь и примерно через 20 минут бактерия лизируется, освобождая большое количество фаговых частиц - потомков. В 1952 году Альфред Херши и Марта Чейз инфицировали бактерии фагами Т2, которые были мечены радиоактивными соединениями: ДНК - с помощью 32P. Белковая часть фага - 35S. После инфекции бактерии фагами, с помощью центрифугирования удалось выделить две фракции: пустые белковые оболочки фага и бактерии, инфицированных фаговой ДНК. Оказалось, что 80% метки 35S осталась в пустых фаговых оболочках, а 70% метки 32P - в инфицированных бактериях. Фаги-потомки получили только около 1% исходного белка, меченного 35S, однако они же обнаружили около 30% метки 32P.